Lasix 40mg, 100mg Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Lasix a jak se používá?
Lasix je lék na předpis používaný k léčbě příznaků zadržování tekutin (edému) u jedinců s městnavým srdečním selháním, onemocněním jater nebo ledvin. Lasix lze užívat samostatně nebo s jinými léky.
Lasix patří do třídy léků nazývaných Diuretika, Loop.
Není známo, zda je Lasix 40 mg bezpečný a účinný u dětí mladších 1 roku při použití k léčbě rezistentní hypertenze.
Jaké jsou možné vedlejší účinky Lasix 40 mg?
Lasix 40 mg může způsobit závažné nežádoucí účinky, včetně:
- točení hlavy,
- zvoní ti v uších,
- ztráta sluchu,
- svalové křeče nebo kontrakce,
- bledá kůže,
- snadná tvorba modřin,
- neobvyklé krvácení,
- zvýšená žízeň,
- zvýšené močení,
- suchá ústa,
- ovocný zápach dechu,
- malé nebo žádné močení,
- otoky nohou nebo kotníků,
- cítit se unaveně,
- dušnost,
- ztráta chuti k jídlu,
- bolest v horní části žaludku,
- nevolnost,
- zvracení,
- tmavá moč,
- zežloutnutí kůže nebo očí (žloutenka),
- ospalost,
- pocit nervozity,
- pocit nejistoty,
- nepravidelný srdeční tep,
- chvění v tvé hrudi,
- necitlivost nebo mravenčení,
- svalové křeče a
- svalová slabost nebo pocit ochablosti
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější vedlejší účinky přípravku Lasix 40 mg patří:
- průjem,
- zácpa,
- ztráta chuti k jídlu,
- necitlivost nebo mravenčení,
- bolest hlavy,
- závratě a
- rozmazané vidění
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky Lasix. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
VAROVÁNÍ
LASIX® (furosemid) je silné diuretikum, které, pokud je podáváno v nadměrném množství, může vést k hluboké diuréze s deplecí vody a elektrolytů. Proto je nutný pečlivý lékařský dohled a dávka a dávkovací schéma musí být přizpůsobeny individuálním potřebám pacienta. (Viz DÁVKOVÁNÍ A PODÁVÁNÍ.)
POPIS
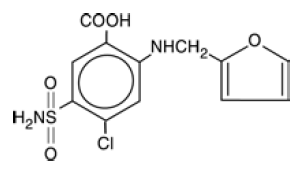
LASIX® je diuretikum, což je derivát kyseliny anthranilové. LASIX 100 mg tablety pro perorální podání obsahují jako účinnou látku furosemid a následující neaktivní složky: monohydrát laktózy NF, stearát hořečnatý NF, škrob NF, mastek USP a koloidní oxid křemičitý NF. Chemicky se jedná o kyselinu 4-chlor-N-furfuryl-5-sulfamoylanthranilovou. LASIX je dostupný ve formě bílých tablet pro perorální podání v dávkových silách 20, 40 a 80 mg. Furosemid je bílý až téměř bílý krystalický prášek bez zápachu. Je prakticky nerozpustný ve vodě, těžce rozpustný v alkoholu, snadno rozpustný ve zředěných alkalických roztocích a nerozpustný ve zředěných kyselinách.
Registrační číslo CAS je 54-31-9.
Strukturní vzorec je následující:
INDIKACE
Otok
LASIX je indikován u dospělých a dětských pacientů k léčbě edému spojeného s městnavým srdečním selháním, cirhózou jater a onemocněním ledvin, včetně nefrotického syndromu. LASIX 100 mg je zvláště užitečný, když je požadována látka s vyšším diuretickým potenciálem.
Hypertenze
Perorální LASIX 40 mg lze u dospělých použít k léčbě hypertenze samostatně nebo v kombinaci s jinými antihypertenzivy. Hypertenzní pacienti, kteří nemohou být adekvátně kontrolováni thiazidy, pravděpodobně také nebudou adekvátně kontrolováni samotným LASIXem.
DÁVKOVÁNÍ A PODÁVÁNÍ
Otok
Terapie by měla být individualizována podle odpovědi pacienta, aby se dosáhlo maximální terapeutické odpovědi a aby se stanovila minimální dávka potřebná k udržení této odpovědi.
Dospělí
Obvyklá počáteční dávka přípravku LASIX je 20 až 80 mg podaná v jedné dávce. Obvykle následuje rychlá diuréza. V případě potřeby lze stejnou dávku podat o 6 až 8 hodin později nebo lze dávku zvýšit. Dávka může být zvýšena o 20 nebo 40 mg a podána nejdříve 6 až 8 hodin po předchozí dávce, dokud se nedosáhne požadovaného diuretického účinku. Individuálně stanovená jednotlivá dávka by se pak měla podávat jednou nebo dvakrát denně (např. v 8:00 a 14:00). U pacientů s klinicky závažnými edematózními stavy lze dávku LASIX 100 mg opatrně titrovat až na 600 mg/den.
Edém lze nejúčinněji a bezpečně mobilizovat podáváním LASIX 100 mg ve 2 až 4 po sobě jdoucích dnech každý týden.
Při dlouhodobém podávání dávek přesahujících 80 mg/den je zvláště vhodné pečlivé klinické sledování a laboratorní sledování. (Vidět OPATŘENÍ : Laboratorní testy .)
Geriatričtí pacienti
Obecně platí, že výběr dávky pro staršího pacienta by měl být opatrný, obvykle začíná na spodní hranici dávkovacího rozmezí (viz OPATŘENÍ : Geriatrické použití ).
Dětští pacienti
Obvyklá počáteční dávka perorálního LASIX 40 mg u pediatrických pacientů je 2 mg/kg tělesné hmotnosti, podaná v jedné dávce. Není-li diuretická odpověď po úvodní dávce uspokojivá, lze dávku zvýšit o 1 nebo 2 mg/kg nejdříve 6 až 8 hodin po předchozí dávce. Dávky vyšší než 6 mg/kg tělesné hmotnosti se nedoporučují. Při udržovací léčbě u pediatrických pacientů by měla být dávka upravena na minimální účinnou hladinu.
Hypertenze
Terapie by měla být individualizována podle pacientovy odpovědi, aby se dosáhlo maximální terapeutické odpovědi a aby se stanovila minimální dávka potřebná k udržení terapeutické odpovědi.
Dospělí
Obvyklá počáteční dávka přípravku LASIX pro hypertenzi je 80 mg, obvykle rozdělená na 40 mg dvakrát denně. Dávkování by pak mělo být upraveno podle odpovědi. Pokud odpověď není uspokojivá, přidejte další antihypertenziva.
Změny krevního tlaku musí být pečlivě sledovány, pokud se LASIX 40 mg užívá s jinými antihypertenzivy, zejména během počáteční léčby. Aby se zabránilo nadměrnému poklesu krevního tlaku, měla by být při přidání přípravku LASIX 100 mg k režimu snížena dávka jiných přípravků alespoň o 50 procent. Vzhledem k tomu, že krevní tlak klesá pod potenciační účinek přípravku LASIX 100 mg, může být nutné další snížení dávkování nebo dokonce vysazení jiných antihypertenziv.
Geriatričtí pacienti
Obecně platí, že výběr dávky a úprava dávky u starších pacientů by měla být opatrná, obvykle začíná na spodní hranici dávkovacího rozmezí (viz OPATŘENÍ : Geriatrické použití ).
JAK DODÁVÁNO
LASIX (furosemid) tablety 20 mg jsou dodávány jako bílé, oválné, monogramové tablety v lahvičkách po 100 ( NDC 0039-0067-10) a 1000 ( NDC 0039-0067-70). 20mg tablety mají na jedné straně potisk „Lasix®“.
LASIX tablety 40 mg jsou dodávány jako bílé, kulaté, monogramované tablety s půlicí rýhou v lahvičkách po 100 ( NDC 0039-0060-13), 500 ( NDC 0039-0060-50) a 1000 ( NDC 0039-0060-70). 40mg tablety mají na jedné straně potisk „Lasix® 40“.
LASIX tablety 80 mg jsou dodávány jako bílé, kulaté, monogramové tablety s fasetovaným okrajem v lahvičkách po 50 ( NDC 0039-0066-05) a 500 ( NDC 0039-0066-50). 80mg tablety mají na jedné straně potisk „Lasix® 80“.
Poznámka: Dávkujte v dobře uzavřených, světlu odolných nádobách. Vystavení světlu může způsobit mírné zbarvení. Odbarvené tablety by se neměly vydávat.
Testováno podle USP Dissolution Test 2
Skladujte při teplotě 25 °C (77 °F); povoleny výchylky do 15-30°C (59-86°F). [Vidět USP řízená pokojová teplota .]
Vyrobeno pro: sanofi-aventis US LLC Bridgewater, NJ 08807. Společnost Sanofi.. Revize: březen 2016
VEDLEJŠÍ EFEKTY
Nežádoucí účinky jsou kategorizovány níže podle orgánových systémů a uvedeny podle klesající závažnosti.
Gastrointestinální systém reakce
Systémové hypersenzitivní reakce
Reakce centrálního nervového systému
Hematologické reakce
Dermatologicko-hypersenzitivní reakce
Kardiovaskulární reakce
Jiné reakce
Kdykoli jsou nežádoucí účinky středně závažné nebo závažné, dávka přípravku LASIX by měla být snížena nebo léčba ukončena.
DROGOVÉ INTERAKCE
LASIX 100 mg může zvýšit ototoxický potenciál aminoglykosidových antibiotik, zejména v případě poruchy funkce ledvin. S výjimkou život ohrožujících situací se této kombinaci vyhněte.
LASIX by se neměl používat současně s kyselinou etakrynovou kvůli možnosti ototoxicity. U pacientů, kteří dostávají vysoké dávky salicylátů současně s přípravkem LASIX, jako u revmatického onemocnění, může dojít při nižších dávkách k toxicitě salicylátu kvůli kompetitivním místům vylučování ledvinami.
Při současném podávání cisplatiny a LASIXu existuje riziko ototoxických účinků. Kromě toho může být nefrotoxicita nefrotoxických léků, jako je cisplatina, zvýšena, pokud se LASIX 100 mg nepodává v nižších dávkách a s pozitivní bilancí tekutin při použití k dosažení forsírované diurézy během léčby cisplatinou.
LASIX má tendenci antagonizovat relaxační účinek tubokurarinu na kosterní svalstvo a může potencovat účinek sukcinylcholinu.
Lithium by se obecně nemělo podávat s diuretiky, protože snižují renální clearance lithia a zvyšují riziko toxicity lithia.
LASIX 40 mg v kombinaci s inhibitory angiotenzin konvertujícího enzymu nebo blokátory receptoru angiotenzinu II může vést k těžké hypotenzi a zhoršení funkce ledvin, včetně selhání ledvin. Může být nezbytné přerušení nebo snížení dávkování LASIX, inhibitorů angiotenzin konvertujícího enzymu nebo blokátorů receptorů pro angiotenzin.
K potenciaci dochází u gangliových nebo periferních adrenergních blokátorů.
LASIX 40 mg může snížit arteriální citlivost na norepinefrin. Norepinefrin však může být stále účinně používán.
Současné podávání sukralfátu a LASIX 100 mg tablet může snížit natriuretické a antihypertenzní účinky LASIX. Pacienti užívající oba léky by měli být pečlivě sledováni, aby se zjistilo, zda je dosaženo požadovaného diuretického a/nebo antihypertenzního účinku přípravku LASIX 40 mg. Mezi užitím LASIX 100 mg a sukralfátu by měly být alespoň dvě hodiny.
ojedinělých případech může intravenózní podání přípravku LASIX do 24 hodin po užití chloralhydrátu vést k zrudnutí, záchvatům pocení, neklidu, nevolnosti, zvýšení krevního tlaku a tachykardii. Použití LASIX 40 mg současně s chloralhydrátem se proto nedoporučuje.
Fenytoin přímo interferuje s renálním působením LASIX. Existují důkazy, že léčba fenytoinem vede ke snížení intestinální absorpce LASIXu a následně ke snížení maximálních sérových koncentrací furosemidu.
Methotrexát a další léky, které podobně jako LASIX podléhají významné renální tubulární sekreci, mohou snížit účinek LASIXu. Naopak LASIX 100 mg může snížit renální eliminaci jiných léků, které podléhají tubulární sekreci. Léčba vysokými dávkami jak LASIX, tak těchto dalších léků může vést ke zvýšeným sérovým hladinám těchto léků a může potencovat jejich toxicitu, stejně jako toxicitu LASIX.
LASIX může zvýšit riziko nefrotoxicity vyvolané cefalosporiny i při mírném nebo přechodném poškození ledvin.
Současné užívání cyklosporinu a LASIX 40 mg je spojeno se zvýšeným rizikem dnavé artritidy sekundárně k hyperurekémii vyvolané LASIXem a cyklosporinovým poškozením renální exkrece urátu.
Vysoké dávky (> 80 mg) furosemidu mohou inhibovat vazbu hormonů štítné žlázy na nosné proteiny a vést k přechodnému zvýšení volných hormonů štítné žlázy, po kterém následuje celkový pokles hladin celkových hormonů štítné žlázy.
Jedna studie u šesti subjektů prokázala, že kombinace furosemidu a kyseliny acetylsalicylové dočasně snižuje clearance kreatininu u pacientů s chronickou renální insuficiencí. Existují kazuistiky pacientů, u kterých došlo ke zvýšení BUN, sérového kreatininu a sérového draslíku a zvýšení tělesné hmotnosti, když byl furosemid používán ve spojení s NSAID.
Literární zprávy naznačují, že současné podávání indometacinu může u některých pacientů snížit natriuretické a antihypertenzní účinky LASIX (furosemid) inhibicí syntézy prostaglandinů. Indomethacin může také ovlivnit plazmatické hladiny reninu, vylučování aldosteronu a hodnocení profilu reninu. Pacienti užívající indomethacin i LASIX by měli být pečlivě sledováni, aby se zjistilo, zda je dosaženo požadovaného diuretického a/nebo antihypertenzního účinku přípravku LASIX 100 mg.
VAROVÁNÍ
pacientů s jaterní cirhózou a ascitem je nejlepší zahájit léčbu přípravkem LASIX 100 mg v nemocnici. U jaterního kómatu a při stavech deplece elektrolytů by léčba neměla být zahájena, dokud se základní stav nezlepší. Náhlé změny rovnováhy tekutin a elektrolytů u pacientů s cirhózou mohou vyvolat jaterní kóma; proto je během období diurézy nutné přísné sledování. Doplňkový chlorid draselný a v případě potřeby antagonista aldosteronu jsou užitečné v prevenci hypokalemie a metabolické alkalózy.
Pokud se během léčby těžkého progresivního onemocnění ledvin objeví narůstající azotemie a oligurie, je třeba léčbu přípravkem LASIX 100 mg přerušit.
Byly hlášeny případy tinnitu a reverzibilní nebo nevratné poruchy sluchu a hluchoty. Zprávy obvykle naznačují, že ototoxicita LASIX je spojena s rychlou injekcí, závažným poškozením ledvin, použitím vyšších než doporučených dávek, hypoproteinémií nebo současnou terapií aminoglykosidovými antibiotiky, kyselinou etakrynovou nebo jinými ototoxickými léky. Pokud se lékař rozhodne pro vysokodávkovou parenterální terapii, doporučuje se kontrolovaná intravenózní infuze (u dospělých byla použita rychlost infuze nepřesahující 4 mg LASIX za minutu). (Vidět OPATŘENÍ : DROGOVÉ INTERAKCE )
OPATŘENÍ
Všeobecné
Nadměrná diuréza může způsobit dehydrataci a snížení objemu krve s oběhovým kolapsem a možná vaskulární trombózou a embolií, zejména u starších pacientů. Stejně jako u jiných účinných diuretik může během léčby přípravkem LASIX 100 mg dojít k depleci elektrolytů, zejména u pacientů, kteří dostávají vyšší dávky a omezený příjem soli. Při léčbě LASIX se může vyvinout hypokalémie, zejména při rychlé diuréze, nedostatečném perorálním příjmu elektrolytů, při cirhóze nebo při současném užívání kortikosteroidů, ACTH, lékořice ve velkých množstvích nebo při dlouhodobém užívání laxativ. Digitalisová terapie může zvýraznit metabolické účinky hypokalémie, zejména účinky na myokard.
Všichni pacienti léčení LASIX by měli být sledováni kvůli těmto známkám nebo příznakům nerovnováhy tekutin nebo elektrolytů (hyponatremie, hypochloremická alkalóza, hypokalémie, hypomagnezémie nebo hypokalcémie): sucho v ústech, žízeň, slabost, letargie, ospalost, neklid, svalové bolesti nebo křeče, svalová únava, hypotenze, oligurie, tachykardie, arytmie nebo gastrointestinální poruchy, jako je nauzea a zvracení. Bylo pozorováno zvýšení hladiny glukózy v krvi a změny glukózových tolerančních testů (s abnormalitami hladiny cukru nalačno a 2 hodiny po jídle) a vzácně byla hlášena precipitace diabetes mellitus.
pacientů se závažnými příznaky retence moči (z důvodu poruch vyprazdňování močového měchýře, hyperplazie prostaty, zúžení uretry) může podávání furosemidu způsobit akutní retenci moči související se zvýšenou tvorbou a zadržováním moči. Tito pacienti tedy vyžadují pečlivé sledování, zejména během počátečních fází léčby.
U pacientů s vysokým rizikem radiokontrastní nefropatie může LASIX 100 mg vést k vyššímu výskytu zhoršení renálních funkcí po podání radiokontrastní látky ve srovnání s vysoce rizikovými pacienty, kteří před podáním radiokontrastu dostávali pouze intravenózní hydrataci.
U pacientů s hypoproteinémií (např. spojenou s nefrotickým syndromem) může být účinek přípravku LASIX 40 mg oslaben a jeho ototoxicita potencována.
Může se objevit asymptomatická hyperurikémie a vzácně se může urychlit dna.
Pacienti alergičtí na sulfonamidy mohou být také alergičtí na LASIX. Existuje možnost exacerbace nebo aktivace systémového lupus erythematodes.
Stejně jako u mnoha jiných léků by pacienti měli být pravidelně sledováni pro možný výskyt krevních dyskrazií, poškození jater nebo ledvin nebo jiných idiosynkratických reakcí.
Laboratorní testy
Sérové elektrolyty (zejména draslík), CO2, kreatinin a BUN by měly být často stanovovány během prvních několika měsíců léčby přípravkem LASIX 100 mg a poté pravidelně. Stanovení elektrolytů v séru a moči je zvláště důležité, když pacient silně zvrací nebo dostává parenterální tekutiny. Abnormality by měly být opraveny nebo lék dočasně vysazen. Jiné léky mohou také ovlivnit sérové elektrolyty.
Může dojít k reverzibilnímu zvýšení BUN a je spojeno s dehydratací, které je třeba se vyhnout, zejména u pacientů s renální insuficiencí.
diabetiků užívajících LASIX 100 mg by měla být pravidelně kontrolována hladina glukózy v moči a krvi, a to i u pacientů s podezřením na latentní diabetes.
LASIX 40 mg může snížit sérové hladiny vápníku (vzácně byly hlášeny případy tetanie) a hořčíku. V souladu s tím by měly být pravidelně stanovovány hladiny těchto elektrolytů v séru.
U předčasně narozených dětí může LASIX 100 mg vyvolat nefrokalcinózu/nefrolitiázu, proto je nutné sledovat renální funkce a provést ultrasonografii ledvin. (Vidět OPATŘENÍ : Pediatrické použití )
Karcinogeneze, mutageneze, zhoršení plodnosti
Furosemid byl testován na karcinogenitu perorálním podáním u jednoho kmene myší a jednoho kmene potkanů. Malý, ale významně zvýšený výskyt karcinomů mléčné žlázy se vyskytl u myších samic při dávce 17,5násobku maximální dávky pro člověka 600 mg. Při dávce 15 mg/kg (o něco vyšší, než je maximální dávka pro člověka), ale ne při dávce 30 mg/kg, došlo u samců potkanů k okrajovému zvýšení výskytu méně častých nádorů.
Furosemid neměl mutagenní aktivitu v různých kmenech Salmonella typhimurium, když byl testován v přítomnosti nebo nepřítomnosti in vitro metabolického aktivačního systému, a byl pochybně pozitivní na genovou mutaci v buňkách myšího lymfomu v přítomnosti potkaních jater S9 v nejvyšší testované dávce. Furosemid neindukoval výměnu sesterských chromatid v lidských buňkách in vitro, ale jiné studie chromozomálních aberací v lidských buňkách in vitro poskytly protichůdné výsledky. V buňkách čínského křečka indukoval chromozomální poškození, ale byl sporně pozitivní na výměnu sesterských chromatid. Studie o indukci chromozomálních aberací u myší furosemidem byly neprůkazné. Moč potkanů léčených tímto lékem neindukovala genovou konverzi u Saccharomyces cerevisiae.
LASIX (furosemid) nezpůsobil žádné poškození fertility u samců nebo samic potkanů při dávce 100 mg/kg/den (maximální účinná diuretická dávka u potkana a 8násobek maximální dávky pro člověka 600 mg/den).
Těhotenství
Kategorie těhotenství C – Bylo prokázáno, že furosemid způsobuje nevysvětlitelná úmrtí matek a potraty u králíků při 2, 4 a 8násobku maximální doporučené dávky pro člověka. Neexistují žádné adekvátní a dobře kontrolované studie u těhotných žen. LASIX by měl být používán během těhotenství pouze tehdy, pokud potenciální přínos ospravedlňuje potenciální riziko pro plod.
Léčba během těhotenství vyžaduje sledování růstu plodu kvůli možné vyšší porodní hmotnosti.
Účinky furosemidu na embryonální a fetální vývoj a na březí samice byly studovány u myší, potkanů a králíků.
Furosemid způsobil nevysvětlitelná úmrtí matek a potraty u králíků v nejnižší dávce 25 mg/kg (dvojnásobek maximální doporučené dávky pro člověka 600 mg/den). V jiné studii dávka 50 mg/kg (čtyřnásobek maximální doporučené dávky pro člověka 600 mg/den) také způsobila smrt matek a potraty, když byla podávána králíkům mezi 12. a 17. dnem březosti. Ve třetí studii žádná z březích králíků nepřežila dávku 100 mg/kg. Údaje z výše uvedených studií naznačují fetální letalitu, která může předcházet úmrtí matek.
Výsledky studie na myších a jedné ze tří studií na králících také ukázaly zvýšený výskyt a závažnost hydronefrózy (roztažení ledvinové pánvičky a v některých případech močovodů) u plodů pocházejících z léčených samic ve srovnání s výskytem u plodů z kontrolní skupiny.
Kojící matky
Vzhledem k tomu, že se objevuje v mateřském mléce, je třeba dbát opatrnosti, když je LASIX podáván kojící matce.
LASIX 40 mg může inhibovat laktaci.
Pediatrické použití
předčasně narozených dětí může LASIX vyvolat nefrokalcinózu/nefrolitiázu. Nefrokalcinóza/nefrolitiáza byla také pozorována u dětí mladších 4 let bez anamnézy nedonošených dětí, které byly chronicky léčeny LASIXem. U pediatrických pacientů užívajících LASIX by mělo být zváženo monitorování renálních funkcí a renální ultrasonografie.
Pokud je LASIX 40 mg podáván předčasně narozeným dětem během prvních týdnů života, může zvýšit riziko přetrvávání otevřeného ductus arteriosus
Geriatrické použití
Kontrolované klinické studie LASIX 100 mg nezahrnovaly dostatečný počet subjektů ve věku 65 let a více, aby bylo možné určit, zda reagují odlišně od mladších subjektů. Jiné hlášené klinické zkušenosti nezjistily rozdíly v odpovědích mezi staršími a mladšími pacienty. Obecně by měl být výběr dávky pro starší pacienty opatrný, obvykle začínající na spodní hranici dávkovacího rozmezí, což odráží vyšší frekvenci snížené funkce jater, ledvin nebo srdce a souběžného onemocnění nebo jiné lékové terapie.
Je známo, že tento lék je v podstatě vylučován ledvinami a riziko toxických reakcí na tento lék může být větší u pacientů s poruchou funkce ledvin. Protože u starších pacientů je pravděpodobnější, že budou mít sníženou funkci ledvin, je třeba věnovat pozornost výběru dávky a může být užitečné sledovat funkci ledvin. (Vidět OPATŘENÍ : Všeobecné a DÁVKOVÁNÍ A PODÁVÁNÍ .)
PŘEDÁVKOVAT
Hlavní známky a příznaky předávkování přípravkem LASIX 40 mg jsou dehydratace, snížení objemu krve, hypotenze, nerovnováha elektrolytů, hypokalémie a hypochloremická alkalóza a jsou rozšířením jeho diuretického účinku.
Akutní toxicita LASIX 100 mg byla stanovena u myší, potkanů a psů. U všech tří přesáhla perorální LD50 1000 mg/kg tělesné hmotnosti, zatímco intravenózní LD50 se pohybovala od 300 do 680 mg/kg. Akutní intragastrická toxicita u novorozených potkanů je 7 až 10krát vyšší než u dospělých potkanů.
Koncentrace LASIXu v biologických tekutinách spojená s toxicitou nebo smrtí není známa.
Léčba předávkování je podpůrná a spočívá v náhradě nadměrných ztrát tekutin a elektrolytů. Je třeba často měřit sérové elektrolyty, hladinu oxidu uhličitého a krevní tlak. U pacientů s obstrukcí vývodu močového měchýře (jako je hypertrofie prostaty) musí být zajištěna adekvátní drenáž.
Hemodialýza neurychluje eliminaci furosemidu.
KONTRAINDIKACE
LASIX 40 mg je kontraindikován u pacientů s anurií a u pacientů s anamnézou přecitlivělosti na furosemid.
KLINICKÁ FARMAKOLOGIE
Při zkoumání mechanismu účinku LASIX byly použity mikropunkční studie u potkanů, experimenty se zastavením průtoku u psů a různé studie clearance u lidí i experimentálních zvířat. Bylo prokázáno, že LASIX inhibuje primárně absorpci sodíku a chloridu nejen v proximálních a distálních tubulech, ale také v Henleově kličce. Vysoký stupeň účinnosti je z velké části způsoben jedinečným místem působení. Účinek na distální tubul je nezávislý na jakémkoli inhibičním účinku na karboanhydrázu a aldosteron.
Nedávné důkazy naznačují, že furosemid-glukuronid je jediným nebo alespoň hlavním biotransformačním produktem furosemidu u člověka. Furosemid se rozsáhle váže na plazmatické proteiny, především na albumin. Plazmatické koncentrace v rozmezí od 1 do 400 μg/ml jsou u zdravých jedinců vázány z 91 až 99 %. Nenavázaná frakce dosahuje v terapeutických koncentracích v průměru 2,3 až 4,1 %.
Nástup diurézy po perorálním podání je do 1 hodiny. Vrchol účinku nastává během první nebo druhé hodiny. Délka diuretického účinku je 6 až 8 hodin.
normálních mužů nalačno je průměrná biologická dostupnost furosemidu z tablet LASIX a perorálního roztoku LASIX 64 % a 60 % ve srovnání s intravenózní injekcí léku. Přestože se furosemid rychleji vstřebává z perorálního roztoku (50 minut) než z tablety (87 minut), vrcholové plazmatické hladiny a plocha pod křivkami plazmatické koncentrace-čas se významně neliší. Maximální plazmatické koncentrace se zvyšují se zvyšující se dávkou, ale časy nejvyšších hodnot se mezi dávkami neliší. Terminální poločas furosemidu je přibližně 2 hodiny.
Po intravenózní injekci se močí vylučuje podstatně více furosemidu než po tabletě nebo perorálním roztoku. Mezi těmito dvěma perorálními formulacemi nejsou žádné významné rozdíly v množství nezměněného léčiva vyloučeného močí.
Geriatrická populace
Vazba furosemidu na albumin může být u starších pacientů snížena. Furosemid se vylučuje převážně nezměněný močí. Renální clearance furosemidu po intravenózním podání u starších zdravých mužů (60-70 let) je statisticky významně nižší než u mladších zdravých mužů (20-35 let). Počáteční diuretický účinek furosemidu u starších subjektů je ve srovnání s mladšími subjekty snížen. (Vidět OPATŘENÍ : Geriatrické použití .)
INFORMACE PRO PACIENTA
Pacienti užívající LASIX by měli být upozorněni, že mohou pociťovat příznaky nadměrné ztráty tekutin a/nebo elektrolytů. Posturální hypotenzi, ke které někdy dochází, lze obvykle zvládnout pomalým vstáváním. Ke kontrole nebo zamezení hypokalemie mohou být zapotřebí doplňky draslíku a/nebo dietní opatření.
Pacienti s diabetes mellitus by měli být informováni, že furosemid může zvyšovat hladiny glukózy v krvi, a tím ovlivnit testy glukózy v moči. Kůže některých pacientů může být při užívání furosemidu citlivější na účinky slunečního záření.
Hypertonici by se měli vyhýbat lékům, které mohou zvyšovat krevní tlak, včetně volně prodejných přípravků na potlačení chuti k jídlu a na příznaky nachlazení.
