Yasmin 3/0.03mg Drospirenone Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Yasmin a jak se používá?
Yasmin je lék na předpis používaný k léčbě příznaků středně těžkého akné, premenstruační dysforické poruchy (PMDD) ak prevenci těhotenství. Yasmin lze užívat samostatně nebo s jinými léky.
Yasmin patří do třídy léků nazývaných Akné, Systémové, Estrogeny/Progestiny, Antikoncepce, Orální.
Není známo, zda je přípravek Yasmin 3 mg bezpečný a účinný u dětí mladších 14 let.
Jaké jsou možné vedlejší účinky přípravku Yasmin?
Yasmin 0,03 mg může způsobit závažné nežádoucí účinky, včetně:
- náhlá necitlivost nebo slabost,
- náhlé silné bolesti hlavy,
- nezřetelná řeč,
- problémy se zrakem,
- potíže s rovnováhou,
- náhlá ztráta zraku,
- bodavá bolest na hrudi,
- dušnost,
- vykašlávání krve,
- bolest nebo teplo v jedné nebo obou nohách,
- bolest nebo tlak na hrudi,
- bolest šířící se do čelisti nebo ramene,
- nevolnost,
- pocení,
- ztráta chuti k jídlu,
- bolest v horní části žaludku,
- únava,
- tmavá moč,
- stolice hliněné barvy,
- zežloutnutí kůže nebo očí (žloutenka),
- rozmazané vidění,
- bušení do krku nebo uší,
- otoky rukou, kotníků nebo nohou,
- změna ve vzoru nebo závažnosti migrénových bolestí hlavy,
- problémy se spánkem,
- slabost,
- pocit únavy a
- změny nálady
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější nežádoucí účinky přípravku Yasmin 3 mg patří:
- nevolnost,
- zvracení,
- citlivost prsou,
- bolest hlavy,
- změny nálady,
- pocit únavy nebo podrážděnosti,
- přibývání na váze,
- změny ve vaší menstruaci a
- snížená chuť na sex
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky přípravku Yasmin. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
VAROVÁNÍ
KOUŘENÍ CIGARET A VÁŽNÉ KARDIOVASKULÁRNÍ PŘÍPADY
Kouření cigaret zvyšuje riziko závažných kardiovaskulárních příhod při užívání kombinované perorální antikoncepce (COC). Toto riziko se zvyšuje s věkem, zejména u žen nad 35 let, as počtem vykouřených cigaret. Z tohoto důvodu by COC neměly užívat ženy, které jsou starší 35 let a kouří (viz KONTRAINDIKACE).
POPIS
Tablety Yasmin (drospirenon/ethinylestradiol) poskytují režim perorální antikoncepce sestávající z 28 potahovaných tablet, které obsahují složky specifikované pro každou tabletu níže:
- 21 žlutých tablet, každá obsahující 3 mg DRSP a 0,03 mg EE
- 7 inertních bílých tablet
Neaktivní složky ve žlutých tabletách jsou monohydrát laktózy NF, kukuřičný škrob NF, předbobtnalý škrob NF, povidon 25000 NF, magnesium-stearát NF, hypromelóza USP, makrogol 6000 NF, oxid titaničitý USP, mastek USP a pigment oxidu železitého, žlutá NF. Bílé inertní potahované tablety obsahují monohydrát laktózy NF, mikrokrystalickou celulózu, stearát hořečnatý NF, hypromelózu USP, mastek USP a oxid titaničitý USP.
Drospirenon (6R,7R,8R,9S,10R,13S,14S,15S,16S,17S)-1,3',4',6,6a,7,8,9,10,11,12 ,13,14,15,15a,16-hexadekahydro10,13-dimethylspiro-[17H-dicyklopropa-[6,7:15,16] cyklopenta[a]fenantren-17,2'(5H)-furan]- 3,5'(2H)-dion) je syntetická progestační sloučenina a má molekulovou hmotnost 366,5 a molekulový vzorec C24H30O3.
Ethinylestradiol (19-nor-17α-pregna 1,3,5(10)-trien-20-yn-3,17-diol) je syntetická estrogenní sloučenina s molekulovou hmotností 296,4 a molekulárním vzorcem C20H24O2.
Strukturní vzorce jsou následující:
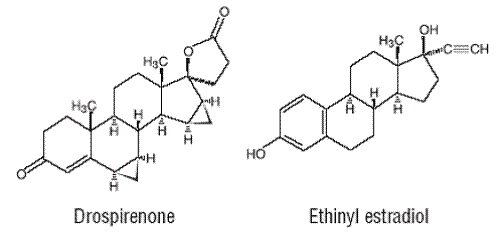
INDIKACE
Yasmin® je indikován pro ženy k prevenci těhotenství.
DÁVKOVÁNÍ A PODÁVÁNÍ
Jak užívat Yasmin
Užívejte jednu tabletu ústy každý den ve stejnou dobu. Míra selhání se může zvýšit, když jsou pilulky vynechány nebo užívány nesprávně.
Pro dosažení maximální antikoncepční účinnosti je třeba Yasmin užívat podle pokynů, v pořadí uvedeném na blistru. Jednotlivé vynechané pilulky je třeba užít, jakmile si vzpomenete.
Jak spustit Yasmin
Poučte pacientku, aby začala užívat přípravek Yasmin buď první den menstruace (začátek 1. dne) nebo první neděli po začátku menstruace (začátek v neděli).
Den 1 Start
Během prvního cyklu užívání přípravku Yasmin poučte pacientku, aby užívala jeden žlutý přípravek Yasmin 3 mg denně, počínaje 1. dnem menstruačního cyklu. (První den menstruace je Den 1.) Měla by užívat jednu žlutou Yasmin 0,03 mg denně po dobu 21 po sobě jdoucích dnů, poté jednu bílou tabletu denně ve dnech 22 až 28. Yasmin 0,03 mg by měla být užívána v pořadí uvedeném na obalu každý den ve stejnou dobu, nejlépe po večeři nebo před spaním s trochou tekutiny, podle potřeby. Yasmin 3 mg lze užívat bez ohledu na jídlo. Pokud se Yasmin poprvé užije později než první den menstruačního cyklu, neměl by být Yasmin považován za účinný jako antikoncepční prostředek dříve, než po prvních 7 po sobě jdoucích dnech podávání přípravku. Poučte pacientku, aby během prvních 7 dnů používala jako zálohu nehormonální antikoncepci. Je třeba vzít v úvahu možnost ovulace a početí před zahájením léčby.
Nedělní začátek
Během prvního cyklu užívání přípravku Yasmin 3 mg poučte pacientku, aby užívala jeden žlutý přípravek Yasmin 0,03 mg denně, počínaje první neděli po začátku menstruace. Měla by užívat jednu žlutou tabletu Yasmin denně po dobu 21 po sobě jdoucích dnů a následně jednu bílou tabletu denně ve dnech 22 až 28. Yasmin by měla být užívána v pořadí uvedeném na obalu každý den ve stejnou dobu, nejlépe po večeři nebo před spaním. s trochou tekutiny, podle potřeby. Yasmin lze užívat bez ohledu na jídlo. Přípravek Yasmin 3 mg by neměl být považován za účinný jako antikoncepční prostředek, dokud nebude po prvních 7 po sobě jdoucích dnech podávání přípravku. Poučte pacientku, aby během prvních 7 dnů používala jako zálohu nehormonální antikoncepci. Je třeba vzít v úvahu možnost ovulace a početí před zahájením léčby.
Pacientka by měla zahájit svůj další a všechny následující 28denní režimy Yasmin 0,03 mg ve stejný den v týdnu, kdy zahájila první režim, podle stejného rozvrhu. Měla by začít užívat své žluté tablety následující den po požití poslední bílé tablety, bez ohledu na to, zda menstruace proběhla nebo ještě probíhá. Kdykoli je následný cyklus Yasminu zahájen později než den po podání poslední bílé tablety, měla by pacientka používat jinou metodu antikoncepce, dokud nebude užívat žlutou Yasmin 3 mg denně po dobu sedmi po sobě jdoucích dnů.
Při přechodu z jiné antikoncepční pilulky
Při přechodu z jiné antikoncepční pilulky by měla být Yasmin 3 mg zahájena ve stejný den, kdy by bylo zahájeno užívání nového balení předchozí perorální antikoncepce.
Při přechodu z jiné metody než antikoncepční pilulky
Při přechodu z transdermální náplasti nebo vaginálního kroužku by měla být Yasmin zahájena v době, kdy měla být další aplikace. Při přechodu z injekce by měla být Yasmin zahájena v době, kdy měla být podána další dávka. Při přechodu z nitroděložní antikoncepce nebo implantátu by měla být Yasmin zahájena v den vyjmutí.
Krvácení z vysazení se obvykle objeví do 3 dnů po užití poslední žluté tablety. Pokud se během užívání přípravku Yasmin objeví špinění nebo krvácení z průniku, poučte pacienta, aby pokračoval v užívání přípravku Yasmin podle výše popsaného režimu. Poraďte jí, že tento typ krvácení je obvykle přechodný a bezvýznamný; doporučte jí však, že pokud je krvácení trvalé nebo dlouhodobé, měla by se poradit se svým poskytovatelem zdravotní péče.
když je výskyt otěhotnění nízký, pokud se Yasmin 3 mg užívá podle pokynů, pokud se nedostaví krvácení z vysazení, zvažte možnost těhotenství. Pokud pacientka nedodržela předepsané dávkovací schéma (vynechala jednu nebo více aktivních tablet nebo je začala užívat o den později, než měla), zvažte možnost těhotenství v době první vynechané menstruace a proveďte vhodná diagnostická opatření. . Pokud pacientka dodržela předepsaný režim a vynechá dvě po sobě jdoucí menstruace, vylučte těhotenství. Pokud se těhotenství potvrdí, přerušte podávání přípravku Yasmin 3 mg.
Riziko otěhotnění se zvyšuje s každou vynechanou aktivní žlutou tabletou. Další pokyny pro pacienty týkající se vynechaných pilulek naleznete v části „ CO DĚLAT, KDYŽ VÁM POUZE PÁLE “ v sekci FDA-Approved Označení pacienta Pokud se po vynechání tablety objeví krvácení z průniku, bude obvykle přechodné a bez následků. Pokud pacientka vynechá jednu nebo více bílých tablet, měla by být stále chráněna proti otěhotnění za předpokladu, že ve správný den začne užívat nový cyklus žlutých tablet.
U žen po porodu, které nekojí nebo po potratu ve druhém trimestru, začněte s Yasminem nejdříve 4 týdny po porodu kvůli zvýšenému riziku tromboembolie. Pokud pacientka začne s přípravkem Yasmin po porodu a ještě nedostala menstruaci, zhodnoťte možné těhotenství a poučte ji, aby používala další metodu antikoncepce, dokud nebude užívat přípravek Yasmin po dobu 7 po sobě jdoucích dnů.
Poradenství V případě Gastrointestinálních Poruch
V případě silného zvracení nebo průjmu nemusí být absorpce úplná a je třeba použít další antikoncepční opatření. Pokud během 3-4 hodin po užití tablety dojde ke zvracení, lze to považovat za vynechanou tabletu.
JAK DODÁVÁNO
Dávkové formy A Síly
Tablety Yasmin (drospirenon/ethinylestradiol) jsou dostupné v blistrech.
Každý blistr obsahuje 28 potahovaných, kulatých, bikonvexních tablet v následujícím pořadí:
- 21 žlutých tablet, každá obsahující 3 mg drospirenonu (DRSP) a 0,03 mg ethinylestradiolu (EE) s vyraženým „DO“ v pravidelném šestiúhelníku na jedné straně
- 7 inertních bílých tablet s vyraženým „DP“ v pravidelném šestiúhelníku na jedné straně
Skladování A Manipulace
Tablety Yasmin (drospirenon/ethinylestradiol). jsou k dispozici v baleních po třech blistrech ( NDC 50419-402-03).
Potahované tablety jsou zaoblené s bikonvexními plochami, na jedné straně je vyražen pravidelný tvar šestiúhelníku s DO nebo DP.
Každý blistr obsahuje 28 potahovaných tablet v následujícím pořadí:
- 21 kulatých, bikonvexních, žlutých, potahovaných tablet s vyraženým „DO“ v pravidelném šestiúhelníku na jedné straně, každá obsahuje 3 mg drospirenonu a 0,03 mg ethinylestradiolu
- kulatých, bikonvexních, bílých, potahovaných tablet s vyraženým „DP“ v pravidelném šestiúhelníku na jedné straně
Úložný prostor
Skladujte při teplotě 25 °C (77 °F); povoleny výchylky do 15-30°C (59-86°F) [viz USP řízená pokojová teplota ].
Vyrobeno pro: Bayer HealthCare Pharmaceuticals Inc. Whippany, NJ 07981. Vyrobeno v Německu. Revize: květen 2015
VEDLEJŠÍ EFEKTY
Následující závažné nežádoucí účinky při užívání COC jsou diskutovány jinde v označení:
- Závažné kardiovaskulární příhody a mrtvice [viz VAROVÁNÍ V KRABICE a VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Cévní události [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Onemocnění jater [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
Nežádoucí účinky běžně hlášené uživateli COC jsou:
- Nepravidelné děložní krvácení
- Nevolnost
- Citlivost prsou
- Bolest hlavy
Zkušenosti z klinických studií
Vzhledem k tomu, že klinické studie probíhají za velmi odlišných podmínek, nelze pozorované míry nežádoucích reakcí přímo srovnávat s mírami v jiných klinických studiích a nemusí odrážet míry pozorované v praxi.
Poskytnuté údaje odrážejí zkušenosti s používáním přípravku Yasmin (3 mg DRSP/0,03 mg EE) v adekvátních a dobře kontrolovaných studiích antikoncepce (N=2 837). Americká pivotní klinická studie (N=326) byla multicentrická, otevřená studie u zdravých žen ve věku 18-35 let, které byly léčeny až 13 cyklů. Druhá klíčová studie (N=442) byla multicentrická, randomizovaná, otevřená srovnávací evropská studie Yasmin vs. 0,150 mg desogestrel/0,03 mg EE prováděná u zdravých žen ve věku 17-40 let, které byly léčeny až 26 cyklů.
Nejčastějšími nežádoucími účinky (≥ 2 % uživatelek) byly: premenstruační syndrom (13,2 %), bolest hlavy/migréna (10,7 %), bolest/citlivost prsou/nepohodlí (8,3 %), nauzea/zvracení (4,5 %) bolest břicha/ nepohodlí/citlivost (2,3 %) a změny nálady (deprese, depresivní nálada, podrážděnost, změny nálady, změna nálady a ovlivnění lability (2,3 %).
Nežádoucí účinky (≥ 1 %) vedoucí k přerušení studie
2 837 žen 6,7 % přerušilo klinické studie kvůli nežádoucí reakci; nejčastější nežádoucí reakcí vedoucí k přerušení léčby byla bolest hlavy/migréna (1,5 %).
Závažné nežádoucí reakce
Deprese, plicní embolie, toxická kožní erupce a děložní leiomyom.
Postmarketingové zkušenosti
Během užívání přípravku Yasmin po schválení byly zjištěny následující nežádoucí účinky. Protože jsou tyto reakce hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo stanovit příčinnou souvislost s expozicí léku.
Nežádoucí účinky, včetně úmrtí, jsou seskupeny do tříd orgánových systémů a seřazeny podle frekvence.
Cévní poruchy: Venózní a arteriální tromboembolické příhody (včetně plicní embolie, hluboké žilní trombózy, intrakardiální trombózy, trombózy intrakraniálního žilního sinu, trombózy sagitálního sinu, okluze retinální žíly, infarktu myokardu a mrtvice), hypertenze
Poruchy jater a žlučových cest: Onemocnění žlučníku
Poruchy imunitního systému: Přecitlivělost
Poruchy metabolismu a výživy: Hyperkalémie
Poruchy kůže a podkoží: Chloasma
DROGOVÉ INTERAKCE
Chcete-li získat další informace o interakcích s hormonální antikoncepcí nebo o potenciálu změn enzymů, podívejte se na označení všech současně užívaných léků.
Účinky jiných léků na kombinovanou perorální antikoncepci
Látky snižující účinnost COC
Léky nebo rostlinné produkty, které indukují určité enzymy, včetně cytochromu P450 3A4 (CYP3A4), mohou snížit účinnost COC nebo zvýšit krvácení z průniku. Některé léky nebo rostlinné produkty, které mohou snižovat účinnost hormonální antikoncepce, zahrnují fenytoin, barbituráty, karbamazepin, bosentan, felbamát, griseofulvin, oxkarbazepin, rifampin, topiramát a přípravky obsahující třezalku tečkovanou. Interakce mezi perorálními kontraceptivy a jinými léky mohou vést ke krvácení z průniku a/nebo selhání antikoncepce. Doporučte ženám používat alternativní metodu antikoncepce nebo záložní metodu, pokud se s COC užívají induktory enzymů, a aby pokračovaly v záložní antikoncepci po dobu 28 dnů po vysazení enzymatického induktoru, aby byla zajištěna spolehlivost antikoncepce.
Látky zvyšující plazmatické koncentrace COC
Současné podávání atorvastatinu a určitých COC obsahujících EE zvyšuje hodnoty AUC pro EE přibližně o 20 %. Kyselina askorbová a acetaminofen mohou zvýšit plazmatické koncentrace EE, pravděpodobně inhibicí konjugace.
Současné podávání středně silných nebo silných inhibitorů CYP3A4, jako jsou azolová antimykotika (např. ketokonazol, itrakonazol, vorikonazol, flukonazol), verapamil, makrolidy (např. klarithromycin, erythromycin), diltiazem a grapefruitová šťáva může zvýšit plazmatické koncentrace estrogenu nebo progestin nebo obojí. V klinické studii lékových interakcí prováděné u premenopauzálních žen vedlo současné podávání DRSP 3 mg/EE 0,02 mg obsahující tablety se silným inhibitorem CYP3A4 a ketokonazolem 200 mg dvakrát denně po dobu 10 dnů k mírnému zvýšení systémové expozice DRSP . Expozice EE byla mírně zvýšena [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ a KLINICKÁ FARMAKOLOGIE ].
Inhibitory proteázy viru lidské imunodeficience (HIV)/viru hepatitidy C (HCV) a nenukleosidové inhibitory reverzní transkriptázy
V některých případech současného podávání s inhibitory proteázy HIV/HCV nebo s nenukleosidovými inhibitory reverzní transkriptázy byly zaznamenány významné změny (zvýšení nebo snížení) plazmatických koncentrací estrogenu a progestinu.
Antibiotika
Byly hlášeny případy těhotenství při užívání hormonální antikoncepce a antibiotik, ale klinické farmakokinetické studie neprokázaly konzistentní účinky antibiotik na plazmatické koncentrace syntetických steroidů.
Účinky kombinovaných perorálních kontraceptiv na jiné léky
COC obsahující EE mohou inhibovat metabolismus jiných sloučenin. Bylo prokázáno, že COC významně snižují plazmatické koncentrace lamotriginu, pravděpodobně v důsledku indukce glukuronidace lamotriginu. To může snížit kontrolu záchvatů; proto může být nutná úprava dávkování lamotriginu. Chcete-li získat další informace o interakcích s COC nebo o potenciálu enzymových změn, podívejte se na označení souběžně užívaného léku.
COC Zvyšující plazmatické koncentrace enzymů CYP450
V klinických studiích nevedlo podávání hormonální antikoncepce obsahující EE k žádnému nebo pouze slabému zvýšení plazmatických koncentrací substrátů CYP3A4 (např. midazolamu), zatímco plazmatické koncentrace substrátů CYP2C19 (např. omeprazol a vorikonazol) a substrátů CYP1A2 (např. teofylin a tizanidin) může mít slabé nebo střední zvýšení.
Klinické studie neprokázaly inhibiční potenciál DRSP vůči lidským CYP enzymům v klinicky relevantních koncentracích (viz KLINICKÁ FARMAKOLOGIE ].
Ženy na substituční terapii hormony štítné žlázy mohou potřebovat zvýšené dávky hormonů štítné žlázy, protože sérová koncentrace globulinu vázajícího štítnou žlázu se zvyšuje s užíváním COC.
Potenciál ke zvýšení koncentrace draslíku v séru
Existuje potenciál pro zvýšení koncentrace draslíku v séru u žen užívajících Yasmin s jinými léky, které mohou zvýšit koncentraci draslíku v séru (viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ a KLINICKÁ FARMAKOLOGIE ].
Interference S Laboratorními Testy
Užívání antikoncepčních steroidů může ovlivnit výsledky některých laboratorních testů, jako jsou koagulační faktory, lipidy, glukózová tolerance a vazebné proteiny. DRSP způsobuje zvýšení aktivity plazmatického reninu a plazmatického aldosteronu indukované jeho mírnou antimineralokortikoidní aktivitou [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ a DROGOVÉ INTERAKCE ].
VAROVÁNÍ
Zahrnuto jako součást OPATŘENÍ sekce.
OPATŘENÍ
Tromboembolické poruchy a jiné cévní problémy
Pokud dojde k arteriální nebo žilní trombotické příhodě (VTE), zastavte přípravek Yasmin.
Na základě aktuálně dostupných informací o přípravku Yasmin 0,03 mg mohou být COC obsahující DRSP spojeny s vyšším rizikem žilního tromboembolismu (VTE) než COC obsahující progestin levonorgestrel nebo některé jiné progestiny. Epidemiologické studie, které porovnávaly riziko VTE, uváděly, že riziko se pohybovalo od žádného zvýšení až po trojnásobné zvýšení. Před zahájením užívání Yasmin u nové uživatelky COC nebo u ženy, která přechází z antikoncepce, která neobsahuje DRSP, zvažte rizika a přínosy COC obsahujícího DRSP s ohledem na riziko VTE. Známé rizikové faktory pro VTE zahrnují kouření, obezitu a rodinnou anamnézu VTE, kromě dalších faktorů, které kontraindikují užívání COC (viz KONTRAINDIKACE ].
Řada studií porovnávala riziko VTE u uživatelek Yasmin s rizikem pro uživatelky jiných COC, včetně COC obsahujících levonorgestrel. Ty, které byly vyžadovány nebo sponzorovány regulačními agenturami, jsou shrnuty v tabulce 1.
Kromě těchto „regulačních studií“ byly provedeny další studie různého designu. Celkově existují dvě prospektivní kohortové studie (viz tabulka 1): americká poregistrační bezpečnostní studie Ingenix [Seeger 2007], evropská poregistrační bezpečnostní studie EURAS (European Active Surveillance Study) [Dinger 2007]. Rozšíření studie EURAS, Long-Term Active Surveillance Study (LASS), nezařadilo další subjekty, ale pokračovalo v hodnocení rizika VTE. Existují tři retrospektivní kohortové studie: jedna studie v USA financovaná FDA (viz tabulka 1) a dvě z Dánska [Lidegaard 2009, Lidegaard 2011]. Existují dvě případové kontrolní studie: holandská analýza studie MEGA [van Hylckama Vlieg 2009] a německá případová kontrolní studie [Dinger 2010]. Existují dvě vnořené studie případ-kontrola, které hodnotily riziko nefatální idiopatické VTE: studie PharMetrics [Jick 2011] a studie GPRD [Parkin 2011]. Výsledky všech těchto studií jsou uvedeny na obrázku 1.
Obrázek 1: Riziko VTE u přípravku Yasmin 0,03 mg ve srovnání s COC obsahujícími LNG (upravené riziko#) 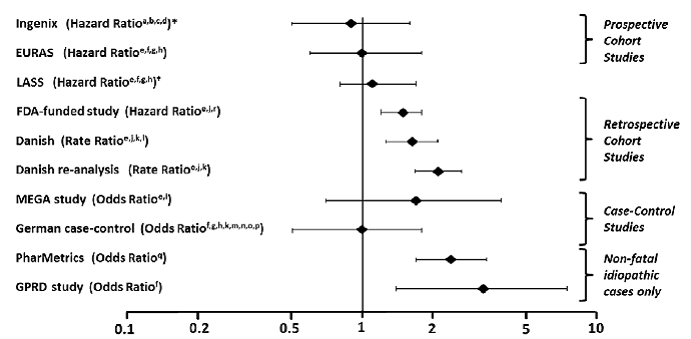
Poměry rizika zobrazené na logaritmické stupnici; poměr rizika 1 znamená zvýšené riziko VTE pro DRSP.
*Srovnávací „Ostatní COC“, včetně COC obsahujících LNG † LASS je rozšířením studie EURAS
#Některé přizpůsobovací faktory jsou označeny horním indexem: a) současné silné kouření, b) hypertenze, c) obezita, d) rodinná anamnéza, e) věk, f) BMI, g) délka užívání, h) anamnéza VTE, i) doba zařazení, j) kalendářní rok, k) vzdělání, l) délka užívání, m) parita, n) chronické onemocnění, o) souběžná medikace, p) kouření, q) délka expozice, r) místo
(Odkazy: Ingenix [Seeger 2007]1, EURAS (European Active Surveillance Study) [Dinger 2007]2, LASS (Long-Term Active Surveillance Study) [Dinger, nepublikovaný dokument v souboru], studie financovaná FDA [Sidney 2011]3 , dánský [Lidegaard 2009]4, dánský reanalýza [Lidegaard 2011]5, studie MEGA [van Hylckama Vlieg 2009]6, německá studie Case-Control [Dinger 2010]7, PharMetrics [Jick 2011]8, studie GPRD [Parkin 200 9)
Přestože je absolutní míra VTE u uživatelek hormonální antikoncepce ve srovnání s neuživatelkami vyšší, míra v těhotenství je ještě vyšší, zejména v poporodním období (viz obrázek 2). Riziko VTE u žen užívajících COC se odhaduje na 3 až 9 na 10 000 žen-roků. Riziko VTE je nejvyšší během prvního roku užívání. Údaje z velké, prospektivní kohortové studie bezpečnosti různých COC naznačují, že toto zvýšené riziko ve srovnání s rizikem u žen, které COC neužívají, je největší během prvních 6 měsíců užívání COC. Údaje z této bezpečnostní studie naznačují, že největší riziko VTE je přítomno po počátečním zahájení užívání COC nebo opětovném zahájení (po 4týdenním nebo delším intervalu bez užívání tablet) se stejnou nebo jinou COC.
Riziko tromboembolické nemoci způsobené perorálními kontraceptivy postupně mizí po vysazení COC.
Obrázek 2 ukazuje riziko rozvoje VTE u žen, které nejsou těhotné a neužívají perorální antikoncepci, u žen užívajících perorální antikoncepci, u těhotných žen a u žen v poporodním období. Pro srovnání rizika rozvoje VTE: Pokud je po dobu jednoho roku sledováno 10 000 žen, které nejsou těhotné a neužívají perorální antikoncepci, u 1 až 5 z těchto žen se VTE vyvine.
Obrázek 2: Pravděpodobnost rozvoje VTE 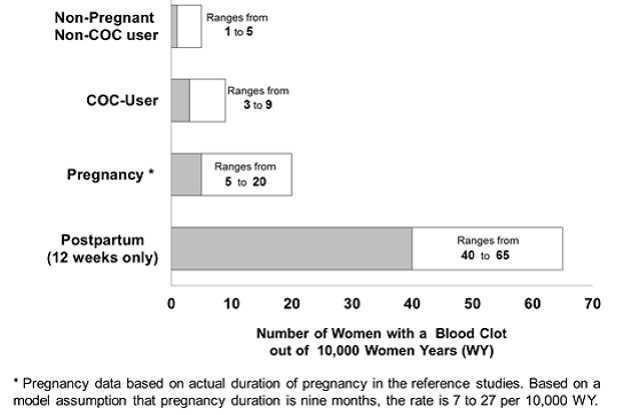
Pokud je to možné, přerušte užívání přípravku Yasmin alespoň 4 týdny před a 2 týdny po velkém chirurgickém zákroku nebo jiných operacích, o kterých je známo, že mají zvýšené riziko tromboembolie.
U žen, které nekojí, začněte Yasmin nejdříve 4 týdny po porodu. Riziko poporodní tromboembolie klesá po třetím týdnu po porodu, zatímco riziko ovulace se zvyšuje po třetím týdnu po porodu.
Užívání COC také zvyšuje riziko arteriálních trombóz, jako jsou mrtvice a infarkty myokardu, zejména u žen s jinými rizikovými faktory pro tyto příhody.
Bylo prokázáno, že COC zvyšují jak relativní, tak i přisouditelná rizika cerebrovaskulárních příhod (trombotické a hemoragické mrtvice), ačkoli obecně je riziko největší u starších (> 35 let věku), hypertoniků, které také kouří. COC také zvyšují riziko cévní mozkové příhody u žen s dalšími základními rizikovými faktory.
Perorální antikoncepce musí být používána s opatrností u žen s rizikovými faktory kardiovaskulárního onemocnění.
Zastavte přípravek Yasmin 0,03 mg, pokud dojde k nevysvětlitelné ztrátě zraku, proptóze, diplopii, edému papily nebo vaskulárním lézím sítnice. Okamžitě vyhodnoťte trombózu retinální žíly. [Vidět NEŽÁDOUCÍ REAKCE ]
Hyperkalémie
Yasmin obsahuje 3 mg progestinu DRSP, který má antimineralokortikoidní aktivitu, včetně potenciálu pro hyperkalemii u vysoce rizikových pacientů, srovnatelnou s dávkou 25 mg spironolaktonu. Yasmin je kontraindikován u pacientů se stavy, které predisponují k hyperkalémii (tj. poškození ledvin, jater a adrenální insuficience). U žen, které se denně dlouhodobě léčí na chronické stavy nebo onemocnění léky, které mohou zvýšit koncentraci draslíku v séru, by měla být koncentrace draslíku v séru kontrolována během prvního léčebného cyklu. Mezi léky, které mohou zvýšit koncentraci draslíku v séru, patří ACE inhibitory, antagonisté receptoru angiotenzinu II, draslík šetřící diuretika, suplementace draslíku, heparin, antagonisté aldosteronu a NSAID. Zvažte sledování koncentrace draslíku v séru u vysoce rizikových pacientů, kteří dlouhodobě a současně užívají silný inhibitor CYP3A4. Mezi silné inhibitory CYP3A4 patří azolová antimykotika (např. ketokonazol, itrakonazol, vorikonazol), inhibitory HIV/HCV proteázy (např. indinavir, boceprevir) a klarithromycin [viz KLINICKÁ FARMAKOLOGIE ].
Karcinom Prsů A Rozmnožovacích Orgánů
Ženy, které v současnosti mají nebo měly rakovinu prsu, by neměly užívat přípravek Yasmin, protože rakovina prsu je hormonálně citlivý nádor.
Existují podstatné důkazy, že COC nezvyšují výskyt rakoviny prsu. Ačkoli některé minulé studie naznačovaly, že COC mohou zvýšit výskyt rakoviny prsu, novější studie taková zjištění nepotvrdily.
Některé studie naznačují, že COC jsou spojeny se zvýšením rizika rakoviny děložního čípku nebo intraepiteliální neoplazie. Existuje však spor o tom, do jaké míry mohou být tato zjištění způsobena rozdíly v sexuálním chování a dalšími faktory.
Nemoc jater
Pokud se rozvine žloutenka, Yasmin přerušte. U pacientů s poruchou funkce jater mohou být steroidní hormony špatně metabolizovány. Akutní nebo chronické poruchy jaterních funkcí mohou vyžadovat přerušení užívání COC, dokud se markery jaterních funkcí nevrátí k normálu a dokud nebude vyloučena příčinná souvislost s COC.
Jaterní adenomy jsou spojeny s užíváním COC. Odhad přiřaditelného rizika je 3,3 případů/100 000 uživatelek COC. Ruptura jaterních adenomů může způsobit smrt intraabdominálním krvácením.
Studie prokázaly zvýšené riziko rozvoje hepatocelulárního karcinomu u dlouhodobých (> 8 let) uživatelek COC. Riziko rakoviny jater u uživatelek COC je však méně než jeden případ na milion uživatelů.
U žen s anamnézou cholestázy související s těhotenstvím se může objevit cholestáza související s perorální antikoncepcí. U žen s anamnézou cholestázy související s COC se může tento stav opakovat při následném užívání COC.
Vysoký krevní tlak
žen s dobře kontrolovanou hypertenzí sledujte krevní tlak a vysaďte přípravek Yasmin 0,03 mg, pokud krevní tlak výrazně stoupne. Ženy s nekontrolovanou hypertenzí nebo hypertenzí s vaskulárním onemocněním by COC neměly užívat.
U žen užívajících COC bylo hlášeno zvýšení krevního tlaku a toto zvýšení je pravděpodobnější u starších žen a při prodloužené době užívání. Výskyt hypertenze se zvyšuje se zvyšující se koncentrací progestinu.
Onemocnění žlučníku
Studie naznačují malé zvýšení relativního rizika rozvoje onemocnění žlučníku mezi uživatelkami COC.
Metabolické účinky sacharidů a lipidů
Pečlivě sledujte prediabetické a diabetické ženy, které užívají Yasmin. COC mohou snižovat glukózovou toleranci v závislosti na dávce.
Zvažte alternativní antikoncepci pro ženy s nekontrolovanou dyslipidémií. Malá část žen bude mít během užívání COC nepříznivé změny lipidů.
Ženy s hypertriglyceridémií nebo s ní v rodinné anamnéze mohou mít při užívání COC zvýšené riziko pankreatitidy.
Bolest hlavy
Pokud se u ženy užívající přípravek Yasmin 0,03 mg objeví nové bolesti hlavy, které jsou opakující se, přetrvávající nebo závažné, zhodnoťte příčinu a v případě potřeby přerušte podávání přípravku Yasmin 3 mg.
Zvýšená frekvence nebo závažnost migrény během užívání COC (která může být prodromem cerebrovaskulární příhody) může být důvodem k okamžitému vysazení COC.
Nepravidelnosti krvácení
U pacientek užívajících COC se někdy objevuje neplánované (průlomové nebo intracyklické) krvácení a špinění, zejména během prvních tří měsíců užívání. Pokud krvácení přetrvává nebo se objeví po předchozích pravidelných cyklech, zkontrolujte příčiny, jako je těhotenství nebo malignita. Pokud jsou vyloučeny patologie a těhotenství, nepravidelnosti krvácení se mohou časem upravit nebo se změnou COC.
Údaje z deseti klinických studií účinnosti antikoncepce (N=2 467) ukazují, že procento žen, které užívaly Yasmin a zažily neplánované krvácení, se v průběhu času snížilo z 12 % v cyklu 2 na 6 % (cyklus 13). Celkem 24 subjektů z 2 837 ve studiích Yasmin (
Průměrné trvání plánovaných krvácivých epizod u většiny subjektů (86 %-88 %) bylo 4-7 dní. U žen, které užívají Yasmin 3 mg, může dojít k absenci krvácení z vysazení, i když nejsou těhotné. Na základě deníků osob ze studií antikoncepční účinnosti nezaznamenalo během cyklů 2–13 1–11 % žen na cyklus žádné krvácení z vysazení. Některé ženy se mohou setkat s amenoreou po užití pilulky nebo oligomenoreou, zejména pokud již takový stav existoval.
Pokud nedojde ke krvácení z vysazení, zvažte možnost těhotenství. Pokud pacientka nedodržela předepsané dávkovací schéma (vynechala jednu nebo více aktivních tablet nebo je začala užívat o den později, než měla), zvažte možnost těhotenství v době první vynechané menstruace a proveďte vhodná diagnostická opatření. . Pokud pacientka dodržela předepsaný režim a vynechá dvě po sobě jdoucí menstruace, vylučte těhotenství.
Užívání COC před nebo během časného těhotenství
Rozsáhlé epidemiologické studie neodhalily žádné zvýšené riziko vrozených vad u žen, které před těhotenstvím užívaly perorální antikoncepci. Studie také nenaznačují teratogenní účinek, pokud jsou COC neúmyslně užívány během časného těhotenství, zejména pokud jde o srdeční anomálie a defekty zmenšení končetin.
Podávání perorální antikoncepce k vyvolání krvácení z vysazení by se nemělo používat jako test na těhotenství (viz Použití ve specifických populacích ].
Deprese
Ženy s depresí v anamnéze by měly být pečlivě sledovány a léčba Yasminem by měla být přerušena, pokud se deprese ve vážném rozsahu vrátí.
Interference S Laboratorními Testy
Užívání COC může změnit výsledky některých laboratorních testů, jako jsou koagulační faktory, lipidy, glukózová tolerance a vazebné proteiny. Ženy na substituční terapii hormony štítné žlázy mohou potřebovat zvýšené dávky hormonů štítné žlázy, protože sérové koncentrace globulinu vázajícího štítnou žlázu se zvyšují s užíváním COC (viz DROGOVÉ INTERAKCE ].
DRSP způsobuje zvýšení aktivity plazmatického reninu a plazmatického aldosteronu indukované jeho mírnou antimineralokortikoidní aktivitou.
Sledování
Žena, která užívá COC, by měla každoročně navštěvovat svého poskytovatele zdravotní péče kvůli kontrole krevního tlaku a další indikované zdravotní péči.
Jiné podmínky
žen s hereditárním angioedémem mohou exogenní estrogeny vyvolat nebo zhoršit příznaky angioedému. Občas se může objevit chloasma, zvláště u žen s chloasma gravidarum v anamnéze. Ženy se sklonem ke chloasmatu by se měly během užívání COC vyhýbat expozici slunci nebo ultrafialovému záření.
Informace pro pacienty
Viz „Označení pacienta schválené FDA ( INFORMACE PRO PACIENTA ).“
- Informujte pacienty, že kouření cigaret zvyšuje riziko závažných kardiovaskulárních příhod při užívání COC a že ženy starší 35 let, které kouří, by COC neměly užívat.
- Informujte pacientky, že zvýšené riziko VTE ve srovnání s ženami, které COC neužívají, je největší po počátečním zahájení užívání COC nebo opětovném zahájení (po 4týdenním nebo delším intervalu bez užívání pilulek) stejného nebo jiného COC.
- Informujte pacientky o informacích týkajících se rizika VTE u COC obsahujících DRSP ve srovnání s COC, která obsahují levonorgestrel nebo některé jiné progestiny.
- Informujte pacienty, že přípravek Yasmin nechrání před infekcí HIV (AIDS) a jinými pohlavně přenosnými chorobami.
- Poraďte pacientům VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ spojené s COC.
- Informujte pacienty, že přípravek Yasmin 3 mg obsahuje DRSP. Drospirenon může zvýšit draslík. Pacienti by měli být poučeni, aby informovali svého poskytovatele zdravotní péče, pokud mají onemocnění ledvin, jater nebo nadledvin, protože užívání přípravku Yasmin v přítomnosti těchto stavů může způsobit vážné srdeční a zdravotní problémy. Měli by také informovat svého poskytovatele zdravotní péče, pokud jsou v současné době na každodenní, dlouhodobé léčbě (NSAID, draslík šetřící diuretika, suplementace draslíkem, ACE inhibitory, antagonisté receptoru angiotensinu-II, heparin nebo antagonisté aldosteronu) kvůli chronickému stavu nebo užívají silné inhibitory CYP3A4.
- Informujte pacientky, že přípravek Yasmin 0,03 mg není indikován během těhotenství. Pokud během léčby přípravkem Yasmin 3 mg dojde k otěhotnění, poučte pacientku, aby přerušila další užívání.
- Doporučte pacientům, aby užívali jednu tabletu denně ústy každý den ve stejnou dobu. Poučte pacienty, co mají dělat v případě vynechání pilulek. Vidět „Co dělat, když vám chybějí prášky“ sekce v Označení pacientů schválené FDA.
- Doporučte pacientkám, aby používali záložní nebo alternativní metodu antikoncepce, pokud se s COC používají induktory enzymů.
- Informujte pacientky, které kojí nebo chtějí kojit, že COC mohou snižovat tvorbu mateřského mléka. To je méně pravděpodobné, pokud je kojení dobře zavedeno.
- Poraďte pacientce, která po porodu začne užívat COC a která ještě nedostala menstruaci, aby používala další metodu antikoncepce, dokud nebude užívat žlutou tabletu po dobu 7 po sobě jdoucích dnů.
- Informujte pacienty, že se může objevit amenorea. Vylučte těhotenství v případě amenorey ve dvou nebo více po sobě jdoucích cyklech.
Neklinická toxikologie
Karcinogeneze, mutageneze, zhoršení plodnosti
Ve 24měsíční studii karcinogenity při perorálním podávání u myší, kterým byl podáván pouze DRSP v dávce 10 mg/kg/den nebo 1 + 0,01, 3 + 0,03 a 10 + 0,1 mg/kg/den DRSP a EE, 0,1 až 2násobek expozice (AUC DRSP) žen užívajících antikoncepční dávku, došlo ke zvýšení karcinomů harderian žlázy ve skupině, která dostávala vysokou dávku samotného DRSP. V podobné studii na potkanech, kterým bylo podáváno 10 mg/kg/den DRSP samostatně nebo 0,3 + 0,003, 3 + 0,03 a 10 + 0,1 mg/kg/den DRSP a EE, 0,8 až 10násobek expozice žen užívajících antikoncepční dávku. byl zvýšený výskyt benigních a celkových (benigních a maligních) feochromocytomů nadledvin ve skupině dostávající vysokou dávku DRSP. Studie mutageneze pro DRSP byly provedeny in vivo a in vitro a nebyly pozorovány žádné známky mutagenní aktivity.
Použití u konkrétních populací
Těhotenství
žen, které neúmyslně užívají COC během časného těhotenství, existuje malé nebo žádné zvýšené riziko vrozených vad. Epidemiologické studie a metaanalýzy nezjistily zvýšené riziko genitálních nebo negenitálních vrozených vad (včetně srdečních anomálií a defektů zmenšení končetin) po expozici nízkým dávkám COC před početím nebo během časného těhotenství.
Podávání COC k vyvolání krvácení z vysazení by se nemělo používat jako test na těhotenství. COC by se neměla používat během těhotenství k léčbě hrozícího nebo obvyklého potratu.
Ženy, které nekojí, mohou začít s COC nejdříve čtyři týdny po porodu.
Kojící matky
Pokud je to možné, doporučte kojící matce, aby používala jiné formy antikoncepce, dokud své dítě neodstaví. COC obsahující estrogeny mohou snížit tvorbu mléka u kojících matek. Toto je méně pravděpodobné, že nastane, jakmile je kojení dobře zavedeno; u některých žen se však může objevit kdykoli. Malá množství steroidů a/nebo metabolitů perorální antikoncepce jsou přítomna v mateřském mléce.
Po perorálním podání přípravku Yasmin 0,03 mg bylo asi 0,02 % dávky DRSP vyloučeno do mateřského mléka žen po porodu během 24 hodin. To vede k maximální denní dávce přibližně 0,003 mg DRSP u kojence.
Pediatrické použití
Bezpečnost a účinnost přípravku Yasmin byla stanovena u žen v reprodukčním věku. Očekává se, že účinnost bude stejná u postpubertálních dospívajících do 18 let au uživatelů ve věku 18 let a starších. Použití tohoto produktu před menarche není indikováno.
Geriatrické použití
Yasmin nebyl studován u žen po menopauze a není u této populace indikován.
Pacienti s poruchou ledvin
Yasmin 0,03 mg je kontraindikován u pacientů s poruchou funkce ledvin (viz KONTRAINDIKACE a VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ].
U subjektů s clearance kreatininu (CLcr) 50–79 ml/min byly sérové koncentrace DRSP srovnatelné s koncentracemi v kontrolní skupině s CLcr ≥ 80 ml/min. U subjektů s CLcr 30–49 ml/min byly sérové koncentrace DRSP v průměru o 37 % vyšší než v kontrolní skupině. Kromě toho existuje potenciál pro rozvoj hyperkalémie u subjektů s poruchou funkce ledvin, jejichž hladina draslíku v séru je v horním referenčním rozmezí a kteří současně užívají léky šetřící draslík (viz KLINICKÁ FARMAKOLOGIE ].
Pacienti s poruchou funkce jater
Yasmin je kontraindikován u pacientů s onemocněním jater [viz KONTRAINDIKACE a VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]. Průměrná expozice DRSP u žen se středně těžkou poruchou funkce jater je přibližně třikrát vyšší než expozice u žen s normální funkcí jater. Přípravek Yasmin nebyl studován u žen s těžkou poruchou funkce jater.
Závod
Nebyl pozorován žádný klinicky významný rozdíl mezi farmakokinetikou DRSP nebo EE u japonských žen oproti běloškám [viz KLINICKÁ FARMAKOLOGIE ].
REFERENCE
1. Seeger, JD, Loughlin, J., Eng, PM, Clifford, ČR, Cutone, J., and Walker, AM (2007). Riziko tromboembolie u žen užívajících ethinylestradiol/drospirenon a jinou perorální antikoncepci. Obstet Gynecol 110, 587-593.
2. Dinger, JC, Heinemann, LA a Kuhl-Habich, D. (2007). Bezpečnost perorální antikoncepce obsahující drospirenon: konečné výsledky evropské studie aktivního sledování perorálních kontraceptiv na základě 142 475 žen-roků pozorování. Antikoncepce 75, 344-354.
3. Kombinovaná hormonální antikoncepce (CHC) a riziko kardiovaskulárních endpointů. Sidney, S. (primární autor) http://www.fda.gov/downloads/Drugs/DrugSafety/UCM277384.pdf, přístup 27. října 2011.
4. Lidegaard, O., Lokkegaard, E., Svendsen, AL a Agger, C. (2009). Hormonální antikoncepce a riziko žilního tromboembolismu: národní následná studie. BMJ 339, b2890.
5. Lidegaard, O., Nielsen, LH, Skovlund, CW, Skjeldestad, FE a Lokkegaard, E. (2011). Riziko žilního tromboembolismu při užívání perorálních kontraceptiv obsahujících různé progestogeny a dávky estrogenu: Dánská kohortová studie, 2001-9. BMJ 343, d6423.
6. van Hylckama Vlieg, A., Helmerhorst, FM, Vandenbroucke, JP, Doggen, CJ a Rosendaal, FR (2009). Venózní trombotické riziko perorální antikoncepce, účinky dávky estrogenu a typ progestogenu: výsledky případové a kontrolní studie MEGA. BMJ 339, b2921.
7. Dinger, J., Assmann, A., Mohner, S. a Minh, TD (2010). Riziko žilního tromboembolismu a užívání perorálních kontraceptiv obsahujících dienogest a drospirenon: výsledky německé případové kontrolní studie. J Fam Plann Reprod Health Care 36, 123-129.
8. Jick, SS a Hernandez, RK (2011). Riziko nefatálního žilního tromboembolismu u žen užívajících perorální antikoncepci obsahující drospirenon ve srovnání s ženami užívajícími perorální kontraceptiva obsahující levonorgestrel: případová kontrolní studie využívající údaje z tvrzení Spojených států. BMJ 342, d2151.
9. Parkin, L., Sharples, K., Hernandez, RK a Jick, SS (2011). Riziko žilního tromboembolismu u uživatelek perorální antikoncepce obsahující drospirenon nebo levonorgestrel: vnořená případová-kontrolní studie založená na UK General Practice Research Database. BMJ 342, d2139.
PŘEDÁVKOVAT
Nebyly hlášeny žádné závažné nežádoucí účinky předávkování, včetně požití dětmi. Předávkování může u žen způsobit krvácení z vysazení a nevolnost.
DRSP je analog spironolaktonu, který má antimineralokortikoidní vlastnosti. V případech předávkování je třeba sledovat sérové koncentrace draslíku a sodíku a známky metabolické acidózy.
KONTRAINDIKACE
Nepředepisujte Yasmin 3 mg ženám, o kterých je známo, že mají následující:
- Renální poškození
- Nedostatek adrenalinu
- Vysoké riziko arteriálních nebo žilních trombotických onemocnění. Příklady zahrnují ženy, o kterých je známo, že:
- Kouř, pokud je starší 35 let [viz VAROVÁNÍ V KRABICE a VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Máte hlubokou žilní trombózu nebo plicní embolii, nyní nebo v minulosti [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Máte cerebrovaskulární onemocnění [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Máte onemocnění koronárních tepen [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Máte trombogenní chlopenní nebo trombogenní srdeční onemocnění srdečního rytmu (například subakutní bakteriální endokarditida s chlopenním onemocněním nebo fibrilace síní) [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Máte zděděné nebo získané hyperkoagulopatie [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Mít nekontrolovanou hypertenzi [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Máte diabetes mellitus s cévním onemocněním [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Máte bolesti hlavy s fokálními neurologickými příznaky nebo máte migrénové bolesti hlavy s aurou nebo bez aury, pokud jsou starší 35 let [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Nediagnostikované abnormální děložní krvácení [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Rakovina prsu nebo jiná rakovina citlivá na estrogen nebo progestin, nyní nebo v minulosti [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Nádor jater (benigní nebo maligní) nebo onemocnění jater [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ a Použití u konkrétních populací ]
- Těhotenství, protože není důvod užívat COC během těhotenství [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ a Použití ve specifických populacích ]
KLINICKÁ FARMAKOLOGIE
Mechanismus působení
COC snižují riziko otěhotnění především potlačením ovulace. Další možné mechanismy mohou zahrnovat změny cervikálního hlenu, které inhibují penetraci spermií a změny endometria, které snižují pravděpodobnost implantace.
Farmakodynamika
Drospirenon je analog spironolaktonu s antimineralokortikoidní aktivitou. Estrogen v Yasminu je ethinylestradiol (EE).
S Yasminem nebyly provedeny žádné specifické farmakodynamické studie.
Farmakokinetika
Vstřebávání
Absolutní biologická dostupnost DRSP z jedné tablety je asi 76 %. Absolutní biologická dostupnost EE je přibližně 40 % v důsledku presystémové konjugace a metabolismu prvního průchodu játry. Absolutní biologická dostupnost přípravku Yasmin 3 mg, což je kombinovaná tableta DRSP a EE, nebyla hodnocena. Sérové koncentrace DRSP a EE dosáhly maximálních hladin během 1-2 hodin po podání Yasminu.
Farmakokinetika DRSP je úměrná dávce po jednotlivých dávkách v rozmezí 1-10 mg. Po denním podávání Yasminu byly po 8 dnech pozorovány koncentrace DRSP v ustáleném stavu. Po podání více dávek Yasminu došlo k přibližně 2 až 3násobné akumulaci hodnot Cmax a AUC (0-24h) DRSP v séru (viz tabulka 2).
U EE jsou stavy ustáleného stavu hlášeny během druhé poloviny léčebného cyklu. Po každodenním podávání Yasmin sérové Cmax a AUC (0-24h) se hodnoty EE akumulují faktorem přibližně 1,5 až 2 (viz tabulka 2).
Food Effect
Rychlost absorpce DRSP a EE po jednorázovém podání formulace podobné Yasminu byla pomalejší za podmínek nasycení (s vysokým obsahem tuku), přičemž sérová Cmax byla snížena o 40 % pro obě složky. Rozsah absorpce DRSP však zůstal nezměněn. Na rozdíl od toho byl rozsah absorpce EE snížen asi o 20 % za podmínek nasycení.

Rozdělení
Koncentrace DRSP a EE v séru klesají ve dvou fázích. Zdánlivý distribuční objem DRSP je přibližně 4 l/kg a distribuční objem EE se uvádí přibližně 4–5 l/kg.
DRSP se neváže na globulin vázající pohlavní hormony (SHBG) nebo globulin vázající kortikosteroidy (CBG), ale váže se asi z 97 % na jiné sérové proteiny. Vícenásobné dávkování během 3 cyklů nevedlo k žádné změně volné frakce (jak bylo měřeno při minimálních koncentracích). Uvádí se, že EE se vysoce, ale nespecificky váže na sérový albumin (přibližně 98,5 %) a vyvolává zvýšení sérových koncentrací SHBG i CBG. Účinky vyvolané EE na SHBG a CBG nebyly ovlivněny změnou dávky DRSP v rozmezí 2 až 3 mg.
Metabolismus
Dva hlavní metabolity DRSP nalezené v lidské plazmě byly identifikovány jako kyselá forma DRSP vytvořená otevřením laktonového kruhu a 4,5-dihydrodrospirenon-3-sulfát vzniklý redukcí a následnou sulfatací.
Ukázalo se, že tyto metabolity nejsou farmakologicky aktivní. Drospirenon také podléhá oxidativnímu metabolismu katalyzovanému CYP3A4.
Bylo hlášeno, že EE podléhá významnému metabolismu prvního průchodu střevem a játry. Metabolismus EE a jeho oxidačních metabolitů probíhá primárně konjugací s glukuronidem nebo sulfátem. CYP3A4 v játrech je zodpovědný za 2-hydroxylaci, která je hlavní oxidační reakcí. 2-hydroxymetabolit je dále transformován methylací a glukuronidací před vylučováním močí a stolicí.
Vylučování
Koncentrace DRSP v séru jsou charakterizovány poločasem terminální dispoziční fáze přibližně 30 hodin po režimu s jednou i více dávkami. Vylučování DRSP bylo téměř úplné po deseti dnech a vyloučená množství byla mírně vyšší ve stolici ve srovnání s močí. DRSP byl extenzivně metabolizován a pouze stopová množství nezměněného DRSP byla vylučována močí a stolicí. V moči a stolici bylo pozorováno nejméně 20 různých metabolitů. Asi 38-47 % metabolitů v moči byly glukuronidové a sulfátové konjugáty. Ve stolici bylo asi 17–20 % metabolitů vyloučeno jako glukuronidy a sulfáty.
U EE byl poločas terminální dispoziční fáze hlášen přibližně 24 hodin. EE se nevylučuje beze změny. EE se vylučuje močí a stolicí jako glukuronidové a sulfátové konjugáty a prochází enterohepatální cirkulací.
Použití ve specifických populacích
Pediatrické použití: Bezpečnost a účinnost přípravku Yasmin 0,03 mg byla stanovena u žen v reprodukčním věku. Očekává se, že účinnost bude stejná u postpubertálních dospívajících do 18 let au uživatelů ve věku 18 let a starších. Použití tohoto produktu před menarche není indikováno.
Geriatrické použití: Yasmin nebyl studován u žen po menopauze a není u této populace indikován.
Závod: Nebyl pozorován žádný klinicky významný rozdíl mezi farmakokinetikou DRSP nebo EE u japonských žen oproti běloškám (ve věku 25-35 let), když byly 3 mg DRSP/0,02 mg EE podávány denně po dobu 21 dnů. Jiné etnické skupiny nebyly konkrétně studovány.
Renální poškození: Yasmin je kontraindikován u pacientů s poruchou funkce ledvin.
Vliv poškození ledvin na farmakokinetiku DRSP (3 mg denně po dobu 14 dnů) a účinek DRSP na koncentrace draslíku v séru byly zkoumány u tří samostatných skupin žen (n=28, věk 30-65). Všechny subjekty byly na dietě s nízkým obsahem draslíku. Během studie 7 subjektů pokračovalo v užívání draslík šetřících léků k léčbě jejich základního onemocnění. 14. den (ustálený stav) léčby DRSP byly sérové koncentrace DRSP ve skupině s CLcr 50–79 ml/min srovnatelné s koncentracemi v kontrolní skupině s CLcr ≥ 80 ml/min. Sérové koncentrace DRSP byly v průměru o 37 % vyšší ve skupině s CLcr 30–49 ml/min ve srovnání s kontrolní skupinou. Léčba DRSP neprokázala žádný klinicky významný účinek na koncentraci draslíku v séru. Ačkoli hyperkalémie nebyla ve studii pozorována, u pěti ze sedmi subjektů, kteří během studie pokračovali v užívání léků šetřících draslík, se průměrné sérové koncentrace draslíku zvýšily až o 0,33 mEq/l. [Vidět KONTRAINDIKACE a VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
Poškození jater: Yasmin 0,03 mg je kontraindikován u pacientů s onemocněním jater.
Průměrná expozice DRSP u žen se středně těžkou poruchou funkce jater je přibližně třikrát vyšší než expozice u žen s normální funkcí jater. Přípravek Yasmin nebyl studován u žen s těžkou poruchou funkce jater. [Vidět KONTRAINDIKACE a VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
Lékové interakce
Chcete-li získat další informace o interakcích s perorálními kontraceptivy nebo o potenciálu enzymových změn, prohlédněte si označení všech současně užívaných léků.
Účinky jiných léků na kombinovanou perorální antikoncepci
Látky snižující účinnost COC: Léky nebo rostlinné produkty, které indukují určité enzymy, včetně CYP3A4, mohou snížit účinnost COC nebo zvýšit krvácení z průniku.
Látky zvyšující plazmatické koncentrace COC: Současné podávání atorvastatinu a určitých COC obsahujících EE zvyšuje hodnoty AUC pro EE přibližně o 20 %. Kyselina askorbová a acetaminofen mohou zvýšit plazmatické koncentrace EE, pravděpodobně inhibicí konjugace. V klinické studii lékových interakcí provedené u 20 premenopauzálních žen zvýšilo současné podávání DRSP (3 mg)/EE (0,02 mg) COC se silným inhibitorem CYP3A4 ketokonazolem (200 mg dvakrát denně) po dobu 10 dnů AUC( 0-24h) DRSP a EE 2,68krát (90% CI: 2,44, 2,95) a 1,40krát (90% CI: 1,31, 1,49), v daném pořadí. Zvýšení Cmax bylo 1,97násobné (90% CI: 1,79, 2,17) a 1,39násobné (90% CI: 1,28, 1,52) pro DRSP a EE, v daném pořadí. Ačkoli nebyly pozorovány žádné klinicky relevantní účinky na bezpečnost nebo laboratorní parametry včetně sérového draslíku, tato studie posuzovala subjekty pouze po dobu 10 dnů. Klinický dopad na pacienta užívajícího COC obsahující DRSP současně s chronickým užíváním inhibitoru CYP3A4/5 není znám (viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ].
Inhibitory HIV/HCV proteázy a nenukleosidové inhibitory reverzní transkriptázy: V některých případech současného podávání s inhibitory proteázy HIV/HCV nebo s nenukleosidovými inhibitory reverzní transkriptázy byly zaznamenány významné změny (zvýšení nebo snížení) plazmatických koncentrací estrogenu a progestinu.
antibiotika: Byly hlášeny případy těhotenství při užívání hormonální antikoncepce a antibiotik, ale klinické farmakokinetické studie neprokázaly konzistentní účinky antibiotik na plazmatické koncentrace syntetických steroidů.
Účinky kombinované perorální antikoncepce na jiné léky
COC obsahující EE mohou inhibovat metabolismus jiných sloučenin. Bylo prokázáno, že COC významně snižují plazmatické koncentrace lamotriginu, pravděpodobně v důsledku indukce glukuronidace lamotriginu. To může snížit kontrolu záchvatů; proto může být nutná úprava dávkování lamotriginu. Chcete-li získat další informace o interakcích s COC nebo o potenciálu enzymových změn, podívejte se na označení souběžně užívaného léku.
In vitro je EE reverzibilním inhibitorem CYP2C19, CYP1A1 a CYP1A2 a také inhibitorem CYP3A4/5, CYP2C8 a CYP2J2 založeným na mechanismu. Metabolismus DRSP a potenciální účinky DRSP na jaterní enzymy CYP byly zkoumány ve studiích in vitro a in vivo. Ve studiích in vitro DRSP neovlivnil obrat modelových substrátů CYP1A2 a CYP2D6, ale měl inhibiční vliv na obrat modelových substrátů CYP1A1, CYP2C9, CYP2C19 a CYP3A4, přičemž nejcitlivějším enzymem byl CYP2C19. Potenciální účinek DRSP na aktivitu CYP2C19 byl zkoumán v klinické farmakokinetické studii s použitím omeprazolu jako markerového substrátu. Ve studii s 24 ženami po menopauze [včetně 12 žen s homozygotním (divoký typ) genotypu CYP2C19 a 12 žen s heterozygotním genotypem CYP2C19] denní perorální podávání 3 mg DRSP po dobu 14 dnů neovlivnilo perorální clearance omeprazolu (40 mg, jedna perorální dávka) a produkt CYP2C19 5-hydroxy omeprazol. Kromě toho nebyl zjištěn žádný významný účinek DRSP na systémovou clearance produktu CYP3A4 omeprazolsulfon. Tyto výsledky ukazují, že DRSP neinhibuje CYP2C19 a CYP3A4 in vivo.
Dvě další klinické studie lékových interakcí s použitím simvastatinu a midazolamu jako markerových substrátů pro CYP3A4 byly provedeny u 24 zdravých žen po menopauze. Výsledky těchto studií prokázaly, že farmakokinetika substrátů CYP3A4 nebyla ovlivněna ustálenými koncentracemi DRSP dosaženými po podání 3 mg DRSP/den.
Ženy na substituční terapii hormony štítné žlázy mohou potřebovat zvýšené dávky hormonů štítné žlázy, protože sérová koncentrace globulinu vázajícího štítnou žlázu se zvyšuje s užíváním COC.
Interakce s léky, které mají potenciál zvýšit koncentraci draslíku v séru: Existuje potenciál pro zvýšení koncentrace draslíku v séru u žen užívajících Yasmin 3 mg s jinými léky, které mohou zvýšit koncentraci draslíku v séru (viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ].
Studie lékových interakcí DRSP 3 mg/estradiol (E2) 1 mg versus placebo byla provedena u 24 mírně hypertenzních postmenopauzálních žen užívajících enalapril maleát 10 mg dvakrát denně. Koncentrace draslíku byly u všech subjektů získávány každý druhý den po dobu celkem 2 týdnů. Průměrné koncentrace draslíku v séru ve skupině léčené DRSP/E2 vzhledem k výchozí hodnotě byly o 0,22 mEq/l vyšší než ve skupině s placebem. Koncentrace draslíku v séru byly také měřeny ve více časových bodech během 24 hodin na začátku a v den 14. V den 14 byly poměry Cmax a AUC draslíku v séru ve skupině DRSP/E2 k těm ve skupině s placebem 0,955 (90% CI : 0,914, 0,999) a 1,010 (90% CI: 0,944, 1,08). U žádného pacienta v žádné z léčebných skupin nedošlo k rozvoji hyperkalémie (koncentrace draslíku v séru > 5,5 mEq/l).
Klinické studie
Ve studiích klinické účinnosti trvajících až 2 roky dokončilo 2 629 subjektů 33 160 cyklů užívání bez jakékoli jiné antikoncepce. Průměrný věk subjektů byl 25,5 ± 4,7 let. Věkové rozmezí bylo 16 až 37 let. Rasová demografická skupina byla: 83 % bělochů, 1 % hispánců, 1 % černochů,
INFORMACE PRO PACIENTA
Průvodce používáním Yasmin
VAROVÁNÍ PRO ŽENY, KTERÉ KOUŘÍ
Nepoužívejte Yasmin, pokud kouříte cigarety a jste starší 35 let. Kouření zvyšuje riziko závažných kardiovaskulárních vedlejších účinků (problémy se srdcem a krevními cévami) antikoncepčních pilulek, včetně úmrtí na srdeční infarkt, krevní sraženiny nebo mrtvici. Toto riziko se zvyšuje s věkem a počtem vykouřených cigaret.
Antikoncepční pilulky pomáhají snížit pravděpodobnost otěhotnění, pokud se užívají podle pokynů. Nechrání před infekcí HIV (AIDS) a jinými pohlavně přenosnými chorobami.
Co je Yasmin 3 mg?
Yasmin je antikoncepční pilulka. Obsahuje dva ženské hormony, syntetický estrogen zvaný ethinylestradiol a progestin zvaný drospirenon.
Progestin drospirenon může zvýšit draslík. Proto byste neměli užívat Yasmin 3 mg, pokud máte onemocnění ledvin, jater nebo nadledvin, protože by to mohlo způsobit vážné srdeční a zdravotní problémy. Jiné léky mohou také zvýšit draslík. Pokud se v současné době denně, dlouhodobě léčíte chronického onemocnění některým z níže uvedených léků, měli byste se poradit se svým poskytovatelem zdravotní péče, zda je pro vás přípravek Yasmin 3 mg vhodný, a během prvního měsíce, kdy užíváte přípravek Yasmin, byste měli krevní test ke kontrole hladiny draslíku.
- NSAID (ibuprofen [Motrin, Advil], naproxen [Aleve a další], pokud jsou užívány dlouhodobě a denně k léčbě artritidy nebo jiných problémů)
- Draslík šetřící diuretika (spironolakton a další)
- Suplementace draslíku
- ACE inhibitory (Capoten, Vasotec, Zestril a další)
- Antagonisté receptoru angiotenzinu II (Cozaar, Diovan, Avapro a další)
- heparin
- Antagonisté aldosteronu
Jak dobře Yasmin funguje?
Vaše šance na otěhotnění závisí na tom, jak dobře dodržujete pokyny pro užívání antikoncepčních pilulek. Čím lépe budete postupovat podle pokynů, tím menší máte šanci otěhotnět.
Na základě výsledků dvou klinických studií může přibližně 1 žena ze 100 žen otěhotnět během prvního roku užívání přípravku Yasmin.
Následující tabulka ukazuje šanci na otěhotnění u žen, které používají různé metody antikoncepce. Každý rámeček v grafu obsahuje seznam metod antikoncepce, které mají podobnou účinnost. Nejúčinnější metody jsou v horní části tabulky. Rámeček ve spodní části grafu ukazuje šanci na otěhotnění u žen, které nepoužívají antikoncepci a snaží se otěhotnět.
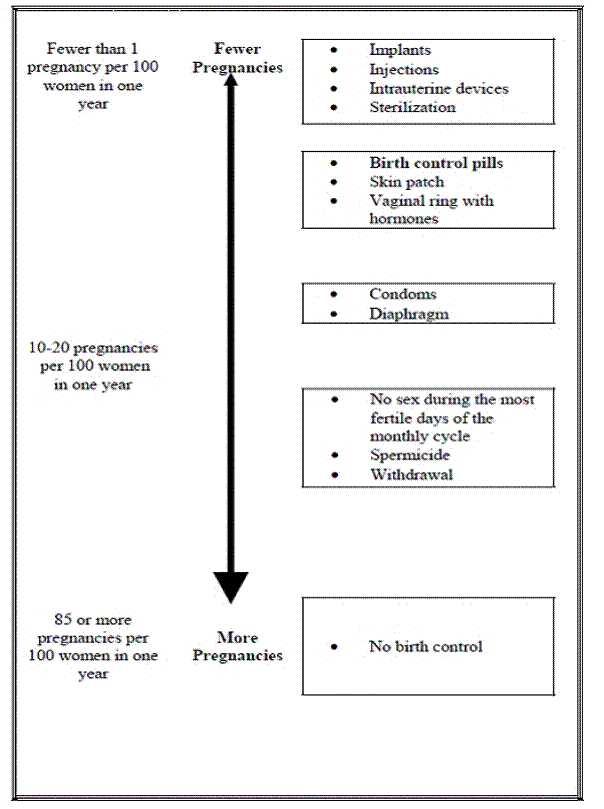
Jak beru Yasmin?
1. Přečtěte si tyto pokyny než začnete užívat své pilulky nebo kdykoli si nejste jisti, co máte dělat.
2. Správný způsob užívání pilulky je užívat jednu pilulku každý den ve stejnou dobu v pořadí uvedeném na obalu. Tabletu užívejte nejlépe po večeři nebo před spaním a podle potřeby ji zapijte trochou tekutiny. Yasmin lze užívat bez ohledu na jídlo.
Pokud vynecháte pilulky, můžete otěhotnět. To zahrnuje pozdní spuštění balíčku. Čím více pilulek vynecháte, tím je pravděpodobnější, že otěhotníte. Viz níže „CO DĚLAT, POKUD VÁM VYJÁDŘÍ PILULKY“.
3. Mnoho žen má špinění nebo slabé krvácení v neočekávaných časech nebo se jim může během prvních 1-3 balení pilulek cítit špatně od žaludku.
Pokud se u Vás objeví špinění nebo slabé krvácení nebo se Vám bude dělat nevolno, pilulku nepřestávejte. Problém obvykle zmizí. Pokud nezmizí, poraďte se se svým poskytovatelem zdravotní péče.
4. Chybějící pilulky mohou také způsobit špinění nebo slabé krvácení, i když tyto vynechané pilulky doplníte. Ve dnech, kdy si vezmete dvě pilulky, abyste nahradili vynechané pilulky, by vám také mohlo být trochu špatně od žaludku.
5. Pokud zvracíte (během 3 až 4 hodin po požití pilulky), měli byste postupovat podle pokynů v části „CO DĚLAT, POKUD VYNECHÁTE PILULKY“. Pokud máte průjem nebo užíváte určité léky, včetně některých antibiotik a některých rostlinných produktů, jako je třezalka tečkovaná, vaše pilulky nemusí tak dobře fungovat.
Používejte záložní metodu (jako jsou kondomy a spermicidy), dokud se nezkontrolujete u svého poskytovatele zdravotní péče.
6. Pokud máte potíže se zapamatováním si pilulky, poraďte se se svým poskytovatelem zdravotní péče o tom, jak si usnadnit užívání pilulek nebo o použití jiné metody antikoncepce.
7. Máte-li jakékoli dotazy nebo si nejste jisti informacemi v tomto letáku, zavolejte svého poskytovatele zdravotní péče.
Než začnete brát své prášky
1. Rozhodněte se, v jakou denní dobu si chcete vzít pilulku Je důležité užívat Yasmin 3 mg v pořadí uvedeném na obalu každý den ve stejnou dobu, nejlépe po večeři nebo před spaním, podle potřeby s trochou tekutiny. Yasmin lze užívat bez ohledu na jídlo.
2. Podívejte se na své balení pilulek – obsahuje 28 pilulek
Balení pilulek Yasmin obsahuje 21 žlutých pilulek (s hormony), které se mají užívat po dobu tří týdnů, následovaných 7 bílými pilulkami (bez hormonů), které se užívají po dobu jednoho týdne.
3. Hledejte také:
a) Kde na balení začít užívat pilulky,
b) V jakém pořadí užívat pilulky (postupujte podle šipek)
4. Ujistěte se, že máte vždy připravený (a) jiný druh antikoncepce (jako jsou kondomy a spermicidy), který použijete jako zálohu pro případ, že byste pilulky vynechali, a (b) další plné balení pilulek.
Kdy začít s prvním balením pilulek
Máte na výběr, který den začnete užívat své první balení pilulek. Rozhodněte se se svým poskytovatelem zdravotní péče, který den je pro vás nejlepší. Vyberte si denní dobu, kterou si budete snadno pamatovat.
Začátek dne 1:
1. Užijte první žlutou pilulku z balení během prvních 24 hodin menstruace.
2. Nebudete muset používat záložní metodu antikoncepce, protože začnete užívat pilulku na začátku menstruace. Pokud však začnete Yasmin 3 mg později než první den menstruace, měla byste použít jinou metodu antikoncepce (jako je kondom a spermicid) jako záložní metodu, dokud neužijete 7 žlutých pilulek.
Nedělní začátek:
1. Užijte první žlutou pilulku z balení v neděli po začátku menstruace, i když stále krvácíte. Pokud vaše menstruace začíná v neděli, začněte s balením ještě tentýž den.
2. Použijte jinou metodu antikoncepce (jako je kondom a spermicid) jako záložní metodu, pokud máte sex kdykoli od neděle, kdy začnete užívat první balení, do příští neděle (7 dní). To platí také v případě, že začnete Yasmin užívat poté, co jste byla těhotná a od těhotenství jste nedostala menstruaci.
Když přejdete z jiné antikoncepční pilulky
Při přechodu z jiné antikoncepční pilulky by měla být Yasmin zahájena ve stejný den, kdy by bylo zahájeno užívání nového balení předchozí antikoncepční pilulky.
Když přejdete z jiného typu metody antikoncepce
Při přechodu z transdermální náplasti nebo vaginálního kroužku by měla být Yasmin 3 mg zahájena v době, kdy měla být další aplikace. Při přechodu z injekce by měla být Yasmin zahájena v době, kdy měla být podána další dávka. Při přechodu z nitroděložní antikoncepce nebo implantátu by měla být Yasmin zahájena v den vyjmutí.
Co dělat během měsíce
1. Užívejte jednu pilulku každý den ve stejnou dobu, dokud se balení nevyprázdní.
Nevynechávejte pilulky, i když mezi jednotlivými menstruacemi špiníte nebo krvácíte nebo je vám špatně od žaludku (nevolnost).
Nevynechávejte pilulky, i když nemáte příliš často sex.
2. Když vypijete balení pilulek, začněte s dalším balením den po vaší poslední bílé pilulce. Mezi baleními nečekejte žádné dny.
Co dělat, když vám chybí prášky
Pokud vynecháte 1 žlutou pilulku z vašeho balení:
- Vezměte si to, jakmile si vzpomenete. Další pilulku si vezměte v obvyklou dobu. To znamená, že můžete užít dvě pilulky v jeden den.
- Pokud máte sex, nemusíte používat záložní metodu antikoncepce.
Pokud vynecháte 2 žluté pilulky za sebou v 1. nebo 2. týdnu vašeho balení:
- Vezměte si dvě pilulky v den, kdy si vzpomenete, a dvě pilulky další den.
- Poté užívejte jednu pilulku denně, dokud nedokončíte balení.
- Mohla byste otěhotnět, pokud budete mít sex do 7 dnů po opětovném užívání pilulek. Po dobu těchto 7 dní musíte jako zálohu použít jinou metodu antikoncepce (jako je kondom a spermicid).
Pokud vynecháte 2 žluté pilulky za sebou ve 3. nebo 4. týdnu vašeho balení:
1. Pokud jste začátečník dne 1:
Vyhoďte zbytek balení pilulek a tentýž den začněte s novým balením.
2. Pokud jste začátečník v neděli:
Pokračujte v užívání jedné pilulky každý den až do neděle. V neděli vyhoďte zbytek balení a tentýž den začněte užívat nové balení pilulek.
3. Mohla byste otěhotnět, pokud budete mít sex do 7 dnů po opětovném užívání pilulek. Po dobu těchto 7 dní musíte jako zálohu použít jinou metodu antikoncepce (jako je kondom a spermicid).
4. Možná nebudete mít tento měsíc menstruaci, ale to se očekává. Pokud však vynecháte menstruaci dva měsíce po sobě, zavolejte svému poskytovateli zdravotní péče, protože byste mohla být těhotná.
Pokud vynecháte 3 nebo více žlutých pilulek za sebou během kteréhokoli týdne:
1. Pokud jste začátečník dne 1:
Vyhoďte zbytek balení pilulek a tentýž den začněte s novým balením.
2. Pokud jste začátečník v neděli:
Pokračujte v užívání 1 pilulky každý den až do neděle. V neděli vyhoďte zbytek balení a tentýž den začněte užívat nové balení pilulek.
3. Mohla byste otěhotnět, pokud budete mít sex do 7 dnů po opětovném užívání pilulek. Po dobu těchto 7 dnů musíte jako zálohu použít jinou metodu kontroly porodnosti (jako jsou kondomy a spermicidy).
4. Možná nebudete mít tento měsíc menstruaci, ale to se očekává. Pokud však vynecháte menstruaci dva měsíce po sobě, zavolejte svému poskytovateli zdravotní péče, protože byste mohla být těhotná.
Pokud vynecháte některou ze 7 bílých pilulek ve 4. týdnu:
Vyhoďte prášky, které jste vynechali.
Pokračujte v užívání jedné pilulky každý den, dokud se balení nevyprázdní.
Nepotřebujete záložní metodu.
Nakonec, pokud si stále nejste jisti, co dělat s pilulkami, které jste vynechali:
Kdykoli máte sex, použijte záložní metodu (jako jsou kondomy a spermicidy).
Kontaktujte svého poskytovatele zdravotní péče a pokračujte v užívání jedné aktivní žluté pilulky každý den, dokud nebude uvedeno jinak.
KDO BY NEMĚL UŽÍVAT Yasmin?
Váš poskytovatel zdravotní péče vám Yasmin 0,03 mg neposkytne, pokud:
- Měl jste někdy krevní sraženiny v nohách (hluboká žilní trombóza), plicích (plicní embolie) nebo očích (trombóza sítnice)
- Měl jsi někdy mrtvici
- Měl jsi někdy infarkt
- Máte určité problémy se srdeční chlopní nebo abnormality srdečního rytmu, které mohou způsobit tvorbu krevních sraženin v srdci
- Máte zděděný problém s krví, kvůli kterému se sráží více než normálně
- Máte vysoký krevní tlak, který léky nemohou ovlivnit
- Máte cukrovku s poškozením ledvin, očí, nervů nebo krevních cév
- Měl jste někdy určité druhy silných migrénových bolestí hlavy s aurou, necitlivostí, slabostí nebo změnami vidění
- Měla jste někdy rakovinu prsu nebo jinou rakovinu, která je citlivá na ženské hormony
- Máte onemocnění jater, včetně nádorů jater
- Máte onemocnění ledvin
- Máte onemocnění nadledvin
Také neužívejte antikoncepční pilulky, pokud:
- Kouří a jsou starší 35 let
- Jste nebo máte podezření, že jste těhotná
Antikoncepční pilulky pro vás nemusí být dobrou volbou, pokud jste někdy měla žloutenku (zežloutnutí kůže nebo očí) způsobenou těhotenstvím (také nazývaná těhotenská cholestáza).
Informujte svého poskytovatele zdravotní péče, pokud jste někdy měli některý z výše uvedených stavů (váš poskytovatel zdravotní péče může doporučit jiný způsob antikoncepce).
Co dalšího bych měl vědět o užívání Yasmin?
Antikoncepční pilulky vás nechrání před žádnou sexuálně přenosnou nemocí, včetně HIV, viru, který způsobuje AIDS.
Nevynechávejte žádné pilulky, i když nemáte často sex.
Pokud vynecháte menstruaci, můžete být těhotná. Některým ženám však vynechává menstruace nebo mají mírnou menstruaci na antikoncepčních pilulkách, i když nejsou těhotné. Obraťte se na svého poskytovatele zdravotní péče o radu, pokud:
- Myslíš si, že jsi těhotná
- Vynecháte jednu menstruaci a nevezmete si antikoncepční pilulky každý den včas
- Chybí dvě třetiny za sebou
Antikoncepční pilulky by se v těhotenství neměly užívat. Není však známo, že by antikoncepční pilulky, které byly požity náhodou během těhotenství, způsobovaly vrozené vady.
Vzhledem ke zvýšenému riziku krevních sraženin byste měl(a) vysadit přípravek Yasmin 0,03 mg nejméně čtyři týdny před velkým chirurgickým zákrokem a nepokračovat jej znovu nejméně dva týdny po operaci.
Pokud kojíte, zvažte jinou metodu antikoncepce, dokud nebudete připravena přestat kojit. Antikoncepční pilulky, které obsahují estrogen, jako je Yasmin, mohou snížit množství vyrobeného mléka. Malé množství hormonů pilulky přechází do mateřského mléka.
Pokud zvracíte nebo máte průjem, vaše antikoncepční pilulky nemusí také fungovat. Vezměte si další pilulku, pokud zvracíte do 3-4 hodin po užití pilulky, nebo použijte jinou metodu antikoncepce, jako jsou kondomy a spermicid, dokud se nezkontrolujete u svého poskytovatele zdravotní péče.
Pokud máte naplánované nějaké laboratorní testy, řekněte svému lékaři, že užíváte antikoncepční pilulky. Některé krevní testy mohou být ovlivněny antikoncepčními pilulkami.
Informujte svého poskytovatele zdravotní péče o všech lécích, které užíváte, včetně léků na předpis a volně prodejných léků, vitamínů a bylinných doplňků.
Yasmin může ovlivnit účinek jiných léků a jiné léky mohou ovlivnit účinek Yasminu 3 mg. Znát léky, které užíváte.
Uchovávejte si jejich seznam, abyste je mohli ukázat svému poskytovateli zdravotní péče a lékárníkovi, když dostanete nový lék.
Jaká jsou nejzávažnější rizika užívání antikoncepčních pilulek?
Stejně jako těhotenství zvyšují antikoncepční pilulky riziko závažných krevních sraženin (viz následující graf), zejména u žen, které mají jiné rizikové faktory, jako je kouření, obezita nebo věk vyšší než 35 let. Toto zvýšené riziko je nejvyšší, když poprvé začnete užívat antikoncepční pilulky a když znovu zahájíte stejné nebo jiné antikoncepční pilulky poté, co je měsíc nebo déle nepoužíváte. Ženy, které užívají antikoncepční pilulky s drospirenonem (jako Yasmin), mohou mít vyšší riziko vzniku krevní sraženiny. Některé studie uvádějí, že riziko krevních sraženin bylo vyšší u žen, které užívají antikoncepční pilulky, které obsahují drospirenon, než u žen, které užívají antikoncepční pilulky, které drospirenon neobsahují.
Promluvte si se svým poskytovatelem zdravotní péče o svém riziku vzniku krevní sraženiny, než se rozhodnete, která antikoncepční pilulka je pro vás ta pravá.
Je možné zemřít nebo být trvale invalidní na problém způsobený krevní sraženinou, jako je infarkt nebo mrtvice. Některé příklady závažných sraženin jsou krevní sraženiny v:
- Nohy (hluboká žilní trombóza nebo DVT)
- Plíce (plicní embolie nebo PE)
- Oči (ztráta zraku)
- Srdce (infarkt)
- Mozková mrtvice)
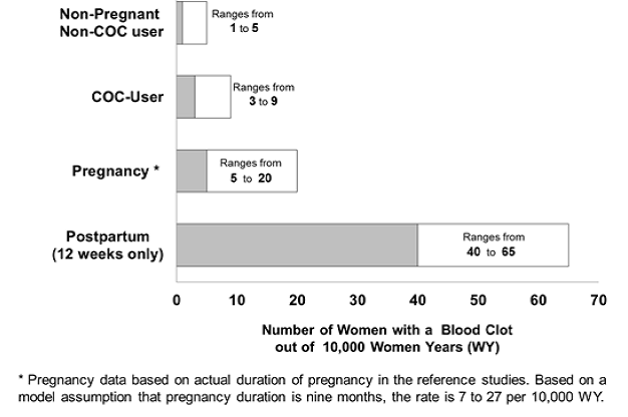
Abychom uvedli riziko vzniku krevní sraženiny do perspektivy: Pokud je po dobu jednoho roku sledováno 10 000 žen, které nejsou těhotné a neužívají antikoncepční pilulky, u 1 až 5 z těchto žen se vyvine krevní sraženina. Obrázek níže ukazuje pravděpodobnost vzniku závažné krevní sraženiny u žen, které nejsou těhotné a neužívají antikoncepční pilulky, u žen, které užívají antikoncepční pilulky, u těhotných žen a u žen v prvních 12 týdnech po porodu. .
Pravděpodobnost vzniku vážné krevní sraženiny
Několik žen, které užívají antikoncepční pilulky, může dostat:
- Vysoký krevní tlak
- Problémy se žlučníkem
- Vzácné rakovinné nebo nezhoubné nádory jater
Všechny tyto příhody jsou u zdravých žen neobvyklé.
Okamžitě zavolejte svého poskytovatele zdravotní péče, pokud máte:
- Trvalá bolest nohou
- Náhlá dušnost
- Náhlá slepota, částečná nebo úplná
- Silná bolest na hrudi
- Náhlá, silná bolest hlavy na rozdíl od vašich obvyklých bolestí hlavy
- Slabost nebo necitlivost v ruce nebo noze nebo potíže s mluvením
- Zežloutnutí kůže nebo oční bulvy
Jaké jsou běžné vedlejší účinky antikoncepčních pilulek?
Nejčastější vedlejší účinky antikoncepčních pilulek jsou:
- Špinění nebo krvácení mezi menstruačními obdobími
- Nevolnost
- Citlivost prsou
- Bolest hlavy
Tyto nežádoucí účinky jsou obvykle mírné a obvykle časem vymizí.
Méně časté nežádoucí účinky jsou:
- Akné
- Menší sexuální touha
- Nadýmání nebo zadržování tekutin
- Skvrnité ztmavnutí kůže, zejména na obličeji
- Vysoká hladina cukru v krvi, zejména u žen, které již mají cukrovku
- Vysoká hladina tuků (cholesterolu; triglyceridů) v krvi
- Deprese, zvláště pokud jste v minulosti trpěli depresí. Okamžitě zavolejte svého poskytovatele zdravotní péče, pokud máte myšlenky na sebepoškození.
- Problémy s tolerancí kontaktních čoček
- Změny hmotnosti
Toto není úplný seznam možných vedlejších účinků. Promluvte si se svým poskytovatelem zdravotní péče, pokud se u Vás objeví nežádoucí účinky, které se Vás týkají. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
Při předávkování antikoncepčními pilulkami nebyly hlášeny žádné vážné problémy, a to ani v případě náhodného požití dětmi.
Způsobují antikoncepční pilulky rakovinu?
Zdá se, že antikoncepční pilulky nezpůsobují rakovinu prsu. Pokud však máte rakovinu prsu nyní nebo jste ji měla v minulosti, neužívejte antikoncepční pilulky, protože některé rakoviny prsu jsou citlivé na hormony.
Ženy, které užívají antikoncepční pilulky, mohou mít o něco vyšší šanci na rakovinu děložního čípku. To však může být způsobeno jinými důvody, jako je více sexuálních partnerů.
Co bych měl vědět o své menstruaci, když užívám Yasmin?
Během užívání přípravku Yasmin se může objevit nepravidelné vaginální krvácení nebo špinění. Nepravidelné krvácení se může lišit od mírného špinění mezi menstruačními obdobími až po průnikové krvácení, což je proud podobný pravidelné menstruaci. Nepravidelné krvácení se objevuje nejčastěji během prvních několika měsíců užívání perorální antikoncepce, ale může se objevit i poté, co jste pilulku nějakou dobu užívala. Takové krvácení může být dočasné a obvykle neznamená žádné vážné problémy. Je důležité pokračovat v užívání pilulek podle plánu. Pokud se krvácení objeví ve více než jednom cyklu, je neobvykle silné nebo trvá déle než několik dní, zavolejte svého poskytovatele zdravotní péče.
Některé ženy nemusí mít menstruaci, ale to by nemělo být důvodem k obavám, pokud užíváte pilulky pravidelně a včas.
Co když při užívání Yasmin zmeškám naplánované období?
Vynechání menstruace není neobvyklé. Pokud však vynecháte dvě menstruace za sebou nebo vynecháte jednu menstruaci, když jste neužívala antikoncepční pilulky pravidelně a včas, zavolejte svého poskytovatele zdravotní péče. Také informujte svého poskytovatele zdravotní péče, pokud máte příznaky těhotenství, jako je ranní nevolnost nebo neobvyklá citlivost prsou. Je důležité, aby vás váš poskytovatel zdravotní péče zkontroloval, aby zjistil, zda jste těhotná. Přestaňte užívat Yasmin 3 mg, pokud jste těhotná.
Co když chci otěhotnět?
Můžete přestat užívat pilulku, kdykoli budete chtít. Zvažte návštěvu svého poskytovatele zdravotní péče za účelem kontroly před těhotenstvím, než přestanete pilulku užívat.
Obecné rady o Yasmin
Váš poskytovatel zdravotní péče vám předepsal Yasmin 0,03 mg. Prosím, nesdílejte Yasmin s nikým jiným. Uchovávejte Yasmin mimo dosah dětí.
Máte-li obavy nebo dotazy, zeptejte se svého poskytovatele zdravotní péče. Můžete také požádat svého poskytovatele zdravotní péče o podrobnější štítek napsaný pro lékařské odborníky.
