Robaxin 500mg Methocarbamol Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Robaxin 500 mg a jak se používá?
Robaxin 500 mg je lék na předpis používaný k léčbě příznaků svalových křečí způsobených bolestí nebo zraněním a tetanem. Robaxin 500 mg lze užívat samostatně nebo s jinými léky.
- Robaxin 500 mg patří do skupiny léků nazývaných relaxanty kosterního svalstva.
- Není známo, zda je přípravek Robaxin 500 mg bezpečný a účinný u dětí mladších 16 let.
Jaké jsou možné vedlejší účinky přípravku Robaxin 500 mg?
Robaxin 500 mg může způsobit závažné nežádoucí účinky včetně:
- točení hlavy,
- pomalý srdeční tep,
- horečka,
- zimnice,
- příznaky chřipky,
- záchvat (křeče) a
- zežloutnutí kůže nebo očí (žloutenka)
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější vedlejší účinky Robaxinu patří:
- závrať,
- ospalost,
- nevolnost,
- zvracení,
- žaludeční nevolnost,
- návaly horka (teplo, zarudnutí nebo pocit brnění),
- zmatek,
- problémy s pamětí,
- rozmazané vidění,
- dvojité vidění,
- problémy se spánkem (nespavost) a
- nedostatek koordinace
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky Robaxinu. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
POPIS
robaxin®/robaxin®-750 (methokarbamolové tablety, USP), karbamátový derivát guaifenesinu, je látka tlumící centrální nervový systém (CNS) se sedativními a muskuloskeletálními relaxačními vlastnostmi.
Chemický název methokarbamolu je 3-(2-methoxyfenoxy)-1,2propandiol-1-karbamát a má empirický vzorec C11H15NO5. Jeho molekulová hmotnost je 241,24. Strukturní vzorec je uveden níže.
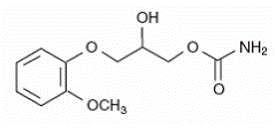
Methokarbamol je bílý prášek, málo rozpustný ve vodě a chloroformu, rozpustný v alkoholu (pouze při zahřívání) a propylenglykolu a nerozpustný v benzenu a n-hexanu.
robaxin® je dostupný jako světle oranžová, kulatá, potahovaná tableta obsahující 500 mg methokarbamolu, USP pro perorální podání. Přítomné neaktivní složky jsou kukuřičný škrob, FD&C Yellow 6, hydroxypropylcelulóza, hypromelóza, magnesium-stearát, polysorbát 20, povidon, propylenglykol, sodná sůl sacharinu, laurylsulfát sodný, sodná sůl glykolátu škrobu, kyselina stearová, oxid titaničitý.
robaxin®-750 je dostupný jako oranžová potahovaná tableta ve tvaru kapsle obsahující 750 mg methokarbamolu, USP pro perorální podání. Kromě neaktivních složek přítomných v robaxinu® obsahuje robaxin® 750 také D&C Yellow 10.
INDIKACE
Injekční forma methokarbamolu je indikována jako doplněk k odpočinku, fyzikální terapii a dalším opatřením k úlevě od nepohodlí spojených s akutními bolestivými muskuloskeletálními stavy. Způsob účinku tohoto léku nebyl jasně identifikován, ale může souviset s jeho sedativními vlastnostmi. Methokarbamol u člověka přímo neuvolňuje napjaté kosterní svaly.
DÁVKOVÁNÍ A PODÁVÁNÍ
Pouze pro intravenózní a intramuskulární použití. Celková dávka pro dospělého by neměla překročit 30 ml (3 lahvičky) denně po dobu delší než 3 po sobě jdoucí dny s výjimkou léčby tetanu. Pokud stav přetrvává, lze podobný průběh opakovat po 48hodinovém intervalu bez léku. Dávkování a frekvence injekcí by měly být založeny na závažnosti léčeného stavu a zaznamenané terapeutické odpovědi.
Pro zmírnění příznaků středního stupně může být dostatečná jedna dávka 1 gram (jedna 10ml lahvička). Obvykle se tato injekce nemusí opakovat, protože podání orální formy obvykle udrží úlevu iniciovanou injekcí. V nejzávažnějších případech nebo v pooperačních stavech, kdy perorální podání není možné, lze další dávky 1 gramu opakovat každých 8 hodin až do maximální dávky 3 g/den po dobu nejvýše 3 po sobě jdoucích dnů.
Pokyny pro intravenózní použití
ROBAXIN Injectable lze podávat neředěný přímo do žíly maximální rychlostí 3 ml za minutu. Může být také přidán do intravenózní injekce chloridu sodného (sterilní izotonický roztok chloridu sodného pro parenterální použití) nebo pětiprocentní injekce dextrózy (sterilní 5procentní roztok dextrózy); jedna lahvička podaná jako jedna dávka by neměla být naředěna na více než 250 ml pro IV infuzi. PO SMĚSENÍ S IV INFŮZNÍ TEKUTINOU NECHLAZUJTE. Je třeba postupovat opatrně, aby nedošlo k vaskulární extravazaci tohoto hypertonického roztoku, která může vést k tromboflebitidě. Je výhodné, aby byl pacient během injekce a alespoň 10 až 15 minut po injekci v poloze vleže.
Pokyny pro intramuskulární použití
Pokud je indikována intramuskulární cesta, nemělo by být do každé gluteální oblasti injikováno více než pět ml (polovina lahvičky). V případě potřeby lze injekce opakovat v osmihodinových intervalech. Když je dosaženo uspokojivé úlevy od příznaků, lze ji obvykle udržet pomocí tablet.
Nedoporučuje se pro subkutánní podání.
Zvláštní pokyny pro použití při tetanu
Existují klinické důkazy, které naznačují, že methokarbamol může mít příznivý účinek při kontrole neuromuskulárních projevů tetanu. Nenahrazuje však obvyklý postup debridementu, tetanový antitoxin, penicilin, tracheotomii, péči o rovnováhu tekutin a podpůrnou péči. ROBAXIN Injectable by měl být přidán do režimu co nejdříve.
Pro dospělé
Vstříkněte jednu nebo dvě lahvičky přímo do hadičky dříve zavedené jehly. Do infuzní lahve lze přidat dalších 10 ml nebo 20 ml, takže celkem je podáno až 30 ml (tři lahvičky) jako počáteční dávka (viz OPATŘENÍ ). Tento postup by se měl opakovat každých šest hodin, dokud podmínky neumožňují zavedení nazogastrické sondy. Touto trubicí pak mohou být podávány rozdrcené tablety methokarbamolu suspendované ve vodě nebo fyziologickém roztoku. Podle odpovědi pacienta mohou být vyžadovány celkové denní perorální dávky až 24 gramů.
Pro dětské pacienty
Doporučuje se minimální počáteční dávka 15 mg/kg nebo 500 mg/m². Tato dávka se může v případě potřeby opakovat každých šest hodin. Celková dávka by neměla překročit 1,8 g/m² po dobu 3 po sobě jdoucích dnů. Udržovací dávka může být podána injekcí do hadičky nebo intravenózní infuzí s vhodným množstvím tekutiny. Viz návod pro IV použití.
JAK DODÁVÁNO
ROBAXIN 500 mg injekčně (100 mg/ml) dodáváno v - 10ml jednodávkových lahvičkách v balení po 25 ( NDC 0641-6103-25).
Skladujte při 20°- 25°C (68°- 77°F), ionty se vylučují do 15°- 30°C (59°- 86°F).
Není vyrobeno z přírodního kaučukového latexu.
Chcete-li nahlásit PODEZŘELNÉ NEŽÁDOUCÍ REAKCE, kontaktujte společnost West-Ward Pharmaceuticals Corp. na čísle 1-877-845-0689 nebo FDA na čísle 1-800-FDA-1088 nebo www.fda.gov/medwatch.
Pro dotaz na produkt volejte 1-877-845-0689.
Výrobce: WEST-WARD A HIKMA COMPANY, Eatontown, NJ 07724 USA. Revize: říjen 2017
VEDLEJŠÍ EFEKTY
Následující nežádoucí účinky byly hlášeny souběžně s podáváním methokarbamolu. Některé příhody mohly být způsobeny příliš vysokou rychlostí intravenózní injekce.
Tělo jako celek: Anafylaktická reakce, angioneurotický edém, horečka, bolest hlavy
Kardiovaskulární systém: Bradykardie, návaly horka, hypotenze, synkopa, tromboflebitida
Ve většině případů synkopy došlo ke spontánnímu zotavení. V jiných byl k urychlení zotavení použit adrenalin, injekční steroidy a/nebo injekční antihistaminika.
Zažívací ústrojí: Dyspepsie, žloutenka (včetně cholestatické žloutenky), nevolnost a zvracení
Hemický a lymfatický systém: Leukopenie
Imunitní systém: Hypersenzitivní reakce

Nervový systém: Amnézie, zmatenost, diplopie, závrať nebo točení hlavy, ospalost, nespavost, mírná svalová nekoordinace, nystagmus, sedace, záchvaty (včetně grand mal), vertigo
U pacientů se záchvatovými poruchami byl hlášen vznik konvulzivních záchvatů během intravenózního podání methokarbamolu. Přispívajícím faktorem mohlo být psychické trauma z procedury. Ačkoli několik pozorovatelů hlásilo úspěch při ukončení epileptiformních záchvatů pomocí přípravku ROBAXIN Injectable, jeho podávání pacientům s epilepsií se nedoporučuje (viz OPATŘENÍ , Všeobecné ).
Kůže a speciální smysly: Rozmazané vidění, konjunktivitida, ucpaný nos, kovová chuť, pruritus, vyrážka, kopřivka
Jiný: Bolest a olupování v místě vpichu
DROGOVÉ INTERAKCE
Vidět VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ pro interakci s léky na CNS a alkoholem.
Methokarbamol může inhibovat účinek pyridostigmin-bromidu. Proto by měl být methokarbamol používán s opatrností u pacientů s myasthenia gravis užívajících anticholinesterázu.
Interakce drog/laboratorních testů
Methokarbamol může způsobit barevnou interferenci v určitých screeningových testech na kyselinu 5-hydroxyindoloctovou (5-HIAA) s použitím nitrosonaftolového činidla a ve screeningových testech na močovou kyselinu vanillylmandlovou (VMA) pomocí Gitlowovy metody.
VAROVÁNÍ
Protože methokarbamol může mít obecný tlumivý účinek na CNS, pacienti užívající ROBAXIN Injectable by měli být upozorněni na kombinované účinky s alkoholem a jinými látkami tlumícími CNS.
Bezpečné použití přípravku ROBAXIN Injectable nebylo stanoveno s ohledem na možné nepříznivé účinky na vývoj plodu. Po expozici methokarbamolu in utero byly velmi vzácně hlášeny fetální a vrozené abnormality. Proto by ROBAXIN Injectable neměl být používán u žen, které jsou nebo mohou otěhotnět, a zejména během časného těhotenství, pokud podle úsudku lékaře potenciální přínosy nepřeváží možná rizika (viz OPATŘENÍ , Těhotenství ).
Použití při činnostech vyžadujících duševní bdělost
Methokarbamol může narušit duševní a/nebo fyzické schopnosti potřebné pro provádění nebezpečných úkolů, jako je obsluha strojů nebo řízení motorového vozidla. Pacienti by měli být upozorněni na obsluhu strojů, včetně automobilů, dokud si nejsou přiměřeně jisti, že léčba methokarbamolem nepříznivě neovlivňuje jejich schopnost zapojit se do takových činností.
OPATŘENÍ
Všeobecné
Stejně jako u jiných látek podávaných buď intravenózně nebo intramuskulárně, je třeba pečlivě sledovat dávku a rychlost injekce. Rychlost injekce by neměla překročit 3 ml za minutu – tj. jedna 10ml lahvička za přibližně tři minuty. Protože ROBAXIN 500 mg Injectable je hypertonický, je třeba se vyvarovat vaskulární extravazace. Poloha vleže sníží pravděpodobnost vedlejších reakcí.
Krev nasátá do stříkačky se nemísí s hypertonickým roztokem. Tento jev se vyskytuje u mnoha dalších intravenózních přípravků. Krev může být injikována s methokarbamolem nebo může být injekce zastavena, když píst dosáhne krve, podle toho, čemu dává lékař přednost.
Celková dávka by neměla překročit 30 ml (tři lahvičky) denně po dobu delší než tři po sobě jdoucí dny s výjimkou léčby tetanu.
Při použití injekční formy u pacientů se suspektními nebo známými záchvatovými poruchami je třeba dbát opatrnosti.
Karcinogeneze, mutageneze, zhoršení plodnosti
Dlouhodobé studie hodnotící karcinogenní potenciál methokarbamolu nebyly provedeny. Nebyly provedeny žádné studie, které by hodnotily účinek methokarbamolu na mutagenezi nebo jeho potenciál narušit plodnost.
Těhotenství
Teratogenní účinky
Kategorie těhotenství C
Reprodukční studie na zvířatech nebyly s methokarbamolem provedeny. Není také známo, zda methokarbamol může způsobit poškození plodu při podání těhotné ženě nebo může ovlivnit reprodukční kapacitu. ROBAXIN 500 mg Injectable by měl být podán těhotné ženě pouze tehdy, je-li to nezbytně nutné.
Bezpečné použití přípravku ROBAXIN Injectable nebylo stanoveno s ohledem na možné nepříznivé účinky na vývoj plodu. Po expozici methokarbamolu in utero byly hlášeny fetální a vrozené abnormality. Proto by ROBAXIN 500 mg Injectable neměl být používán u žen, které jsou nebo mohou otěhotnět, a zejména během časného těhotenství, pokud podle úsudku lékaře potenciální přínosy nepřeváží možná rizika (viz VAROVÁNÍ ).
Kojící matky
Methokarbamol a/nebo jeho metabolity jsou vylučovány do mléka psů; není však známo, zda se methokarbamol nebo jeho metabolity vylučují do lidského mléka. Vzhledem k tomu, že mnoho léků se vylučuje do mateřského mléka, je třeba postupovat opatrně, pokud je ROBAXIN 500 mg injekčně podáván kojící ženě.
Pediatrické použití
Bezpečnost a účinnost přípravku ROBAXIN Injectable u pediatrických pacientů nebyla stanovena s výjimkou tetanu. Vidět DÁVKOVÁNÍ A PODÁVÁNÍ , Speciální pokyny pro Použití při tetanu , Pro dětské pacienty .
PŘEDÁVKOVAT
O akutní toxicitě methokarbamolu jsou dostupné omezené informace. Předávkování methokarbamolem je často spojeno s alkoholem nebo jinými látkami tlumícími CNS a zahrnuje následující příznaky: nauzea, ospalost, rozmazané vidění, hypotenze, křeče a kóma. Po uvedení přípravku na trh byla hlášena úmrtí při předávkování samotným methokarbamolem nebo v přítomnosti jiných látek tlumících CNS, alkoholu nebo psychofarmak.
Léčba
Léčba předávkování zahrnuje symptomatickou a podpůrnou léčbu. Podpůrná opatření zahrnují udržování adekvátních dýchacích cest, monitorování výdeje moči a vitálních funkcí a v případě potřeby podávání nitrožilních tekutin. Užitečnost hemodialýzy při zvládání předávkování není známa.
KONTRAINDIKACE
ROBAXIN 500 mg Injectable by neměl být podáván pacientům se známou nebo suspektní renální patologií. Tato opatrnost je nutná kvůli přítomnosti polyethylenglykolu 300 ve vozidle.
Je známo, že mnohem větší množství polyethylenglykolu 300, než je přítomno v doporučených dávkách přípravku ROBAXIN Injectable, zvyšuje již existující acidózu a retenci močoviny u pacientů s poruchou funkce ledvin. Přestože je množství přítomné v tomto přípravku dobře v rámci bezpečnostních limitů, tato kontraindikace vyžaduje opatrnost.
ROBAXIN Injectable je kontraindikován u pacientů přecitlivělých na methokarbamol nebo na kteroukoli složku injekce.
KLINICKÁ FARMAKOLOGIE
Mechanismus účinku methokarbamolu u lidí nebyl stanoven, ale může být způsoben celkovou útlumem CNS. Nemá přímý účinek na kontraktilní mechanismus příčně pruhovaného svalu, motorickou koncovou ploténku nebo nervové vlákno.
Farmakokinetika
U zdravých dobrovolníků se plazmatická clearance methokarbamolu pohybuje mezi 0,20 a 0,80 l/h/kg, průměrný poločas eliminace z plazmy se pohybuje mezi 1 a 2 hodinami a vazba na plazmatické proteiny se pohybuje mezi 46 % a 50 %.
Methokarbamol je metabolizován dealkylací a hydroxylací. Pravděpodobná je také konjugace methokarbamolu. V podstatě všechny metabolity methokarbamolu jsou eliminovány močí. Malá množství nezměněného methokarbamolu jsou také vylučována močí.
Zvláštní populace
Starší
Průměrný (± SD) poločas eliminace methokarbamolu u starších zdravých dobrovolníků (průměrný (± SD) věk, 69 (± 4) let) byl mírně prodloužen ve srovnání s mladším (průměrný (± SD) věk, 53,3 (± 8,8) ) let), zdravá populace (1,5 (± 0,4) hodiny versus 1,1 (± 0,27) hodiny, v tomto pořadí). Frakce vázaného methokarbamolu byla mírně snížena u starších osob oproti mladším dobrovolníkům (41 až 43 % oproti 46 až 50 %).
Renally Impaired
Clearance methokarbamolu u 8 pacientů s renálním poškozením na udržovací hemodialýze byla snížena asi o 40 % ve srovnání se 17 normálními subjekty, ačkoli průměrný (± SD) poločas eliminace v těchto dvou skupinách byl podobný (1,2 (± 0,6) oproti 1,1 ( ± 0,3) hodin).
Jaterně postižený
8 pacientů se sekundární cirhózou po abúzu alkoholu byla průměrná celková clearance methokarbamolu snížena přibližně o 70 % ve srovnání s hodnotou získanou u 8 normálních jedinců stejného věku a hmotnosti. Průměrný (± SD) poločas eliminace u pacientů s cirhózou a normálních subjektů byl 3,38 (± 1,62) hodin a 1,11 (± 0,27) hodin, v daném pořadí. Procento methokarbamolu vázaného na plazmatické proteiny bylo sníženo na přibližně 40 až 45 % ve srovnání se 46 až 50 % u normálních jedinců.
INFORMACE PRO PACIENTA
Pacienti by měli být upozorněni, že methokarbamol může způsobit ospalost nebo závratě, což může zhoršit jejich schopnost řídit motorová vozidla nebo stroje.
Protože methokarbamol může mít obecný tlumivý účinek na CNS, pacienti by měli být upozorněni na kombinované účinky s alkoholem a jinými látkami tlumícími CNS.
