Ventolin Inhaler 100mcg Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Ventolin a jak se používá?
Ventolin HFA je lék na předpis používaný k léčbě příznaků akutního nebo těžkého astmatu nebo námahou vyvolaného astmatu (bronkospasmus). Ventolin HFA lze užívat samostatně nebo s jinými léky.
Ventolin HFA patří do třídy léků nazývaných Beta2 Agonisté.
Není známo, zda je Ventolin HFA bezpečný a účinný u dětí mladších 4 let.
Jaké jsou možné vedlejší účinky přípravku Ventolin?
Ventolin může způsobit závažné nežádoucí účinky, včetně:
- sípání,
- dusit se,
- dýchací problémy,
- bolest na hrudi,
- rychlý srdeční tep,
- bušení srdce,
- chvění v tvé hrudi,
- těžká bolest hlavy,
- bušení do krku nebo uší,
- bolest nebo pálení při močení,
- zvýšená žízeň,
- zvýšené močení,
- suchá ústa,
- ovocný zápach dechu,
- křeče v nohou,
- zácpa
- nepravidelný srdeční tep,
- necitlivost nebo mravenčení,
- svalová slabost a
- ochablý pocit
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější vedlejší účinky přípravku Ventolin patří:
- bolest na hrudi,
- rychlé nebo bušení srdce,
- závrať,
- cítit se roztřeseně,
- nervozita,
- bolest hlavy,
- bolesti zad,
- bolesti těla,
- žaludeční nevolnost,
- bolest krku,
- bolest dutin a
- rýma nebo ucpaný nos
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky přípravku Ventolin. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
POPIS
Aktivní složkou přípravku VENTOLIN HFA je albuterol sulfát, USP, racemická forma albuterolu a relativně selektivní beta-adrenergní bronchodilatátor. Albuterol sulfát má chemický název α1 - [(terc-butylamino)methyl]-4-hydroxy-m-xylen-α, α'-diol sulfát (2:1) (sůl) a následující chemickou strukturu:
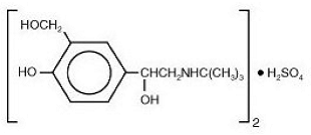
Albuterol sulfát je bílý krystalický prášek s molekulovou hmotností 576,7 a empirický vzorec je (C13H21NO3)2•H2SO4. Je rozpustný ve vodě a mírně rozpustný v ethanolu.
Světovou zdravotnickou organizací doporučený název pro albuterolovou bázi je salbutamol.
VENTOLIN HFA je modrý plastový inhalátor s modrým řemínkem obsahující tlakový aerosolový kanystr s odměřenou dávkou vybavený počítadlem. Každá nádobka obsahuje mikrokrystalickou suspenzi albuterol sulfátu v hnacím plynu HFA-134a (1,1,1,2-tetrafluorethan). Neobsahuje žádné další pomocné látky.
Po naplnění každá aktivace inhalátoru dodá 120 mcg albuterol sulfátu, USP v 75 mg suspenze z ventilu a 108 mcg albuterol sulfátu, USP z náustku (ekvivalent 90 mcg albuterolové báze z náustku).
Před prvním použitím naplňte VENTOLIN HFA, pokud nebyl inhalátor používán déle než 2 týdny nebo když inhalátor upadl. Pro základní nátěr VENTOLIN HFA vypusťte 4 střiky do vzduchu směrem od obličeje a před každým nástřikem dobře protřepejte.
INDIKACE
Bronchospasmus
Inhalační aerosol VENTOLIN® HFA je indikován k léčbě nebo prevenci bronchospasmu u pacientů ve věku 4 let a starších s reverzibilním obstrukčním onemocněním dýchacích cest.
Bronchospasmus vyvolaný cvičením
VENTOLIN HFA je indikován k prevenci bronchospasmu vyvolaného cvičením u pacientů ve věku 4 let a starších.
DÁVKOVÁNÍ A PODÁVÁNÍ
Bronchospasmus
Pro léčbu akutních epizod bronchospasmu nebo prevenci symptomů spojených s bronchospasmem je obvyklá dávka pro dospělé a děti 2 inhalace opakované každých 4 až 6 hodin; u některých pacientů může stačit 1 inhalace každé 4 hodiny. Častější podávání nebo větší počet inhalací se nedoporučuje.
Bronchospasmus vyvolaný cvičením
Pro prevenci bronchospasmu vyvolaného cvičením je obvyklá dávka pro dospělé a děti ve věku 4 let a starší 2 inhalace 15 až 30 minut před cvičením.
Informace o administraci
VENTOLIN HFA by měl být podáván pouze perorální inhalační cestou.
Základní nátěr
Základní nátěr VENTOLIN HFA je nezbytný pro zajištění vhodného obsahu albuterolu při každém spuštění. Před prvním použitím naplňte VENTOLIN HFA, pokud nebyl inhalátor používán déle než 2 týdny nebo když inhalátor upadl. Pro základní nátěr VENTOLIN HFA vypusťte 4 střiky do vzduchu směrem od obličeje a před každým nástřikem dobře protřepejte.
Čištění
Pro zajištění správného dávkování a zabránění ucpání otvoru aktuátoru omyjte aktuátor teplou vodou a nechte jej úplně vyschnout na vzduchu alespoň jednou týdně.
JAK DODÁVÁNO
Dávkové formy A Síly
Inhalační aerosol. Modrý plastový inhalátor s modrým řemínkem obsahující tlakovou aerosolovou nádobku s odměřenou dávkou obsahující 60 nebo 200 odměřených inhalací a vybavený počítadlem. Každé stisknutí uvolní 108 mcg albuterol sulfátu (90 mcg báze albuterolu) z náustku.
Skladování A Manipulace
VENTOLIN HFA inhalační aerosol je dodáván v následujících krabicích po 1 jako tlakový hliníkový kanystr vybavený počítadlem a dodáván s modrým plastovým ovladačem s modrým uzávěrem:
NDC 0173-0682-20 18g kanystr obsahující 200 aktivací NDC 0173-0682-21 8g kanystr obsahující 60 aktivací NDC 0173-0682-24 8g kanystr pro ústavní balení obsahující 60 aktivací
Každý inhalátor je utěsněn v sáčku z fólie chránící před vlhkostí s vysoušedlem, které je třeba po otevření sáčku zlikvidovat. Každý inhalátor je zabalen s příbalovou informací pro pacienty.
Modrý aktuátor dodávaný s VENTOLIN HFA by neměl být používán s žádnými jinými kanystry produktů a aktuátory z jiných produktů by neměly být používány s kanystrem VENTOLIN HFA.
VENTOLIN HFA má počítadlo připevněné ke kanystru. Počítadlo začíná na 204 nebo 64 a odpočítává při každém uvolnění spreje. Správné množství léku v každé aktivaci nelze zaručit poté, co počítadlo zobrazí 000, i když nádobka není zcela prázdná a bude nadále fungovat. Inhalátor by měl být zlikvidován, když počítadlo ukazuje 000 nebo 12 měsíců po vyjmutí ze sáčku z ochranné fólie proti vlhkosti, podle toho, co nastane dříve.
Uchovávejte mimo dosah dětí. Vyvarujte se vstříknutí do očí.
Obsah pod tlakem: Nepropichujte. Nepoužívejte ani neskladujte v blízkosti tepla nebo otevřeného ohně. Vystavení teplotám nad 120 °F může způsobit prasknutí. Nikdy nevhazujte kanystr do ohně nebo spalovny.
Skladujte při pokojové teplotě mezi 68°F a 77°F (20°C a 25°C); povoleny výchylky od 59°F do 86°F (15°C až 30°C) [Viz USP řízená pokojová teplota ]. Uchovávejte inhalátor náustkem dolů. Pro dosažení nejlepších výsledků by měl mít inhalátor před použitím pokojovou teplotu. PŘED KAŽDÝM STŘÍKÁNÍM DOBŘE PROTŘEPEJTE.
GlaxoSmithKline, Research Triangle Park, NC 27709. Revize: prosinec 2014
VEDLEJŠÍ EFEKTY
Použití VENTOLIN HFA může být spojeno s následujícím:
- Paradoxní bronchospasmus [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Kardiovaskulární účinky [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Okamžité reakce přecitlivělosti [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
- Hypokalémie [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ]
Zkušenosti z klinických studií
Vzhledem k tomu, že klinické studie jsou prováděny za velmi odlišných podmínek, nelze míry nežádoucích reakcí pozorované v klinických studiích léku přímo srovnávat s mírami v klinických studiích jiného léku a nemusí odrážet míry pozorované v praxi.
Údaje o bezpečnosti popsané níže odrážejí expozici VENTOLIN HFA u 248 subjektů léčených VENTOLIN HFA ve 3 placebem kontrolovaných klinických studiích trvajících 2 až 12 týdnů. Údaje od dospělých a dospívajících jsou založeny na 2 klinických studiích, ve kterých bylo 202 subjektů s astmatem ve věku 12 let a starších léčeno VENTOLIN HFA 2 inhalacemi 4krát denně po dobu 12 týdnů. Dospělá/dospívající populace byla 92 žen, 110 mužů a 163 bílých, 19 černých, 18 hispánců, 2 ostatní. Údaje od pediatrických subjektů jsou založeny na 1 klinické studii, ve které bylo 46 subjektů s astmatem ve věku 4 až 11 let léčeno VENTOLIN HFA 2 inhalacemi 4krát denně po dobu 2 týdnů. Populace byla 21 žen, 25 mužů a 25 bílých, 17 černých, 3 hispánci, 1 další.
Dospělí a dospívající ve věku 12 let a starší: Dvě 12týdenní, randomizované, dvojitě zaslepené studie u 610 dospělých a dospívajících subjektů s astmatem, které porovnávaly VENTOLIN HFA, inhalátor albuterolu s CFC 11/12 a placebo inhalátor HFA-134a. Celkově byla incidence a povaha nežádoucích účinků hlášených pro VENTOLIN HFA a inhalátor albuterolu s pohonem CFC 11/12 srovnatelná. Tabulka 1 uvádí incidenci všech nežádoucích účinků (ať už se zkoušejícím domnívají, že souvisejí nebo nesouvisejí s lékem) z těchto studií, které se vyskytovaly v míře 3 % nebo vyšší ve skupině léčené přípravkem VENTOLIN HFA a častěji ve skupině léčené s VENTOLIN HFA než ve skupině placeba HFA-134a.
Nežádoucí účinky hlášené méně než 3 % dospělých a dospívajících subjektů užívajících VENTOLIN HFA a větší částí subjektů užívajících VENTOLIN HFA než užívajících placebo inhalátor HFA-134a a které mají potenciál souviset s VENTOLIN HFA zahrnují průjem, laryngitidu, orofaryngeální edém, kašel, plicní poruchy, tachykardie a extrasystoly. U přípravku VENTOLIN HFA byly také pozorovány palpitace a závratě.
Pediatričtí jedinci ve věku 4 až 11 let: Výsledky z 2týdenní klinické studie u pediatrických pacientů s astmatem ve věku 4 až 11 let ukázaly, že tato pediatrická populace měla profil nežádoucích účinků podobný profilu dospělé a dospívající populace.
Byly provedeny tři studie s cílem vyhodnotit bezpečnost a účinnost přípravku VENTOLIN HFA u jedinců ve věku od narození do 4 let. Výsledky těchto studií neprokázaly účinnost VENTOLIN HFA v této věkové skupině [viz Použití ve specifických populacích ]. Vzhledem k tomu, že účinnost přípravku VENTOLIN HFA nebyla prokázána u dětí ve věku od narození do 48 měsíců, nelze bezpečnost přípravku VENTOLIN HFA v této věkové skupině stanovit. Bezpečnostní profil pozorovaný u pediatrické populace mladší než 4 roky byl však srovnatelný s profilem pozorovaným u starších pediatrických subjektů au dospělých a dospívajících. Tam, kde byl výskyt nežádoucích účinků vyšší u subjektů mladších než 4 roky ve srovnání se staršími subjekty, byl vyšší výskyt zaznamenán ve všech léčebných ramenech, včetně placeba. Tyto nežádoucí účinky zahrnovaly infekci horních cest dýchacích, nazofaryngitidu, pyrexii a tachykardii.
Postmarketingové zkušenosti
Kromě nežádoucích účinků hlášených z klinických studií byly během poregistračního použití albuterol sulfátu zjištěny následující nežádoucí účinky. Protože jsou tyto reakce hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo stanovit příčinnou souvislost s expozicí léku. Tyto příhody byly vybrány pro zahrnutí buď na základě jejich závažnosti, četnosti hlášení nebo kauzální souvislosti s albuterolem nebo kombinací těchto faktorů.
Po použití přípravku VENTOLIN HFA byly hlášeny případy paradoxního bronchospasmu, chrapotu, arytmií (včetně fibrilace síní, supraventrikulární tachykardie) a reakcí z přecitlivělosti (včetně kopřivky, angioedému, vyrážky).
Kromě toho může albuterol, stejně jako ostatní sympatomimetika, způsobit nežádoucí reakce, jako je hypokalémie, hypertenze, periferní vazodilatace, angina pectoris, třes, stimulace centrálního nervového systému, hyperaktivita, nespavost, bolest hlavy, svalové křeče, vysušení nebo podráždění orofaryngu a metabolické acidóza.
DROGOVÉ INTERAKCE
Jiné krátkodobě působící sympatomimetické aerosolové bronchodilatátory by neměly být užívány současně s albuterolem. Pokud mají být jakýmkoli způsobem podávány další adrenergní léky, měly by být používány s opatrností, aby se zabránilo škodlivým kardiovaskulárním účinkům.
Látky blokující beta-adrenergní receptory
Beta-blokátory nejen blokují plicní účinek beta-agonistů, jako je VENTOLIN HFA, ale mohou také vyvolat těžký bronchospasmus u pacientů s astmatem. Pacienti s astmatem by proto za normálních okolností neměli být léčeni betablokátory. Za určitých okolností však pro tyto pacienty nemusí existovat žádné přijatelné alternativy k použití beta-adrenergních blokátorů; lze zvážit kardioselektivní beta-blokátory, i když by měly být podávány s opatrností.
Diuretika nešetřící draslík
Změny EKG a/nebo hypokalémie, které mohou být důsledkem podávání draslík nešetřících diuretik (jako jsou kličková nebo thiazidová diuretika), mohou být beta-agonisty akutně zhoršeny, zvláště když je překročena doporučená dávka beta-agonistů. Ačkoli klinický význam těchto účinků není znám, doporučuje se opatrnost při současném podávání přípravku VENTOLIN HFA s diuretiky nešetřícími draslík.
Digoxin
Průměrné snížení sérových hladin digoxinu o 16 % až 22 % bylo prokázáno po jednorázovém intravenózním a perorálním podání albuterolu normálním dobrovolníkům, kteří dostávali digoxin po dobu 10 dnů. Klinický význam těchto nálezů pro pacienty s obstrukčním onemocněním dýchacích cest, kteří chronicky užívají inhalační albuterol a digoxin, není jasný. Přesto by bylo rozumné pečlivě vyhodnotit hladiny digoxinu v séru u pacientů, kteří v současné době užívají digoxin a albuterol.
Inhibitory monoaminoxidázy a tricyklická antidepresiva
VENTOLIN HFA by měl být podáván s extrémní opatrností pacientům léčeným inhibitory monoaminooxidázy nebo tricyklickými antidepresivy nebo do 2 týdnů po vysazení takových přípravků, protože účinek albuterolu na cévní systém může být zesílen.
VAROVÁNÍ
Zahrnuto jako součást OPATŘENÍ sekce.
OPATŘENÍ
Paradoxní bronchospasmus
VENTOLIN HFA může vyvolat paradoxní bronchospasmus, který může být život ohrožující. Pokud se po podání přípravku VENTOLIN HFA objeví paradoxní bronchospasmus, je třeba jej okamžitě přerušit a zahájit alternativní léčbu. Je třeba si uvědomit, že paradoxní bronchospasmus, pokud je spojen s inhalačními přípravky, se často vyskytuje při prvním použití nové nádobky.
Zhoršení astmatu
Astma se může zhoršit akutně po dobu několika hodin nebo chronicky po několik dní nebo déle. Pokud pacient potřebuje více dávek přípravku VENTOLIN HFA než obvykle, může to být marker destabilizace astmatu a vyžaduje přehodnocení pacienta a léčebného režimu se zvláštním ohledem na možnou potřebu protizánětlivé léčby, např. kortikosteroidy.
Použití protizánětlivých činidel
Použití samotných bronchodilatátorů s beta-adrenergními agonisty nemusí u mnoha pacientů stačit ke kontrole astmatu. Je třeba včas zvážit přidání protizánětlivých látek, např. kortikosteroidů, do terapeutického režimu.
Kardiovaskulární účinky
VENTOLIN HFA, stejně jako všichni ostatní beta2-adrenergní agonisté, může u některých pacientů vyvolat klinicky významné kardiovaskulární účinky, jako jsou změny tepové frekvence nebo krevního tlaku. Pokud se takové účinky objeví, může být nutné léčbu přípravkem VENTOLIN HFA přerušit. Kromě toho bylo hlášeno, že beta-agonisté způsobují změny na elektrokardiogramu (EKG), jako je zploštění vlny T, prodloužení intervalu QTc a deprese segmentu ST. Klinický význam těchto nálezů není znám. Proto by měl být VENTOLIN HFA, stejně jako všechny ostatní sympatomimetické aminy, používán s opatrností u pacientů se základními kardiovaskulárními poruchami, zejména s koronární insuficiencí, srdečními arytmiemi a hypertenzí.
Nepřekračujte doporučenou dávku
souvislosti s nadměrným užíváním inhalačních sympatomimetik u pacientů s astmatem byly hlášeny případy úmrtí. Přesná příčina smrti není známa, ale existuje podezření na zástavu srdce po neočekávaném rozvoji těžké akutní astmatické krize a následné hypoxii.
Okamžité hypersenzitivní reakce
Po podání přípravku VENTOLIN HFA se mohou objevit okamžité hypersenzitivní reakce (např. kopřivka, angioedém, vyrážka, bronchospasmus, hypotenze), včetně anafylaxe (viz KONTRAINDIKACE ].
Koexistující podmínky
VENTOLIN HFA, stejně jako jiné sympatomimetické aminy, by měl být používán s opatrností u pacientů s křečovými poruchami, hypertyreózou nebo diabetes mellitus a u pacientů, kteří neobvykle reagují na sympatomimetické aminy. Bylo hlášeno, že velké dávky intravenózního albuterolu zhoršují již existující diabetes mellitus a ketoacidózu.
Hypokalémie
Léky s beta-adrenergními agonisty mohou u některých pacientů vyvolat významnou hypokalémii, pravděpodobně prostřednictvím intracelulárního zkratu, který má potenciál vyvolat nežádoucí kardiovaskulární účinky (viz KLINICKÁ FARMAKOLOGIE ]. Pokles sérového draslíku je obvykle přechodný a nevyžaduje suplementaci.
Informace pro pacienty
Doporučte pacientovi, aby si přečetl označení pacienta schválené FDA ( INFORMACE PRO PACIENTA a návod k použití ).
Frekvence používání
Informujte pacienty, že účinek přípravku VENTOLIN HFA by měl trvat až 4 až 6 hodin. Nepoužívejte VENTOLIN HFA častěji, než je doporučeno. Poučte pacienty, aby nezvyšovali dávku nebo frekvenci dávek přípravku VENTOLIN HFA bez porady s lékařem. Poučte pacienty, aby okamžitě vyhledali lékařskou pomoc, pokud se léčba přípravkem VENTOLIN HFA stane méně účinná pro úlevu od symptomů, příznaky se zhorší a/nebo potřebují přípravek používat častěji než obvykle.
Základní nátěr
Poučte pacienty, aby před prvním použitím VENTOLIN HFA naplnili, pokud inhalátor nebyl používán déle než 2 týdny nebo když inhalátor upadl. Pro základní nátěr VENTOLIN HFA vypusťte 4 střiky do vzduchu směrem od obličeje a před každým nástřikem dobře protřepejte.
Čištění
Aby bylo zajištěno správné dávkování a aby se zabránilo ucpání otvoru aktuátoru, poučte pacienty, aby omyli aktuátor teplou vodou a nechali jej úplně vyschnout na vzduchu alespoň jednou týdně. Informujte pacienty, že podrobné pokyny k čištění jsou uvedeny v příbalové informaci pro pacienty.
Paradoxní bronchospasmus
Informujte pacienty, že VENTOLIN HFA může vyvolat paradoxní bronchospasmus. Poučte je, aby v případě výskytu paradoxního bronchospasmu vysadili VENTOLIN HFA.
Současné užívání drog
Informujte pacienty, že zatímco užívají VENTOLIN HFA, ostatní inhalační léky a léky na astma by měli užívat pouze podle pokynů lékaře.
Časté nežádoucí účinky
Mezi běžné nežádoucí účinky léčby inhalačním albuterolem patří palpitace, bolest na hrudi, zrychlený srdeční tep, třes a nervozita.
Těhotenství
Doporučte pacientkám, které jsou těhotné nebo kojící, aby kontaktovaly svého lékaře ohledně užívání přípravku VENTOLIN HFA.
VENTOLIN je registrovaná ochranná známka skupiny společností GSK. Ostatní uvedené značky jsou ochrannými známkami příslušných vlastníků a nejsou ochrannými známkami skupiny společností GSK. Tvůrci těchto značek nejsou přidruženi a nepodporují skupinu společností GSK ani její produkty.
Neklinická toxikologie
Karcinogeneze, mutageneze, zhoršení plodnosti
Ve dvouleté studii na potkanech Sprague-Dawley způsobil albuterol sulfát v závislosti na dávce zvýšení výskytu benigních leiomyomů mezovaria při dietních dávkách 2,0 mg/kg a vyšších (přibližně 14 a 6násobek MRHDID u dospělých a děti na základě mg/m). V jiné studii byl tento účinek blokován současným podáváním propranololu, neselektivního betaadrenergního antagonisty. V 18měsíční studii na myších CD-1 neukázal albuterol sulfát žádný důkaz tumorigenicity při dietních dávkách až 500 mg/kg (přibližně 1 700krát a 800krát vyšší než MRHDID pro dospělé a děti, v přepočtu na mg/m² ). Ve 22měsíční studii u křečků zlatých nevykázal albuterol sulfát žádné známky tumorigenicity při dietních dávkách až 50 mg/kg (přibližně 225 a 110násobek MRHDID pro dospělé a děti, v přepočtu na mg/m²).
Albuterol sulfát nebyl mutagenní v Amesově testu ani v mutačním testu na kvasinkách. Albuterol sulfát nebyl klastogenní v testu na lidských periferních lymfocytech nebo v testu na mikronukleu myší kmene AH1.
Reprodukční studie na potkanech neprokázaly žádné známky poškození plodnosti při perorálních dávkách albuterol sulfátu až do 50 mg/kg (přibližně 340násobek MRHDID pro dospělé na základě mg/m).
Použití u konkrétních populací
Těhotenství
Teratogenní účinky
Kategorie těhotenství C. Neexistují žádné adekvátní a dobře kontrolované studie s VENTOLIN HFA nebo albuterol sulfátem u těhotných žen. Během celosvětové marketingové zkušenosti byly u potomků pacientů léčených albuterolem hlášeny různé vrozené anomálie, včetně rozštěpu patra a defektů končetin. Některé z matek během těhotenství užívaly více léků. Nelze rozpoznat žádný konzistentní vzor defektů a vztah mezi užíváním albuterolu a vrozenými anomáliemi nebyl stanoven. Reprodukční studie na zvířatech u myší a králíků odhalily důkazy teratogenity. VENTOLIN HFA by měl být používán během těhotenství pouze tehdy, pokud potenciální přínos ospravedlňuje potenciální riziko pro plod. Ženám by mělo být doporučeno, aby kontaktovaly svého lékaře, pokud otěhotní během užívání přípravku VENTOLIN HFA.
reprodukční studii na myších vyvolal subkutánně podaný albuterol sulfát tvorbu rozštěpu patra u 5 ze 111 (4,5 %) plodů při expozicích nižších, než je maximální doporučená denní inhalační dávka u lidí (MRHDID) pro dospělé na bázi mg/m² a u 10 ze 108 (9,3 %) plodů na přibližně 8násobku MRHDID. Podobné účinky nebyly pozorovány u přibližně jedné jedenáctiny MRHDID. Rozštěp patra se také vyskytl u 22 ze 72 (30,5 %) plodů od žen léčených subkutánně isoproterenolem (pozitivní kontrola).
V reprodukční studii králíků vyvolal orálně podávaný albuterol sulfát kranioschízu u 7 z 19 plodů (37 %) při přibližně 680násobku MRHDID.
V jiné studii na králících přípravek albuterol sulfát/HFA-134a podávaný inhalací způsobil zvětšení přední části fetálních fontanel přibližně na jednu třetinu MRHDID.
Neteratogenní účinky
Studie, ve které byl březím krysám podáván radioaktivně značený albuterol sulfát, prokázala, že materiál související s léčivem se přenáší z mateřského oběhu na plod.
Práce a dodání
Neexistují žádné dobře kontrolované studie na lidech, které by zkoumaly účinky VENTOLIN HFA na předčasný porod nebo porod v termínu. Vzhledem k možné interferenci beta-agonistů s kontraktilitou dělohy by mělo být použití přípravku VENTOLIN HFA během porodu omezeno na pacientky, u kterých přínosy jasně převažují nad riziky.
Kojící matky
Plazmatické hladiny albuterol sulfátu a HFA-134a po inhalačních terapeutických dávkách jsou u lidí velmi nízké, ale není známo, zda se složky přípravku VENTOLIN HFA vylučují do lidského mléka. Vzhledem k možnosti tumorigenicity prokázané u albuterolu ve studiích na zvířatech a nedostatku zkušeností s používáním přípravku VENTOLIN HFA kojícími matkami by se mělo rozhodnout, zda přerušit kojení nebo přerušit léčbu, přičemž je třeba vzít v úvahu důležitost léčiva matka. Při podávání přípravku VENTOLIN HFA kojící ženě je třeba postupovat opatrně.
Pediatrické použití
Bezpečnost a účinnost přípravku VENTOLIN HFA u dětí ve věku 4 let a starších byla stanovena na základě dvou 12týdenních klinických studií u subjektů ve věku 12 let a starších s astmatem a jedné dvoutýdenní klinické studie u subjektů ve věku 4 až 11 let s astmatem [vidět NEŽÁDOUCÍ REAKCE , Klinické studie ]. Bezpečnost a účinnost přípravku VENTOLIN HFA u dětí mladších 4 let nebyla stanovena. Byly provedeny tři studie k vyhodnocení bezpečnosti a účinnosti přípravku VENTOLIN HFA u subjektů mladších 4 let a zjištění jsou popsána níže.
Dvě 4týdenní randomizované, dvojitě zaslepené, placebem kontrolované studie byly provedeny u 163 pediatrických pacientů ve věku od narození do 48 měsíců s příznaky bronchospasmu spojeného s obstrukčním onemocněním dýchacích cest (příznaky zahrnovaly: sípání, kašel, dušnost nebo tlak na hrudi). . VENTOLIN HFA nebo placebo HFA byly podávány buď s ventilovou zádržnou komorou AeroChamber Plus® nebo s ventilovou zádržnou komorou Optichamber® s maskou 3krát denně. V jedné studii byly dětem ve věku 24 až 48 měsíců podávány VENTOLIN HFA 90 mcg (n = 26), VENTOLIN HFA 180 mcg (n = 25) a placebo HFA (n = 26). Ve druhé studii byly dětem ve věku od narození do 24 měsíců podávány VENTOLIN HFA 90 mcg (n = 29), VENTOLIN HFA 180 mcg (n = 29) a placebo HFA (n = 28). Během 4týdenního léčebného období nebyly v žádné studii žádné rozdíly v léčbě ve skóre příznaků astmatu mezi skupinami, které dostávaly VENTOLIN HFA 90 mcg, VENTOLIN HFA 180 mcg a placebo.
Ve třetí studii byl VENTOLIN HFA hodnocen u 87 pediatrických pacientů mladších 24 měsíců pro léčbu akutního pískotu. VENTOLIN HFA byl v tomto testu dodán s ventilovou přidržovací komorou AeroChamber Plus. Mezi VENTOLIN HFA 180 mcg a VENTOLIN HFA 360 mcg nebyly žádné signifikantní rozdíly ve skóre příznaků astmatu a průměrné změně oproti výchozí hodnotě.
Byly provedeny studie charakterizace dávek in vitro, aby se vyhodnotila dodávka VENTOLIN HFA prostřednictvím zádržných komor s připojenými maskami. Studie byly provedeny se 2 různými zadržovacími komorami s maskami (malé a střední velikosti). Údaje ze studie in vitro při simulaci dýchání pacienta naznačují, že dávka přípravku VENTOLIN HFA předložená k inhalaci přes zádržnou komoru s ventilem a maskou bude srovnatelná s dávkou podávanou dospělým bez spaceru a masky na kilogram tělesné hmotnosti (tabulka 2). Výše popsané klinické studie u dětí mladších 4 let však naznačují, že buď nebyla v této věkové skupině definována optimální dávka přípravku VENTOLIN HFA, nebo v této věkové skupině není přípravek VENTOLIN HFA účinný. Bezpečnost a účinnost přípravku VENTOLIN HFA podávaného s distančním zařízením nebo bez něj u dětí mladších 4 let nebyla prokázána.
Geriatrické použití
Klinické studie přípravku VENTOLIN HFA nezahrnovaly dostatečný počet subjektů ve věku 65 let a starších, aby bylo možné určit, zda starší subjekty reagují odlišně než mladší subjekty. Jiné hlášené klinické zkušenosti nezjistily rozdíly v odpovědích mezi staršími a mladšími pacienty. Obecně by měl být výběr dávky pro staršího pacienta opatrný, obvykle začínající na spodní hranici dávkovacího rozmezí, což odráží vyšší frekvenci snížené funkce jater, ledvin nebo srdce a souběžného onemocnění nebo jiné lékové terapie.
PŘEDÁVKOVAT
Očekávané známky a příznaky předávkování albuterolem jsou příznaky nadměrné beta-adrenergní stimulace a/nebo výskyt nebo zvýraznění jakýchkoli známek a příznaků beta-adrenergní stimulace (např. záchvaty, angina pectoris, hypertenze nebo hypotenze, tachykardie se zvýšenými frekvencemi do 200 tepů/min, arytmie, nervozita, bolest hlavy, třes, svalové křeče, sucho v ústech, bušení srdce, nevolnost, závratě, únava, malátnost, nespavost, hyperglykémie, hypokalémie, metabolická acidóza).
Stejně jako u všech inhalačních sympatomimetik může být předávkování inhalačním aerosolem VENTOLIN HFA spojeno se zástavou srdce a dokonce i se smrtí.
Léčba spočívá ve vysazení VENTOLIN HFA spolu s vhodnou symptomatickou terapií. Je možné zvážit uvážlivé použití kardioselektivního blokátoru beta-receptorů, přičemž je třeba mít na paměti, že taková léčba může vyvolat bronchospasmus. Neexistují dostatečné důkazy ke stanovení, zda je dialýza prospěšná při předávkování přípravkem VENTOLIN HFA.
KONTRAINDIKACE
VENTOLIN HFA je kontraindikován u pacientů s anamnézou přecitlivělosti na kteroukoli složku (viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ , POPIS ].
KLINICKÁ FARMAKOLOGIE
Mechanismus působení
Studie in vitro a farmakologické studie in vivo prokázaly, že albuterol má ve srovnání s isoproterenolem přednostní účinek na beta2-adrenergní receptory. Ačkoli beta2-adrenoceptory jsou převládajícími adrenergními receptory v hladkém svalstvu průdušek a beta1-adrenoceptory jsou převládajícími receptory v srdci, existují také beta2-adrenoceptory v lidském srdci, které tvoří 10 % až 50 % celkových beta-adrenoceptorů. Přesná funkce těchto receptorů nebyla stanovena, ale jejich přítomnost zvyšuje možnost, že i selektivní beta2-agonisté mohou mít účinky na srdce.

Aktivace beta2-adrenergních receptorů na hladkém svalstvu dýchacích cest vede k aktivaci adenylcyklázy a ke zvýšení intracelulární koncentrace cyklického-3',5'-adenosinmonofosfátu (cyklický AMP). Toto zvýšení cyklického AMP vede k aktivaci proteinkinázy A, která inhibuje fosforylaci myosinu a snižuje intracelulární koncentrace iontového vápníku, což vede k relaxaci. Albuterol uvolňuje hladké svaly všech dýchacích cest, od průdušnice až po terminální bronchioly. Albuterol působí jako funkční antagonista k uvolnění dýchacích cest bez ohledu na obsažený spasmogen, čímž chrání před všemi bronchokonstrikčními výzvami. Zvýšené koncentrace cyklického AMP jsou také spojeny s inhibicí uvolňování mediátorů z žírných buněk v dýchacích cestách.
Ve většině kontrolovaných klinických studií bylo prokázáno, že albuterol má větší účinek na dýchací cesty ve formě relaxace hladkého svalstva průdušek než isoproterenol ve srovnatelných dávkách, přičemž má méně kardiovaskulárních účinků. Kontrolované klinické studie a další klinické zkušenosti ukázaly, že inhalovaný albuterol, stejně jako jiné léky s beta-adrenergními agonisty, může u některých pacientů vyvolat významný kardiovaskulární účinek, měřeno tepovou frekvencí, krevním tlakem, symptomy a/nebo elektrokardiografickými změnami [viz VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ ].
Farmakokinetika
Systémové hladiny albuterolu jsou po inhalaci doporučených dávek nízké. Studie provedená na 12 zdravých mužských a ženských subjektech s použitím vyšší dávky (1 080 mcg báze albuterolu) ukázala, že průměrné maximální plazmatické koncentrace přibližně 3 ng/ml se objevily po dávkování, když byl albuterol podáván s použitím hnací látky HFA-134a. Průměrná doba dosažení maximálních koncentrací (Tmax) byla zpožděna po podání přípravku VENTOLIN HFA (Tmax= 0,42 hodiny) ve srovnání s inhalátorem albuterolu poháněným CFC (Tmax= 0,17 hodiny). Zdánlivý terminální plazmatický poločas albuterolu je přibližně 4,6 hodiny. Žádné další farmakokinetické studie pro VENTOLIN HFA nebyly provedeny u novorozenců, dětí nebo starších subjektů.
Toxikologie zvířat a/nebo farmakologie
Preklinický
Intravenózní studie na potkanech s albuterol sulfátem prokázaly, že albuterol prochází hematoencefalickou bariérou a dosahuje koncentrace v mozku dosahující přibližně 5,0 % plazmatických koncentrací. Ve strukturách mimo hematoencefalickou bariéru (šišinka a hypofýza) byly zjištěny koncentrace albuterolu 100krát vyšší než v celém mozku.
Studie na laboratorních zvířatech (miniprasata, hlodavci a psi) prokázaly výskyt srdečních arytmií a náhlé smrti (s histologickým důkazem nekrózy myokardu), pokud jsou beta-agonisté a methylxantiny podávány současně. Klinický význam těchto nálezů není znám.
Pohonná látka HFA-134a
zvířat a lidí bylo zjištěno, že hnací látka HFA-134a je rychle absorbována a rychle eliminována, s poločasem eliminace 3 až 27 minut u zvířat a 5 až 7 minut u lidí. Doba do dosažení maximální plazmatické koncentrace (Tmax) a střední doba zdržení jsou extrémně krátké, což vede k přechodnému výskytu HFA-134a v krvi bez známek akumulace.
Hnací látka HFA-134a postrádá farmakologickou aktivitu, s výjimkou velmi vysokých dávek u zvířat (tj. 380 až 1 300násobek maximální expozice u člověka na základě srovnání hodnot plochy pod křivkou plazmatické koncentrace proti času [AUC]), primárně způsobuje ataxii, třes dušnost nebo slinění. Tyto jevy jsou podobné účinkům, které vyvolávají strukturálně příbuzné CFC, které byly široce používány v inhalátorech s odměřenými dávkami.
Klinické studie
Bronchospasmus spojený s astmatem
Dospělí a dospívající subjekty ve věku 12 let a starší
Účinnost přípravku VENTOLIN HFA byla hodnocena ve dvou 12týdenních, randomizovaných, dvojitě zaslepených, placebem kontrolovaných studiích u subjektů ve věku 12 let a starších s mírným až středně těžkým astmatem. Tyto studie zahrnovaly celkem 610 subjektů (323 mužů, 287 žen). V každé studii subjekty dostávaly 2 inhalace VENTOLIN HFA, CFC 11/12-poháněný albuterol nebo HFA-134a placebo 4krát denně po dobu 12 týdnů. Subjekty užívající placebo inhalátor HFA-134a také užívaly VENTOLIN HFA pro zmírnění příznaků astmatu podle potřeby. Někteří jedinci, kteří se účastnili těchto klinických studií, užívali souběžnou léčbu inhalačními steroidy. Účinnost byla hodnocena sériovým usilovným výdechovým objemem za 1 sekundu (FEV). V každé z těchto studií vedly 2 inhalace VENTOLIN HFA k významně většímu zlepšení FEV1 oproti hodnotě před léčbou než placebo. Výsledky ze 2 klinických studií jsou popsány níže.
Ve 12týdenní, randomizované, dvojitě zaslepené studii byl VENTOLIN HFA (101 subjektů) srovnáván s albuterolem s pohonem CFC 11/12 (99 subjektů) a placebo inhalátorem HFA-134a (97 subjektů) u dospívajících a dospělých ve věku 12 až 76 let s mírným až středně těžkým astmatem. Sériová měření FEV1 [uvedena níže jako procentuální změna od výchozí hodnoty testovacího dne v den 1 (n = 297) a v týdnu 12 (n = 249)] prokázala, že 2 inhalace VENTOLIN HFA přinesly významně větší zlepšení FEV1 oproti hodnotě před léčbou placebo.
FEV1 jako procentuální změna oproti stavu před podáním dávky ve velké, 12týdenní klinické studii, den 1 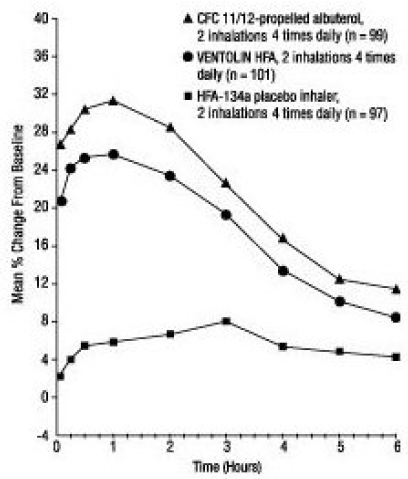
12. týden 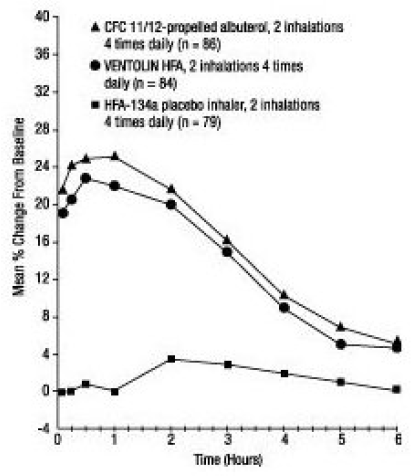
populaci respondérů (větší nebo rovné 15% zvýšení FEV1 během 30 minut po dávce) léčené přípravkem VENTOLIN HFA byla průměrná doba do nástupu 15% zvýšení FEV1 oproti hodnotě před léčbou 5,4 minuty a průměrná doba do maximální účinek byl 56 minut. Průměrná doba trvání účinku měřená 15% zvýšením FEV1 oproti hodnotě před léčbou byla přibližně 4 hodiny. U některých subjektů byla doba trvání účinku až 6 hodin.
Druhá 12týdenní randomizovaná, dvojitě zaslepená studie byla provedena za účelem vyhodnocení účinnosti a bezpečnosti přechodu subjektů z albuterolu s CFC 11/12 na VENTOLIN HFA. Během 3týdenní zaváděcí fáze studie dostávali všichni jedinci albuterol s pohonem CFC 11/12. Během dvojitě zaslepené léčebné fáze byl VENTOLIN HFA (91 subjektů) srovnáván s albuterolem poháněným CFC 11/12 (100 subjektů) a inhalátorem placeba HFA-134a (95 subjektů) u dospělých a dospívajících subjektů s mírným až středně těžkým astmatem. Sériová měření FEV1 prokázala, že 2 inhalace VENTOLIN HFA vyvolaly významně větší zlepšení funkce plic než placebo. Přechod z inhalátoru albuterolu s pohonem CFC 11/12 na VENTOLIN HFA neodhalil žádné klinicky významné změny v profilu účinnosti.
Ve 2 studiích pro dospělé byly výsledky účinnosti přípravku VENTOLIN HFA významně vyšší než u placeba a byly klinicky srovnatelné s výsledky dosaženými s albuterolem s pohonem CFC 11/12, ačkoli byly pozorovány malé číselné rozdíly v průměrné odpovědi FEV a dalších měřeních. Lékaři by si měli uvědomit, že individuální odpovědi na beta-adrenergní agonisty podávané prostřednictvím různých hnacích látek se mohou lišit a že ekvivalentní odpovědi u jednotlivých pacientů nelze předpokládat.
Pediatričtí jedinci ve věku 4 až 11 let
Účinnost přípravku VENTOLIN HFA byla hodnocena v jedné 2týdenní, randomizované, dvojitě zaslepené, placebem kontrolované studii u 135 pediatrických pacientů ve věku 4 až 11 let s mírným až středně těžkým astmatem. V této studii subjekty dostávaly VENTOLIN HFA, CFC 11/12 poháněný albuterol nebo HFA-134a placebo. Sériová měření plicních funkcí prokázala, že 2 inhalace VENTOLIN HFA vyvolaly významně větší zlepšení plicní funkce než placebo a že nebyly žádné významné rozdíly mezi skupinami léčenými VENTOLIN HFA a salbuterolem s CFC 11/12. V populaci respondérů léčených přípravkem VENTOLIN HFA byla průměrná doba do nástupu 15% zvýšení maximální rychlosti výdechového průtoku (PEFR) oproti hodnotě před léčbou 7,8 minuty a průměrná doba do dosažení maximálního účinku byla přibližně 90 minut. Průměrná doba trvání účinku měřená 15% zvýšením PEFR oproti hodnotě před léčbou byla delší než 3 hodiny. U některých subjektů byla doba trvání účinku až 6 hodin.
Bronchospasmus vyvolaný cvičením
Jedna kontrolovaná klinická studie u dospělých subjektů s astmatem (N = 24) prokázala, že 2 inhalace VENTOLIN HFA podané přibližně 30 minut před cvičením významně zabránily bronchospasmu vyvolanému cvičením (měřeno maximálním procentem poklesu FEV1 po cvičení) ve srovnání s HFA-134a. placebo inhalátor. Navíc bylo prokázáno, že VENTOLIN HFA je pro tuto indikaci klinicky srovnatelný s inhalátorem albuterolu s pohonem CFC 11/12.
INFORMACE PRO PACIENTA
VENTOLIN® [vent' o-lin] HFA (albuterol sulfát) Inhalační aerosol
Přečtěte si informace pro pacienty, které jsou součástí inhalačního aerosolu VENTOLIN HFA, než jej začnete používat, a pokaždé, když dostanete náplň. Mohou se objevit nové informace. Tyto informace pro pacienta nenahrazují rozhovor s vaším poskytovatelem zdravotní péče o vašem zdravotním stavu nebo léčbě.
Co je VENTOLIN HFA?
VENTOLIN HFA je inhalační lék na předpis používaný u lidí ve věku 4 let a starších k:
- k léčbě nebo prevenci bronchospasmu u lidí, kteří mají reverzibilní obstrukční onemocnění dýchacích cest
- zabránit bronchospasmu vyvolanému cvičením
Není známo, zda je VENTOLIN HFA bezpečný a účinný u dětí mladších 4 let.
Kdo by neměl užívat VENTOLIN HFA?
Nepoužívejte VENTOLIN HFA jestliže jste alergický(á) na albuterol sulfát nebo na kteroukoli složku přípravku VENTOLIN HFA. Viz "Jaké jsou složky ve VENTOLIN HFA?" níže pro úplný seznam ingrediencí.
Co mám sdělit svému poskytovateli zdravotní péče před použitím VENTOLIN HFA?
Informujte svého poskytovatele zdravotní péče o všech svých zdravotních stavech, včetně toho, zda:
- mít problémy se srdcem.
- mají vysoký krevní tlak.
- mít záchvaty.
- mít problémy se štítnou žlázou.
- mít cukrovku.
- máte nízké hladiny draslíku v krvi.
- jste alergický(á) na kteroukoli složku přípravku VENTOLIN HFA nebo na jiné léky. Viz "Jaké jsou složky ve VENTOLIN HFA?" níže pro úplný seznam ingrediencí.
- mít jiné zdravotní potíže.
- jste těhotná nebo těhotenství plánujete. Není známo, zda VENTOLIN HFA může poškodit vaše nenarozené dítě.
- kojí. Není známo, zda léčivý přípravek v přípravku VENTOLIN HFA přechází do vašeho mléka a zda může poškodit vaše dítě.
Informujte svého poskytovatele zdravotní péče o všech lécích, které užíváte, včetně léků na předpis a volně prodejných léků, vitamínů a bylinných doplňků. VENTOLIN HFA a některé další léky se mohou vzájemně ovlivňovat. To může způsobit závažné nežádoucí účinky.
Zejména informujte svého poskytovatele zdravotní péče, pokud užíváte:
- jiné inhalační léky nebo léky na astma
- beta-blokátory
- diuretika
- digoxin
- inhibitory monoaminooxidázy
- tricyklická antidepresiva
Pokud si nejste jisti, požádejte svého poskytovatele zdravotní péče nebo lékárníka o seznam těchto léků.
Znát léky, které užíváte. Uchovávejte si jejich seznam, abyste je mohli ukázat svému poskytovateli zdravotní péče a lékárníkovi, když dostanete nový lék.
Jak mám používat VENTOLIN HFA?
Přečtěte si podrobné pokyny pro použití přípravku VENTOLIN HFA na konci této informace pro pacienta.
- Ne používejte VENTOLIN HFA, pokud vás váš poskytovatel zdravotní péče nenaučil, jak inhalátor používat, a nerozumíte tomu, jak jej správně používat.
- Děti by měly užívat VENTOLIN HFA s pomocí dospělé osoby podle pokynů poskytovatele zdravotní péče o dítě.
- Používejte VENTOLIN HFA přesně tak, jak vám řekl váš poskytovatel zdravotní péče. Nepoužívejte VENTOLIN HFA častěji, než je předepsáno.
- Ne zvyšte svou dávku nebo si vezměte další dávky přípravku VENTOLIN HFA, aniž byste se nejprve poradili se svým poskytovatelem zdravotní péče.
- Každá dávka přípravku VENTOLIN HFA by měla trvat až 4 hodiny až 6 hodin.
- Okamžitě vyhledejte lékařskou pomoc, pokud VENTOLIN HFA již nepomáhá na vaše příznaky.
- Okamžitě vyhledejte lékařskou pomoc, pokud se vaše příznaky zhorší nebo pokud potřebujete inhalátor používat častěji.
- Pokud používáte VENTOLIN HFA, používejte jiné inhalační léky a léky na astma pouze podle pokynů svého poskytovatele zdravotní péče.
- Zavolejte svého poskytovatele zdravotní péče, pokud se vaše příznaky astmatu, jako je sípání a potíže s dýcháním, zhorší během několika hodin nebo dnů. Váš poskytovatel zdravotní péče vám možná bude muset podat jiný lék k léčbě vašich příznaků.
Jaké jsou možné vedlejší účinky přípravku VENTOLIN HFA?
VENTOLIN HFA může způsobit závažné nežádoucí účinky, včetně:
- zhoršení potíží s dýcháním, kašel a sípání (paradoxní bronchospasmus). Pokud k tomu dojde, přestaňte VENTOLIN HFA používat a zavolejte svého poskytovatele zdravotní péče nebo okamžitě vyhledejte pohotovostní pomoc. Paradoxní bronchospasmus je pravděpodobnější při prvním použití nového kanystru s lékem.
- srdeční problémy, včetně rychlejší srdeční frekvence a vyššího krevního tlaku
- možná smrt u lidí s astmatem, kteří užívají příliš mnoho VENTOLIN HFA
- závažné alergické reakce. Zavolejte svého poskytovatele zdravotní péče nebo vyhledejte pohotovostní lékařskou péči, pokud se u Vás objeví některý z následujících příznaků závažné alergické reakce:
- vyrážka
- kopřivka
- otok obličeje, úst a jazyka
- dýchací problémy
- změny laboratorních hladin v krvi (cukr, draslík)
Mezi běžné vedlejší účinky přípravku VENTOLIN HFA patří:
- bolest krku
- infekce horních cest dýchacích, včetně virové infekce
- kašel
- bolest svalů
- máte pocit, že vám srdce buší nebo se ohání (bušení srdce)
- bolest na hrudi
- rychlý srdeční tep
- chvění
- nervozita
- závrať
Informujte svého poskytovatele zdravotní péče o jakémkoli nežádoucím účinku, který vás obtěžuje nebo který nezmizí.
To nejsou všechny vedlejší účinky přípravku VENTOLIN HFA. Požádejte svého poskytovatele zdravotní péče nebo lékárníka o další informace.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
Jak mám VENTOLIN HFA uchovávat?
- Skladujte VENTOLIN HFA při pokojové teplotě mezi 68 °F a 77 °F (20 °C a 25 °C) s náustkem dolů.
- Obsah vašeho VENTOLIN HFA je pod tlakem: Nepropichujte. Nepoužívejte ani neskladujte v blízkosti tepla nebo otevřeného ohně. Teploty nad 120 °F mohou způsobit prasknutí kanystru.
- Nevhazujte do ohně ani do spalovny.
- Skladujte VENTOLIN HFA v neotevřeném fóliovém sáčku a otevřete jej, až když je připraven k použití.
- Uchovávejte VENTOLIN HFA a všechny léky mimo dosah dětí.
Obecné informace o bezpečném a účinném používání přípravku VENTOLIN HFA
Léky jsou někdy předepisovány pro účely, které nejsou uvedeny v příbalové informaci pro pacienty. Nepoužívejte VENTOLIN HFA na stav, pro který nebyl předepsán. Nedávejte svůj VENTOLIN HFA jiným lidem, i když mají stejný stav jako vy. Může jim to ublížit.
Tento leták s informacemi pro pacienty shrnuje nejdůležitější informace o přípravku VENTOLIN HFA. Pokud byste chtěli další informace, promluvte si se svým poskytovatelem zdravotní péče nebo lékárníkem. Můžete požádat svého poskytovatele zdravotní péče nebo lékárníka o informace o přípravku VENTOLIN HFA, který byl napsán pro zdravotnické pracovníky.
Pro více informací o VENTOLIN HFA volejte 1-888-825-5249 nebo navštivte naši webovou stránku www.ventolin.com.
Jaké složky obsahuje VENTOLIN HFA?
Aktivní složka: albuterol sulfát
Neaktivní složka: hnací plyn HFA-134a
Návod k použití
Pouze pro orální inhalaci
Váš inhalátor VENTOLIN HFA
- Kovová nádobka obsahuje lék. Vidět Obrázek A.
Obrázek A 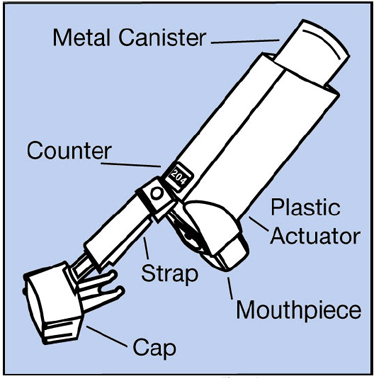
- Kanystr má počítadlo, které ukazuje, kolik sprejů léku vám zbývá. Číslo se zobrazuje přes okénko v zadní části pohonu. Viz obrázek B.
Obrázek B 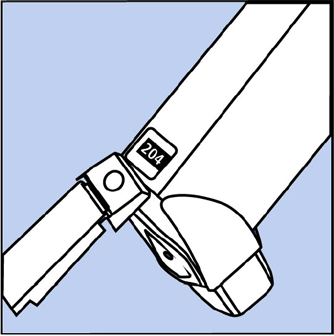
- Počítadlo začíná na obou 204 nebo 064 závislosti na velikosti inhalátoru. Číslo se bude odpočítávat o 1 při každém stříknutí inhalátoru. Počítadlo přestane počítat na 000.
- Nepokoušejte se měnit čísla ani sundávat počítadlo z kovového kanystru. Počítadlo nelze resetovat a je trvale připojeno ke kanystru.
- Modrý plastový ovladač stříká lék z nádobky. Pohon má ochranný kryt, který zakrývá náustek. Vidět Obrázek A . Když nádobku nepoužíváte, ponechejte na náustku ochranné víčko. Pásek drží víčko připevněné k pohonu.
- Ne používejte aktuátor s nádobkou s lékem z jakéhokoli jiného inhalátoru.
- Ne použijte kanystr VENTOLIN HFA s aktuátorem z jakéhokoli jiného inhalátoru.
Před použitím inhalátoru VENTOLIN HFA
- Vyjměte VENTOLIN HFA z fóliového sáčku těsně před prvním použitím. Bezpečně vyhoďte sáček a sušící balíček, který je uvnitř sáčku.
- Inhalátor by měl mít před použitím pokojovou teplotu.
- Pokud vaše dítě potřebuje používat VENTOLIN HFA, pečlivě ho sledujte, abyste se ujistili, že vaše dítě používá inhalátor správně. Váš poskytovatel zdravotní péče vám ukáže, jak má vaše dítě používat VENTOLIN HFA.
Naplňte svůj inhalátor VENTOLIN HFA
- Před prvním použitím VENTOLIN HFA musíte inhalátor naplnit, abyste při jeho použití dostali správné množství léku.
- Chcete-li inhalátor naplnit, sejměte uzávěr z náustku a dobře inhalátorem protřepejte. Poté 1krát vystříkněte inhalátor do vzduchu směrem od vašeho obličeje. Viz obrázek C. Zabraňte vstříknutí do očí.
Obrázek C 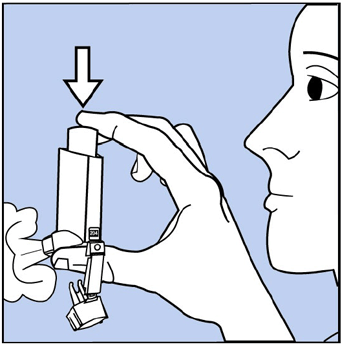
- Inhalátor takto protřepejte a nastříkejte ještě 3x, aby se dokončilo jeho naplnění. Počítadlo by nyní mělo číst 200 nebo 60 v závislosti na velikosti inhalátoru. Viz obrázek D.
Obrázek D 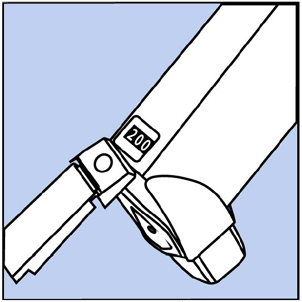
- Pokud jste inhalátor nepoužili déle než 14 dní nebo pokud jej upustíte, musíte svůj inhalátor znovu naplnit. Sundejte uzávěr z náustku a zatřeste a vystříkněte inhalátor 4krát do vzduchu směrem od vašeho obličeje.
Jak používat inhalátor VENTOLIN HFA
Při každém použití VENTOLIN HFA postupujte podle těchto kroků.
Krok 1. Ujistěte se, že nádobka pevně sedí v pohonu. Počítadlo by mělo ukazovat okénkem v aktuátoru.
Dobře protřepejte inhalátor před každým postřikem.
Sundejte víčko z náustku pohonu. Hledejte uvnitř náustku cizí předměty a všechny, které vidíte, vyjměte.
Krok 2. Držte inhalátor náustkem dolů. Vidět Obrázek E .
Obrázek E 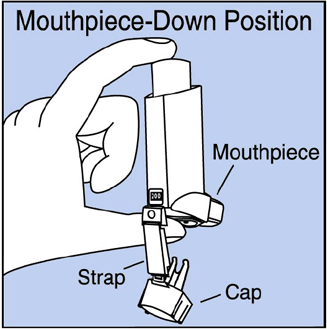
Krok 3 Vydechněte ústy a vytlačte z plic co nejvíce vzduchu. Vložte náustek do úst a sevřete kolem něj rty. Viz obrázek F .
Obrázek F 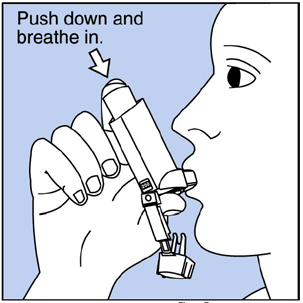
Krok 4. Zatlačte horní část nádobky až na doraz, zatímco se zhluboka a pomalu nadechujete ústy. Vidět Obrázek F .
Krok 5. Jakmile sprej vyteče, sundejte prst z kanystru. Poté, co se úplně nadechnete, vyjměte inhalátor z úst a zavřete ústa.
Krok 6. Zadržte dech asi 10 sekund nebo tak dlouho, jak je to pohodlné. Potichu vydechujte, dokud můžete.
Pokud vám váš poskytovatel zdravotní péče řekl, abyste se modlili, počkejte 1 minutu a znovu inhalátorem protřepejte. Opakujte kroky 2 až 6.
Krok 7. Po každém použití inhalátoru nasaďte uzávěr zpět na náustek. Ujistěte se, že pevně zapadla na místo.
Čištění vašeho inhalátoru VENTOLIN HFA
Vyčistěte svůj inhalátor alespoň 1krát týdně. Na inhalátoru možná neuvidíte žádné usazeniny léku, ale je důležité udržovat jej čistý, aby nahromaděný lék neblokoval sprej. Viz obrázek G.
Obrázek G 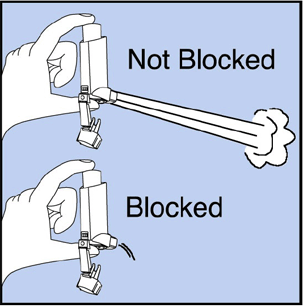
Krok 8. Vyjměte nádobku z ovladače a sejměte uzávěr z náustku. Pásek na uzávěru zůstane připojen k pohonu.
Krok 9. Podržte pohon pod kohoutkem a nechte jím protékat teplou vodu po dobu asi 30 sekund. Vidět Obrázek H.
Obrázek H 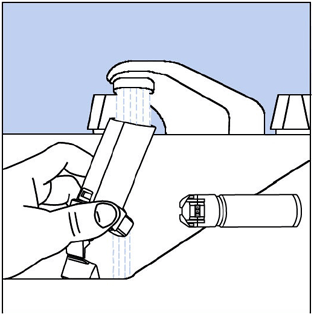
Krok 10. Otočte akční člen vzhůru nohama a nechte protékat teplou vodou náustkem po dobu asi 30 sekund. Vidět Obrázek I .
Obrázek I 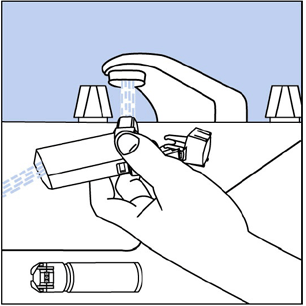
Krok 11. Setřeste z pohonu co nejvíce vody. Podívejte se do náustku, abyste se ujistili, že veškerý nahromaděný lék byl zcela smyt. Pokud dojde k nahromadění, opakujte kroky 9 a 10.
Krok 12. Nechte akční člen přes noc vyschnout na vzduchu. Viz obrázek J.
Obrázek J 
Krok 13. Když je aktuátor suchý, nasaďte ochranný kryt na náustek a poté vložte nádobku do aktuátoru a ujistěte se, že pevně sedí. Inhalátor dobře protřepejte, sejměte uzávěr a jednou vystříkněte inhalátor do vzduchu směrem od vašeho obličeje. (Počítadlo bude odpočítávat 1 číslo.) Nasaďte uzávěr zpět na náustek.
Pokud potřebujete použít inhalátor předtím, než je aktuátor zcela suchý:
- Setřeste z pohonu tolik vody, kolik můžete.
- Nasaďte uzávěr na náustek a poté vložte nádobku do aktuátoru a ujistěte se, že pevně sedí.
- Inhalátor dobře protřepejte a vystříkněte jej 1x do vzduchu směrem od obličeje.
- Užívejte dávku VENTOLIN HFA podle předpisu.
- Proveďte čištění podle kroků 8 až 13 výše.
Výměna inhalátoru VENTOLIN HFA:
- Když počítadlo ukazuje 020, měli byste si doplnit předpis nebo se zeptat svého poskytovatele zdravotní péče, pokud potřebujete další předpis na VENTOLIN HFA.
- Vyhoďte inhalátor když počítadlo čte 0 nebo 12 měsíců po otevření fóliového sáčku, podle toho, co nastane dříve. Neměli byste nadále používat inhalátor, když počítadlo ukazuje 000, protože nedostanete správné množství léku.
- Nepoužívejte inhalátor po datu expirace, které je uvedeno na obalu, ve kterém je dodáván.
Pro správné používání vašeho inhalátoru VENTOLIN HFA mějte na paměti:
- Kanystr by měl vždy pevně zapadnout do ovladače.
- Zhluboka a pomalu se nadechněte, abyste se ujistili, že dostanete všechen lék.
- Po vdechnutí léku zadržte dech asi na 10 sekund. Poté plně vydechněte.
- Když inhalátor nepoužíváte, vždy mějte na náustku ochranný kryt.
- Vždy uchovávejte inhalátor tak, aby náustek směřoval dolů.
- Vyčistěte svůj inhalátor alespoň 1krát týdně.
Máte-li dotazy ohledně VENTOLIN HFA nebo jak používat váš inhalátor, zavolejte GlaxoSmithKline (GSK) na číslo 1-888-825-5249 nebo navštivte www.ventolin.com.
Tyto informace pro pacienty a návod k použití byly schváleny americkým Úřadem pro kontrolu potravin a léčiv.
