Reglan 10mg Metoclopramide Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Reglan 10 mg a jak se používá?
Reglan 10 mg je lék na předpis používaný k léčbě příznaků gastroezofageální refluxní choroby (GERD), nevolnosti a zvracení způsobených chemoterapií, diabetické gastroparézy a během radiologie horního gastrointestinálního traktu. Reglan 10 mg lze užívat samostatně nebo s jinými léky.
Reglan 10 mg patří do třídy léků nazývaných antiemetika; Prokinetická činidla.
Jaké jsou možné vedlejší účinky přípravku Reglan 10 mg?
Reglan může způsobit závažné nežádoucí účinky včetně:
- třes nebo chvění v rukou nebo nohou,
- zmatek,
- Deprese,
- myšlenky na sebevraždu nebo sebepoškození,
- pomalé nebo trhavé pohyby svalů v obličeji,
- křeče (záchvaty),
- úzkost,
- míchání,
- pocit nervozity,
- problém zůstat v klidu,
- problémy se spánkem (nespavost),
- otok,
- dušnost,
- rychlý nárůst hmotnosti,
- velmi ztuhlé nebo ztuhlé svaly,
- vysoká horečka,
- pocení,
- zmatek,
- rychlý nebo nerovnoměrný srdeční tep a
- točení hlavy
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější nežádoucí účinky přípravku Reglan 10 mg patří:
- neklid,
- ospalost,
- nedostatek energie,
- nevolnost,
- zvracení,
- bolest hlavy,
- zmatek a
- problémy se spánkem (nespavost)
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky přípravku Reglan. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
VAROVÁNÍ
TARDIVNÍ DYSKINEZE
Léčba metoklopramidem může způsobit tardivní dyskinezi, závažnou pohybovou poruchu, která je často nevratná. Riziko rozvoje tardivní dyskineze se zvyšuje s délkou léčby a celkovou kumulativní dávkou.
Léčba metoklopramidem by měla být přerušena u pacientů, u kterých se rozvinou známky nebo příznaky tardivní dyskineze. Není známa žádná léčba tardivní dyskineze. U některých pacientů se příznaky mohou zmírnit nebo vymizet po ukončení léčby metoklopramidem.
Léčbě metoklopramidem po dobu delší než 12 týdnů je třeba se vyhnout ve všech kromě vzácných případů, kdy se předpokládá, že terapeutický přínos převáží riziko rozvoje tardivní dyskineze.
Viz VAROVÁNÍ
POPIS
Pro perorální podání jsou tablety reglan® (tablety metoklopramidu, USP) 10 mg bílé tablety ve tvaru tobolky s půlicí rýhou, s vyrytým „REGLAN“ na jedné straně a „ANI 10“ na druhé straně.
Každá tableta obsahuje:
Metoklopramid báze 10 mg (jako monohydrát monohydrochloridu)
Neaktivní ingredience
Stearát hořečnatý, mannitol, mikrokrystalická celulóza, kyselina stearová.
reglan® tablety (metoklopramidové tablety, USP) 5 mg jsou zelené tablety eliptického tvaru s vyrytým „REGLAN“ nad „5“ na jedné straně a „ANI“ na opačné straně.
Každá tableta obsahuje:
Metoklopramid báze 5 mg (jako monohydrát monohydrochloridu)
Neaktivní ingredience
Kukuřičný škrob, D&C Yellow 10 Aluminium Lake, FD&C Blue 1 Aluminium Lake, laktóza, mikrokrystalická celulóza, oxid křemičitý, kyselina stearová.
Metoklopramid hydrochlorid je bílá krystalická látka bez zápachu, volně rozpustná ve vodě. Chemicky se jedná o monohydrát monohydrochloridu 4-amino-5-chlor-N-[2-(diethylamino)ethyl]-2-methoxybenzamidu. Jeho molekulární vzorec je C14H22ClN3O2 • HCl • H2O. Jeho molekulová hmotnost je 354,3.
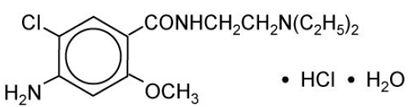
INDIKACE
Užívání tablet reglan® se doporučuje pouze pro dospělé. Léčba by neměla trvat déle než 12 týdnů.
Symptomatický gastroezofageální reflux
reglan® tablety jsou indikovány jako krátkodobá (4 až 12 týdnů) terapie pro dospělé se symptomatickým, dokumentovaným gastroezofageálním refluxem, kteří nereagují na konvenční léčbu.
Hlavní účinek metoklopramidu je na symptomy postprandiálního a denního pálení žáhy s méně pozorovaným účinkem na noční symptomy. Pokud se symptomy omezují na konkrétní situace, jako je po večeři, je třeba zvážit použití metoklopramidu v jednotlivých dávkách před provokativní situací spíše než užívání léku během dne. Hojení vředů a erozí jícnu bylo endoskopicky prokázáno na konci 12týdenní studie s použitím dávek 15 mg qid. Vzhledem k tomu, že neexistuje žádná zdokumentovaná korelace mezi symptomy a hojením lézí jícnu, pacienti s dokumentovanými lézemi by měli být endoskopicky sledováni.
Diabetická gastroparéza (diabetická žaludeční stáza)
reglan® tablety (metoklopramidové tablety, USP) je indikován k úlevě od příznaků spojených s akutní a recidivující diabetickou žaludeční stázou. Zdá se, že obvyklé projevy opožděného vyprazdňování žaludku (např. nevolnost, zvracení, pálení žáhy, přetrvávající plnost po jídle a anorexie) reagují na reglan® v různých časových intervalech. K významné úlevě od nevolnosti dochází brzy a nadále se zlepšuje po dobu tří týdnů. Úleva od zvracení a anorexie může předcházet úlevě od plnosti břicha o jeden týden nebo déle.
DÁVKOVÁNÍ A PODÁVÁNÍ
Léčba tabletami reglan® by neměla trvat déle než 12 týdnů.
Pro úlevu od symptomatického gastroezofageálního refluxu
Podávejte od 10 mg do 15 mg reglan® (metoklopramid hydrochlorid, USP) perorálně až qid 30 minut před každým jídlem a před spaním, v závislosti na léčených příznacích a klinické odpovědi (viz KLINICKÁ FARMAKOLOGIE a INDIKACE A POUŽITÍ ). Pokud se symptomy vyskytují pouze přerušovaně nebo v určitou denní dobu, může být před kontinuální léčbou upřednostněno použití metoklopramidu v jednotlivých dávkách až do 20 mg před provokující situací. Občas budou pacienti (jako jsou starší pacienti), kteří jsou citlivější na terapeutické nebo nežádoucí účinky metoklopramidu, potřebovat pouze 5 mg na dávku.
Zkušenosti s erozemi a ulceracemi jícnu jsou omezené, ale hojení bylo dosud dokumentováno v jedné kontrolované studii s qid terapií v dávce 15 mg/dávku a tento režim by měl být použit, pokud jsou přítomny léze, pokud je tolerováno (viz NEŽÁDOUCÍ REAKCE ). Vzhledem ke špatné korelaci mezi symptomy a endoskopickým vzhledem jícnu je terapie zaměřená na léze jícnu nejlépe vedena endoskopickým hodnocením.
Léčba delší než 12 týdnů nebyla hodnocena a nelze ji doporučit.
Pro úlevu od příznaků souvisejících s diabetickou gas tropares is (Diabetic Gastric Stas is ) Podávejte 10 mg metoklopramidu 30 minut před každým jídlem a před spaním po dobu dvou až osmi týdnů, v závislosti na reakci a pravděpodobnosti trvalé pohody. při vysazení léku.
Počáteční cesta podání by měla být určena závažností přítomných symptomů. Pokud jsou přítomny pouze nejčasnější projevy diabetické žaludeční stáze, může být zahájeno perorální podávání reglanu®. Jsou-li však přítomny závažné příznaky, léčba by měla začít injekcí metoklopramidu (před zahájením parenterálního podání si prostudujte označení injekce).
Než symptomy odezní, může být nutné podání injekce metoklopramidu po dobu až 10 dnů, kdy může být zahájeno perorální podávání. Vzhledem k tomu, že diabetická žaludeční stáza je často recidivující, měla by být léčba reglanem obnovena při nejčasnějším projevu.
Použití u pacientů s poruchou ledvin nebo jater
Vzhledem k tomu, že metoklopramid je vylučován hlavně ledvinami, u pacientů, jejichž clearance kreatininu je nižší než 40 ml/min, by měla být léčba zahájena přibližně poloviční dávkou doporučené dávky. V závislosti na zvážení klinické účinnosti a bezpečnosti může být dávka zvýšena nebo snížena podle potřeby.
Vidět PŘEDÁVKOVAT sekce pro informace týkající se dialýzy.
Metoklopramid podléhá minimálnímu jaternímu metabolismu, s výjimkou jednoduché konjugace. Jeho bezpečné použití bylo popsáno u pacientů s pokročilým onemocněním jater, jejichž funkce ledvin byla normální.
JAK DODÁVÁNO
Každá bílá tableta reglan® ve tvaru tobolky s rýhou (metoklopramidové tablety, USP) obsahuje 10 mg metoklopramidové báze (jako monohydrát monohydrochloridu). K dispozici v:
Lahvičky po 100 tabletách ( NDC 62559-166-01)
Každá zelená tableta reglan® eliptického tvaru (metoklopramidové tablety, USP) obsahuje 5 mg metoklopramidové báze (jako monohydrát monohydrochloridu). K dispozici v:
Lahvičky po 100 tabletách ( NDC 62559-165-01)
Dávkujte tablety v těsném, světlu odolném obalu.
Tablety by měly být skladovány při kontrolované pokojové teplotě, mezi 20 °C a 25 °C (68 °F a 77 °F).
Výrobce: ANI Pharmaceuticals, Inc. Baudette, MN 56623. Revize: prosinec 2014
VEDLEJŠÍ EFEKTY
Obecně výskyt nežádoucích účinků koreluje s dávkou a délkou podávání metoklopramidu. Byly hlášeny následující reakce, ačkoli ve většině případů údaje neumožňují odhad frekvence:
Účinky na CNS
Neklid, ospalost, únava a malátnost se vyskytují přibližně u 10 % pacientů, kteří dostávají nejčastěji předepisovanou dávku 10 mg qid (viz OPATŘENÍ ). Nespavost, bolest hlavy, zmatenost, závratě nebo duševní deprese se sebevražednými myšlenkami (viz VAROVÁNÍ se vyskytují méně často. Výskyt ospalosti je vyšší při vyšších dávkách. Existují ojedinělé zprávy o konvulzivních záchvatech bez jasného vztahu k metoklopramidu. Vzácně byly hlášeny halucinace.
Extrapyramidové reakce (EPS)
Akutní dystonické reakce, nejběžnější typ EPS spojený s metoklopramidem, se vyskytují přibližně u 0,2 % pacientů (1 z 500) léčených 30 až 40 mg metoklopramidu denně. Symptomy zahrnují mimovolní pohyby končetin, obličejové grimasy, torticollis, okulogyrickou krizi, rytmické protruze jazyka, bulbární typ řeči, trismus, opistotonus (reakce podobné tetanu) a vzácně stridor a dušnost pravděpodobně způsobenou laryngospasmem; obvykle jsou tyto příznaky snadno zvráceny difenhydraminem (viz VAROVÁNÍ ).
Příznaky podobné Parkinsonově chorobě mohou zahrnovat bradykinezi, třes, ztuhlost ozubených kol, maskovité obličeje (viz VAROVÁNÍ ).
Tardivní dyskineze je nejčastěji charakterizována mimovolními pohyby jazyka, obličeje, úst nebo čelisti a někdy mimovolními pohyby trupu a/nebo končetin; pohyby mohou mít choreoatetotický vzhled (viz VAROVÁNÍ ).
Motorický neklid (akatizie) se může skládat z pocitů úzkosti, agitovanosti, nervozity a nespavosti, stejně jako z neschopnosti sedět v klidu, přecházení, klepání nohou. Tyto příznaky mohou spontánně vymizet nebo reagovat na snížení dávky.
Neuroleptický maligní syndrom
Byly hlášeny vzácné výskyty neuroleptického maligního syndromu (NMS). Tento potenciálně fatální syndrom se skládá z komplexu příznaků hypertermie, změněného vědomí, svalové rigidity a autonomní dysfunkce (viz VAROVÁNÍ ).
Endokrinní poruchy
Galaktorea, amenorea, gynekomastie, impotence sekundární k hyperprolaktinemii (viz OPATŘENÍ ). Sekundární retence tekutin po přechodném zvýšení aldosteronu (viz KLINICKÁ FARMAKOLOGIE ).
Kardiovaskulární
Hypotenze, hypertenze, supraventrikulární tachykardie, bradykardie, retence tekutin, akutní městnavé srdeční selhání a možná AV blokáda (viz KONTRAINDIKACE a OPATŘENÍ ).
Gastrointestinální
Nevolnost a poruchy střev, především průjem.
Jaterní
Vzácně se vyskytly případy hepatotoxicity, charakterizované takovými nálezy, jako je žloutenka a změněné jaterní testy, když byl metoklopramid podáván s jinými léky se známým hepatotoxickým potenciálem.
Renální
Frekvence moči a inkontinence.
Hematologické
Několik případů neutropenie, leukopenie nebo agranulocytózy, obecně bez jasného vztahu k metoklopramidu. Methemoglobinémie u dospělých a zvláště při předávkování u novorozenců (viz PŘEDÁVKOVAT ). Sulfhemoglobinémie u dospělých.
Alergické reakce
Několik případů vyrážky, kopřivky nebo bronchospasmu, zejména u pacientů s astmatem v anamnéze. Vzácně angioneurotický edém, včetně glosálního nebo laryngeálního edému.
Smíšený
Poruchy zraku. porfyrie.
DROGOVÉ INTERAKCE
Účinky metoklopramidu na gastrointestinální motilitu jsou antagonizovány anticholinergními léky a narkotickými analgetiky. Aditivní sedativní účinky se mohou objevit, pokud je metoklopramid podáván s alkoholem, sedativy, hypnotiky, narkotiky nebo trankvilizéry.
Zjištění, že metoklopramid uvolňuje katecholaminy u pacientů s esenciální hypertenzí, naznačuje, že by měl být používán opatrně, pokud vůbec, u pacientů užívajících inhibitory monoaminooxidázy.
Absorpce léků ze žaludku může být snížena (např. digoxin) metoklopramidem, zatímco rychlost a/nebo rozsah absorpce léků z tenkého střeva může být zvýšena (např. acetaminofen, tetracyklin, levodopa, ethanol, cyklosporin).
Gastroparéza (žaludeční stáza) může být u některých pacientů zodpovědná za špatnou kontrolu diabetu. Exogenně podávaný inzulín může začít působit dříve, než potrava opustí žaludek a vést k hypoglykémii. Protože účinek metoklopramidu ovlivní dodávku potravy do střev, a tím i rychlost absorpce, může dávkování inzulínu nebo načasování dávkování vyžadovat úpravu.
VAROVÁNÍ
Duševní deprese se vyskytla u pacientů s depresí v anamnéze i bez ní. Příznaky se pohybovaly od mírných až po těžké a zahrnovaly sebevražedné myšlenky a sebevraždu. Metoklopramid by měl být podáván pacientům s předchozí anamnézou deprese, pouze pokud očekávaný přínos převáží potenciální rizika.
Extrapyramidové příznaky, projevující se primárně jako akutní dystonické reakce, se vyskytují přibližně u 1 z 500 pacientů léčených obvyklými dávkami metoklopramidu pro dospělé 30 až 40 mg/den. Ty jsou obvykle pozorovány během prvních 24 až 48 hodin léčby metoklopramidem, vyskytují se častěji u pediatrických pacientů a dospělých pacientů mladších 30 let a jsou ještě častější při vyšších dávkách. Tyto příznaky mohou zahrnovat mimovolní pohyby končetin a obličejové grimasy, torticollis, okulogyrickou krizi, rytmické protruze jazyka, bulbární typ řeči, trismus nebo dystonické reakce připomínající tetanus. Vzácně se mohou dystonické reakce projevit jako stridor a dušnost, pravděpodobně v důsledku laryngospasmu. Pokud se tyto příznaky objeví, aplikujte 50 mg difenhydramin hydrochloridu intramuskulárně a obvykle odezní. Ke zvrácení těchto reakcí lze také použít benztropin mesylát, 1 až 2 mg intramuskulárně.
Objevily se příznaky podobné Parkinsonově chorobě, častěji během prvních 6 měsíců po zahájení léčby metoklopramidem, ale příležitostně i po delších obdobích. Tyto příznaky obvykle odezní během 2 až 3 měsíců po vysazení metoklopramidu. Pacientům s již existující Parkinsonovou chorobou by měl být metoklopramid podáván opatrně, pokud vůbec, protože u těchto pacientů může při užívání metoklopramidu dojít k exacerbaci parkinsonských příznaků.
Tardivní dyskineze
(Viz BOX VAROVÁNÍ)
Léčba metoklopramidem může způsobit tardivní dyskinezi (TD), potenciálně nevratnou a znetvořující poruchu charakterizovanou mimovolními pohyby obličeje, jazyka nebo končetin. Riziko rozvoje tardivní dyskineze se zvyšuje s délkou léčby a celkovou kumulativní dávkou. Analýza vzorců užívání ukázala, že asi 20 % pacientů, kteří užívali metoklopramid, jej užívalo déle než 12 týdnů. Léčbě metoklopramidem po dobu delší než doporučených 12 týdnů je třeba se vyhnout ve všech kromě vzácných případů, kdy se předpokládá, že terapeutický přínos převáží riziko rozvoje TD.
Přestože riziko rozvoje TD v obecné populaci může být zvýšené u starších osob, žen a diabetiků, není možné předpovědět, u kterých pacientů se vyvine TD vyvolaná metoklopramidem. Jak riziko rozvoje TD, tak pravděpodobnost, že se TD stane nevratným, se zvyšuje s délkou léčby a celkovou kumulativní dávkou.
Metoklopramid by měl být vysazen u pacientů, u kterých se rozvinou známky nebo příznaky TD. Není známa účinná léčba prokázaných případů TD, ačkoli u některých pacientů může TD částečně nebo úplně ustoupit během několika týdnů až měsíců po vysazení metoklopramidu.
Samotný metoklopramid může potlačit nebo částečně potlačit příznaky TD, čímž maskuje základní proces onemocnění. Účinek této symptomatické suprese na dlouhodobý průběh TD není znám. Metoklopramid by se proto neměl používat k symptomatické kontrole TD.
Neuroleptický maligní syndrom (NMS)
Vzácně byly hlášeny případy méně častého, ale potenciálně fatálního komplexu symptomů, někdy označovaného jako neuroleptický maligní syndrom (NMS) spojený s metoklopramidem. Mezi klinické projevy NMS patří hypertermie, svalová rigidita, změněné vědomí a známky autonomní nestability (nepravidelný puls nebo krevní tlak, tachykardie, pocení a srdeční arytmie).
Diagnostické hodnocení pacientů s tímto syndromem je složité. Při stanovení diagnózy je důležité identifikovat případy, kdy klinický obraz zahrnuje jak závažná zdravotní onemocnění (např. zápal plic, systémová infekce atd.), tak neléčené nebo nedostatečně léčené extrapyramidové příznaky a symptomy (EPS). Další důležitá hlediska v diferenciální diagnostice zahrnují centrální anticholinergní toxicitu, úpal, maligní hypertermii, horečku po drogách a primární patologii centrálního nervového systému (CNS).
Léčba NMS by měla zahrnovat 1) okamžité vysazení metoklopramidu a dalších léků, které nejsou nezbytné pro souběžnou léčbu, 2) intenzivní symptomatickou léčbu a lékařské sledování a 3) léčbu jakýchkoli doprovodných závažných zdravotních problémů, pro které je k dispozici specifická léčba. Bromokriptin a dantrolen sodný byly použity v léčbě NMS, ale jejich účinnost nebyla stanovena (viz NEŽÁDOUCÍ REAKCE ).
OPATŘENÍ
Všeobecné
V jedné studii u pacientů s hypertenzí bylo prokázáno, že intravenózně podaný metoklopramid uvolňuje katecholaminy; proto je třeba opatrnosti při podávání metoklopramidu pacientům s hypertenzí.
Vzhledem k tomu, že metoklopramid způsobuje přechodné zvýšení plazmatického aldosteronu, u některých pacientů, zejména u pacientů s cirhózou nebo městnavým srdečním selháním, může být riziko rozvoje retence tekutin a objemového přetížení. Pokud se tyto nežádoucí účinky vyskytnou kdykoli během léčby metoklopramidem, je třeba léčbu přerušit.
Po ukončení užívání přípravku reglan® se mohou objevit nežádoucí účinky, zejména ty, které postihují nervový systém. U malého počtu pacientů může po vysazení přípravku reglan® dojít k abstinenčnímu období, které může zahrnovat závratě, nervozitu a/nebo bolesti hlavy.
Informace pro pacienty
Použití reglanu® se doporučuje pouze pro dospělé. Metoklopramid může narušit duševní a/nebo fyzické schopnosti potřebné pro provádění nebezpečných úkolů, jako je obsluha strojů nebo řízení motorového vozidla. Ambulantní pacient by měl být odpovídajícím způsobem varován.
Pro další informace by pacienti měli být poučeni, aby si prohlédli Medikační příručku pro tablety reglan®.

Karcinogeneze, mutageneze, zhoršení plodnosti
77týdenní studie byla provedena na potkanech s perorálními dávkami až do přibližně 40násobku maximální doporučené denní dávky pro člověka. Metoklopramid zvyšuje hladiny prolaktinu a toto zvýšení přetrvává během chronického podávání. Experimenty na tkáňových kulturách ukazují, že přibližně jedna třetina lidských karcinomů prsu je in vitro závislá na prolaktinu, což je faktor potenciální důležitosti, pokud se uvažuje o předepisování metoklopramidu u pacientky s dříve zjištěnou rakovinou prsu. Ačkoli byly u léků zvyšujících hladinu prolaktinu hlášeny poruchy jako galaktorea, amenorea, gynekomastie a impotence, klinický význam zvýšených hladin prolaktinu v séru je u většiny pacientů neznámý. Po chronickém podávání neuroleptik stimulujících prolaktin a metoklopramidu byl u hlodavců zjištěn nárůst novotvarů mléčné žlázy. Dosud provedené klinické studie ani epidemiologické studie však neprokázaly souvislost mezi chronickým podáváním těchto léků a tumorigenezí mléčné žlázy; dostupné důkazy jsou příliš omezené na to, aby byly v tuto chvíli nezvratné.
Amesův test mutagenity provedený u metoklopramidu byl negativní.
Těhotenství kategorie B
Reprodukční studie provedené na potkanech, myších a králících IV, IM, SC a perorálním podáním při maximálních hladinách v rozmezí 12 až 250násobku lidské dávky neprokázaly žádné poškození plodnosti nebo významné poškození plodu v důsledku metoklopramidu. Neexistují však žádné adekvátní a dobře kontrolované studie u těhotných žen. Vzhledem k tomu, že reprodukční studie na zvířatech nejsou vždy prediktivní pro lidskou odpověď, měl by být tento lék používán během těhotenství pouze tehdy, je-li to nezbytně nutné.
Kojící matky
Metoklopramid se vylučuje do lidského mléka. Při podávání metoklopramidu kojící matce je třeba postupovat opatrně.
Pediatrické použití
Bezpečnost a účinnost u pediatrických pacientů nebyla stanovena (viz PŘEDÁVKOVAT ).
Při podávání metoklopramidu novorozencům je třeba postupovat opatrně, protože prodloužená clearance může způsobit nadměrné sérové koncentrace (viz KLINICKÁ FARMAKOLOGIE - Farmakokinetika ). Kromě toho mají novorozenci snížené hladiny NADH-cytochrom b5 reduktázy, což v kombinaci s výše uvedenými farmakokinetickými faktory činí novorozence náchylnějšími k methemoglobinémii (viz. PŘEDÁVKOVAT ).
Bezpečnostní profil metoklopramidu u dospělých nelze extrapolovat na dětské pacienty. Dystonie a další extrapyramidové reakce spojené s metoklopramidem jsou častější u pediatrické populace než u dospělých. (Vidět VAROVÁNÍ a NEŽÁDOUCÍ REAKCE - Extrapyramidové reakce. )
Geriatrické použití
Klinické studie s reglanem® nezahrnovaly dostatečný počet subjektů ve věku 65 let a více, aby bylo možné určit, zda starší subjekty reagují odlišně od mladších subjektů.
Riziko rozvoje nežádoucích účinků podobných parkinsonismu se zvyšuje se stoupající dávkou. Starší pacienti by měli dostávat nejnižší dávku reglanu®, která je účinná. Pokud se u geriatrického pacienta užívajícího reglan® rozvinou symptomy podobné Parkinsonově chorobě, léčba reglanem® by měla být obecně přerušena před zahájením jakýchkoli specifických antiparkinsonických léků (viz VAROVÁNÍ a DÁVKOVÁNÍ A PODÁVÁNÍ – Pro úlevu od symptomatické plynatosti a refluxu ophageu ).
Starší lidé mohou být vystaveni většímu riziku tardivní dyskineze (viz VAROVÁNÍ - Tardivní dyskineze ).
U uživatelů reglanu® byla hlášena sedace. Sedace může způsobit zmatenost a projevit se jako nadměrná sedace u starších osob (viz KLINICKÁ FARMAKOLOGIE , OPATŘENÍ – Informace pro pacienty a NEŽÁDOUCÍ REAKCE – Účinky na CNS ).
Je známo, že reglan® je v podstatě vylučován ledvinami a riziko toxických reakcí na tento lék může být vyšší u pacientů s poruchou funkce ledvin (viz DÁVKOVÁNÍ A PODÁVÁNÍ – Použití u pacientů s poruchou funkce ledvin nebo jater ).
těchto důvodů by měl být výběr dávky pro staršího pacienta opatrný, obvykle začíná na spodním konci dávkovacího rozmezí, což odráží vyšší frekvenci snížené funkce ledvin, souběžného onemocnění nebo jiné lékové terapie u starších osob (viz DÁVKOVÁNÍ A PODÁVÁNÍ – K úlevě od symptomatického gastroezofageálního refluxu a použití u pacientů s poruchou ledvin nebo jater ).
Jiné zvláštní populace
U pacientů s deficitem NADH-cytochrom b5 reduktázy je při podávání metoklopramidu zvýšené riziko rozvoje methemoglobinémie a/nebo sulfhemoglobinémie. U pacientů s nedostatkem G6PD, kteří prodělají metoklopramidem indukovanou methemoglobinémii, se léčba methylenovou modří nedoporučuje (viz PŘEDÁVKOVAT ).
PŘEDÁVKOVAT
Příznaky předávkování mohou zahrnovat ospalost, dezorientaci a extrapyramidové reakce. Anticholinergika nebo antiparkinsonika nebo antihistaminika s anticholinergními vlastnostmi mohou pomoci při kontrole extrapyramidových reakcí. Příznaky odezní samy a obvykle vymizí do 24 hodin.
Hemodialýza odstraňuje relativně málo metoklopramidu, pravděpodobně kvůli malému množství léku v krvi ve srovnání s tkáněmi. Podobně kontinuální ambulantní peritoneální dialýza neodstraní významné množství léku. Je nepravděpodobné, že by bylo nutné upravit dávkování, aby se kompenzovaly ztráty dialýzou. Dialýza pravděpodobně nebude účinnou metodou odstranění léku v situacích předávkování.
Neúmyslné předávkování způsobené nesprávným podáním bylo hlášeno u kojenců a dětí při použití perorálního roztoku metoklopramidu. I když neexistoval žádný konzistentní vzorec hlášení spojených s těmito předávkováními, příhody zahrnovaly záchvaty, extrapyramidové reakce a letargii.
Methemoglobinémie se vyskytla u nedonošených a donošených novorozenců, kterým byly podávány nadměrné dávky metoklopramidu (1 až 4 mg/kg/den perorálně, intramuskulárně nebo intravenózně po dobu 1 až 3 nebo více dnů). Methemoglobinemii lze zvrátit intravenózním podáním methylenové modři. Methylenová modř však může u pacientů s deficitem G6PD způsobit hemolytickou anémii, která může být fatální (viz OPATŘENÍ – Jiné zvláštní populace ).
KONTRAINDIKACE
Metoklopramid by se neměl používat vždy, když by stimulace gastrointestinální motility mohla být nebezpečná, např. v přítomnosti gastrointestinálního krvácení, mechanické obstrukce nebo perforace.
Metoklopramid je kontraindikován u pacientů s feochromocytomem, protože lék může způsobit hypertenzní krizi, pravděpodobně v důsledku uvolňování katecholaminů z nádoru. Takové hypertenzní krize mohou být kontrolovány fentolaminem.
Metoklopramid je kontraindikován u pacientů se známou citlivostí nebo intolerancí na lék. Metoklopramid by se neměl používat u epileptiků nebo pacientů užívajících jiné léky, které pravděpodobně způsobí extrapyramidové reakce, protože frekvence a závažnost záchvatů nebo extrapyramidových reakcí může být zvýšena.
KLINICKÁ FARMAKOLOGIE
Metoklopramid stimuluje motilitu horního gastrointestinálního traktu bez stimulace žaludeční, žlučové nebo pankreatické sekrece. Způsob jeho působení je nejasný. Zdá se, že senzibilizuje tkáně na působení acetylcholinu. Účinek metoklopramidu na motilitu nezávisí na intaktní inervaci vagu, ale lze jej zrušit anticholinergními léky.
Metoklopramid zvyšuje tonus a amplitudu žaludečních (zejména antrálních) kontrakcí, uvolňuje pylorický svěrač a bulbus duodena a zvyšuje peristaltiku duodena a jejuna, což má za následek zrychlené vyprazdňování žaludku a střevní tranzit. Zvyšuje klidový tonus dolního jícnového svěrače. Má malý, pokud vůbec nějaký, vliv na motilitu tlustého střeva nebo žlučníku.
U pacientů s gastroezofageálním refluxem a nízkým LESP (dolní tlak jícnového svěrače) jednorázové perorální dávky metoklopramidu vyvolávají na dávce závislé zvýšení LESP. Účinky začínají na přibližně 5 mg a zvyšují se až po 20 mg (nejvyšší testovaná dávka). Zvýšení LESP z dávky 5 mg trvá asi 45 minut a zvýšení 20 mg trvá 2 až 3 hodiny. Při jednorázové perorální dávce 10 mg byla pozorována zvýšená rychlost vyprazdňování žaludku.
Zdá se, že antiemetické vlastnosti metoklopramidu jsou výsledkem jeho antagonismu vůči centrálním a periferním dopaminovým receptorům. Dopamin vyvolává nevolnost a zvracení stimulací medulární chemoreceptorové spouštěcí zóny (CTZ) a metoklopramid blokuje stimulaci CTZ látkami, jako je ldopa nebo apomorfin, o kterých je známo, že zvyšují hladiny dopaminu nebo mají účinky podobné dopaminu. Metoklopramid také odstraňuje zpomalení vyprazdňování žaludku způsobené apomorfinem.
Podobně jako fenothiaziny a příbuzné léky, které jsou rovněž antagonisty dopaminu, vyvolává metoklopramid sedaci a může vyvolat extrapyramidové reakce, i když ty jsou poměrně vzácné (viz VAROVÁNÍ ). Metoklopramid inhibuje centrální a periferní účinky apomorfinu, indukuje uvolňování prolaktinu a způsobuje přechodné zvýšení hladin cirkulujícího aldosteronu, které může být spojeno s přechodnou retencí tekutin.
Nástup farmakologického účinku metoklopramidu je 1 až 3 minuty po intravenózní dávce, 10 až 15 minut po intramuskulárním podání a 30 až 60 minut po perorální dávce; farmakologické účinky přetrvávají 1 až 2 hodiny.
Farmakokinetika
Metoklopramid se rychle a dobře vstřebává. Ve vztahu k intravenózní dávce 20 mg je absolutní perorální biologická dostupnost metoklopramidu 80 % ± 15,5 %, jak bylo prokázáno ve zkřížené studii s 18 subjekty. Vrcholové plazmatické koncentrace se objevují přibližně za 1 až 2 hodiny po jednorázové perorální dávce. Podobná doba do vrcholu je pozorována po jednotlivých dávkách v ustáleném stavu.
Ve studii s jednorázovou dávkou u 12 subjektů se plocha pod křivkou závislosti koncentrace léčiva na čase lineárně zvyšuje s dávkami od 20 do 100 mg. Špičkové koncentrace rostou lineárně s dávkou; doba do dosažení maximálních koncentrací zůstává stejná; celotělová vůle je nezměněna; a rychlost eliminace zůstává stejná. Průměrný poločas eliminace u jedinců s normální funkcí ledvin je 5 až 6 hodin. Lineární kinetické procesy adekvátně popisují absorpci a eliminaci metoklopramidu.
Přibližně 85 % radioaktivity orálně podané dávky se objeví v moči během 72 hodin. Z 85 % vyloučených močí je asi polovina přítomna jako volný nebo konjugovaný metoklopramid.
Lék se ve velké míře neváže na plazmatické proteiny (asi 30 %). Distribuční objem po celém těle je vysoký (asi 3,5 l/kg), což naznačuje rozsáhlou distribuci léčiva do tkání.
Poškození ledvin ovlivňuje clearance metoklopramidu. Ve studii s pacienty s různým stupněm poruchy funkce ledvin korelovalo snížení clearance kreatininu se snížením plazmatické clearance, renální clearance, nerenální clearance a prodloužením eliminačního poločasu. Kinetika metoklopramidu v přítomnosti poruchy funkce ledvin však zůstala lineární. Snížení clearance v důsledku poruchy funkce ledvin naznačuje, že je třeba upravit udržovací dávku směrem dolů, aby se zabránilo akumulaci léku.
Farmakokinetická data pro dospělé
U pediatrických pacientů je farmakodynamika metoklopramidu po perorálním a intravenózním podání vysoce variabilní a vztah koncentrace-účinek nebyl stanoven.
závěru, zda je farmakokinetika metoklopramidu u dospělých a pediatrické populace podobná, není dostatek spolehlivých údajů. Ačkoli nejsou k dispozici dostatečné údaje, které by podpořily účinnost metoklopramidu u pediatrických pacientů se symptomatickým gastroezofageálním refluxem (GER) nebo nevolností a zvracením souvisejícím s chemoterapií rakoviny, jeho farmakokinetika byla studována u těchto populací pacientů.
otevřené studii dostávalo šest pediatrických pacientů (věkové rozmezí 3,5 týdne až 5,4 měsíce) s GER metoklopramid 0,15 mg/kg perorální roztok každých 6 hodin v 10 dávkách. Průměrná maximální plazmatická koncentrace metoklopramidu po desáté dávce byla 2krát vyšší (56,8 μg/l) ve srovnání s koncentrací pozorovanou po první dávce (29 μg/l), což ukazuje na akumulaci léku při opakovaném podávání. Po desáté dávce byl průměrný čas k dosažení maximálních koncentrací (2,2 h), poločas (4,1 h), clearance (0,67 l/h/kg) a distribuční objem (4,4 l/kg) metoklopramidu podobné jako ty pozorované po první dávce. U nejmladšího pacienta (věk 3,5 týdne) byl poločas metoklopramidu po první a desáté dávce (23,1 a 10,3 h) významně delší ve srovnání s ostatními kojenci v důsledku snížené clearance. To lze přičíst nezralým jaterním a renálním systémům při narození.
Jednorázové intravenózní dávky metoklopramidu 0,22 až 0,46 mg/kg (průměrně 0,35 mg/kg) byly podávány během 5 minut 9 dětským pacientům s rakovinou, kteří dostávali chemoterapii (průměrný věk 11,7 let; rozmezí 7 až 14 let) za účelem profylaxe cytotoxických látek. vyvolané zvracení. Plazmatické koncentrace metoklopramidu extrapolované do času nula se pohybovaly od 65 do 395 μg/l (průměr 152 μg/l). Průměrný eliminační poločas, clearance a distribuční objem metoklopramidu byly 4,4 h (rozmezí 1,7 až 8,3 h), 0,56 l/h/kg (rozmezí 0,12 až 1,20 l/h/kg) a 3,0 l/ kg (rozsah 1,0 až 4,8 l/kg).
jiné studii dostalo devět dětských pacientů s rakovinou (věkové rozmezí 1 až 9 let) 4 až 5 intravenózních infuzí (po dobu 30 minut) metoklopramidu v dávce 2 mg/kg ke kontrole zvracení. Po poslední dávce se maximální sérové koncentrace metoklopramidu pohybovaly od 1060 do 5680 μg/l. Průměrný eliminační poločas, clearance a distribuční objem metoklopramidu byly 4,5 h (rozmezí 2,0 až 12,5 h), 0,37 l/h/kg (rozmezí 0,10 až 1,24 l/h/kg) a 1,93 l/ kg (rozsah, 0,95 až 5,50 l/kg), resp.
INFORMACE PRO PACIENTA
REGLAN (REG-lan) (metoklopramid tablety) Tablety
Než začnete užívat přípravek REGLAN a pokaždé, když dostanete náplň, přečtěte si Průvodce léčivými přípravky, který je dodáván s přípravkem REGLAN. Mohou se objevit nové informace. Pokud užíváte jiný přípravek, který obsahuje metoklopramid (jako je REGLAN 10 mg injekce, REGLAN ODT nebo metoklopramid perorální roztok), měli byste si přečíst Příručku o medikaci, která je součástí tohoto přípravku. Některé informace se mohou lišit. Tento průvodce léky nenahrazuje rozhovor s lékařem o vašem zdravotním stavu nebo léčbě.
Jaké jsou nejdůležitější informace, které bych měl vědět o REGLAN?
REGLAN může způsobit závažné nežádoucí účinky, včetně:
Tardivní dyskineze (abnormální pohyby svalů). Tyto pohyby se většinou odehrávají v obličejových svalech. Tyto pohyby nemůžete ovládat. Nemusí zmizet ani po vysazení přípravku REGLAN. Na tardivní dyskinezi neexistuje žádná léčba, ale příznaky se mohou po ukončení užívání přípravku REGLAN časem zmírnit nebo vymizet.
Vaše šance na získání tardivní dyskineze se zvyšují:
- čím déle budete užívat REGLAN 10 mg a tím více REGLAN 10 mg užíváte. REGLAN 10 mg byste neměli užívat déle než 12 týdnů.
- pokud jste starší, zvláště pokud jste žena
- jestliže máte cukrovku
Váš lékař nemůže vědět, zda se u Vás při užívání přípravku REGLAN objeví tardivní dyskineze.
Okamžitě zavolejte svého lékaře, pokud zaznamenáte pohyby, které nemůžete zastavit nebo ovládat, jako například:
- mlácení rtů, žvýkání nebo svrašťování úst
- mračit se nebo mračit
- vypláznout jazyk
- mrkání a pohyb očí
- třes rukou a nohou
Viz část "Jaké jsou možné nežádoucí účinky přípravku REGLAN 10 mg?" pro více informací o vedlejších účincích.
Co je REGLAN 10 mg?
REGLAN 10 mg je lék na předpis používaný:
- dospělých po dobu 4 až 12 týdnů ke zmírnění příznaků pálení žáhy s gastroezofageální refluxní chorobou (GERD), když některé jiné léčby nefungují. REGLAN zmírňuje denní pálení žáhy a pálení žáhy po jídle. Pomáhá také hojit vředy v jícnu.
- ke zmírnění příznaků pomalého vyprazdňování žaludku u lidí s cukrovkou. REGLAN pomáhá léčit příznaky, jako je nevolnost, zvracení, pálení žáhy, pocit plnosti dlouho po jídle a ztráta chuti k jídlu. Ne všechny tyto příznaky se zlepší současně.
Není známo, zda je přípravek REGLAN bezpečný a zda působí u dětí.
Kdo by neměl užívat REGLAN 10 mg?
Neužívejte REGLAN, pokud:
- máte žaludeční nebo střevní potíže, které se mohou s přípravkem REGLAN zhoršit, jako je krvácení, ucpání nebo trhlina v žaludku nebo střevní stěně
- máte nádor nadledvin nazývaný feochromocytom
- jste alergičtí na REGLAN 10 mg nebo cokoli v něm. Seznam složek v přípravku REGLAN naleznete na konci tohoto Průvodce léčivy.
- užívat léky, které mohou způsobit nekontrolované pohyby, jako jsou léky na duševní onemocnění, mající záchvaty
Co mám říct svému lékaři, než začnu užívat REGLAN?
Informujte svého lékaře o všech svých zdravotních potížích, včetně, pokud máte:
- Deprese
- Parkinsonova choroba
- vysoký krevní tlak
- problémy s ledvinami. Váš lékař může začít s nižší dávkou.
- problémy s játry nebo srdeční selhání. REGLAN může způsobit zadržování tekutin ve vašem těle.
- cukrovka. Možná bude nutné změnit dávku inzulinu.
- rakovina prsu
- jste těhotná nebo těhotenství plánujete. Není známo, zda REGLAN 10 mg poškodí vaše nenarozené dítě.
- kojíte. REGLAN 10 mg může přecházet do mateřského mléka a může poškodit Vaše dítě. Poraďte se se svým lékařem o nejlepším způsobu krmení dítěte, pokud užíváte REGLAN.
Informujte svého lékaře o všech lécích, které užíváte, včetně léků na předpis i bez předpisu, vitamínů a bylinných doplňků. REGLAN a některé další léky se mohou vzájemně ovlivňovat a nemusí tak dobře fungovat nebo způsobovat možné nežádoucí účinky. Během užívání přípravku REGLAN 10 mg nezačínejte užívat žádné nové léky, dokud si nepromluvíte se svým lékařem.
Zejména informujte svého lékaře, pokud užíváte:
- jiný lék, který obsahuje metoklopramid, jako je REGLAN 10 mg ODT nebo metoklopramid perorální roztok
- lék na krevní tlak
- lék na depresi, zejména inhibitor monoaminooxidázy (MAOI)
- inzulín
- lék, který vám může způsobit ospalost, jako jsou léky proti úzkosti, léky na spaní a narkotika.
Pokud si nejste jistý/á, zda je Váš lék uveden výše, zeptejte se svého lékaře nebo lékárníka.
Znát léky, které užíváte. Uchovávejte si jejich seznam a ukažte jej svému lékaři a lékárníkovi, když dostanete nový lék.
Jak mám užívat REGLAN?
- REGLAN 10 mg se dodává jako tableta, kterou užíváte ústy.
- Užívejte REGLAN přesně podle pokynů svého lékaře. Neměňte svou dávku, pokud vám to neřekne lékař.
- REGLAN byste neměli užívat déle než 12 týdnů.
- Jestliže jste užil(a) příliš mnoho přípravku REGLAN 10 mg, ihned zavolejte svého lékaře nebo toxikologické středisko.
Čemu se mám vyvarovat při užívání přípravku REGLAN?
- Během užívání přípravku REGLAN nepijte alkohol. Alkohol může zhoršit některé nežádoucí účinky přípravku REGLAN 10 mg, jako je pocit ospalosti.
- Neřiďte, nepracujte se stroji ani neprovádějte nebezpečné úkoly, dokud nevíte, jak na vás REGLAN působí. REGLAN může způsobit ospalost.
Jaké jsou možné vedlejší účinky přípravku REGLAN?
Reglan může způsobit závažné nežádoucí účinky, včetně:
- Tardivní dyskineze (abnormální pohyby svalů). Viz "Jaké jsou nejdůležitější informace, které potřebuji vědět o REGLAN?"
- Nekontrolované křeče obličejových a krčních svalů nebo svalů těla, paží a nohou (dystonie). Tyto svalové křeče mohou způsobit abnormální pohyby a polohy těla. Tyto křeče obvykle začínají během prvních 2 dnů léčby. Tyto křeče se vyskytují častěji u dětí a dospělých do 30 let.
- Deprese, myšlenky na sebevraždu a sebevraždu. Někteří lidé, kteří užívají REGLAN, upadají do deprese. Můžete mít myšlenky na ublížení nebo sebevraždu. Někteří lidé, kteří užívají Reglan, ukončili svůj vlastní život (sebevražda).
- Neuroleptický maligní syndrom (NMS). NMS je velmi vzácný, ale velmi vážný stav, který se může stát u přípravku Reglan. NMS může způsobit smrt a musí být léčena v nemocnici. Příznaky NMS zahrnují: vysokou horečku, ztuhlé svaly, problémy s myšlením, velmi rychlý nebo nerovnoměrný srdeční tep a zvýšené pocení.
- Parkinsonismus. Příznaky zahrnují mírný třes, ztuhlost těla, potíže s pohybem nebo udržením rovnováhy. Pokud již máte Parkinsonovu chorobu, mohou se Vaše příznaky během léčby přípravkem REGLAN zhoršit.
Zavolejte svého lékaře a okamžitě vyhledejte lékařskou pomoc, pokud:
- cítit se depresivně nebo mít myšlenky na sebepoškození nebo sebevraždu
- máte vysokou horečku, ztuhlé svaly, problémy s myšlením, velmi rychlý nebo nerovnoměrný srdeční tep a zvýšené pocení
- máte svalové pohyby, které nemůžete zastavit nebo ovládat
- máte svalové pohyby, které jsou nové nebo neobvyklé
Mezi časté nežádoucí účinky přípravku Reglan 10 mg patří:
- pocit neklidu, ospalosti, únavy, závratě nebo vyčerpání
- bolest hlavy
- zmatek
- problémové spaní
Čím déle užíváte REGLAN a čím více REGLANu užíváte, můžete mít více nežádoucích účinků.
Nežádoucí účinky můžete mít i po ukončení léčby přípravkem REGLAN. Můžete mít příznaky z vysazení (vysazení) přípravku REGLAN 10 mg, jako jsou bolesti hlavy, závratě nebo nervozita.
Informujte svého lékaře o jakýchkoli nežádoucích účincích, které vás obtěžují nebo nezmizí. To nejsou všechny možné vedlejší účinky přípravku REGLAN.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800- FDA-1088.
Jak mám REGLAN uchovávat?
- Uchovávejte REGLAN při pokojové teplotě mezi 68 °F až 77 °F (20 °C až 25 °C).
- Uchovávejte REGLAN 10 mg v lahvičce, ve které je dodáván. Lahvičku udržujte pevně uzavřenou.
Uchovávejte REGLAN 10 mg a všechny léky mimo dosah dětí.
Obecné informace o REGLAN
Léky jsou někdy předepisovány pro jiné účely, než které jsou uvedeny v Průvodci léky. Nepoužívejte REGLAN pro stav, pro který nebyl předepsán. Nedávejte REGLAN 10 mg jiným lidem, i když mají stejné příznaky jako vy. Může jim to ublížit.
Tento průvodce léky shrnuje nejdůležitější informace o přípravku REGLAN. Pokud chcete více informací, promluvte si se svým lékařem. Můžete požádat svého lékaře nebo lékárníka o informace o přípravku REGLAN 10 mg, který je určen pro zdravotnické pracovníky. Další informace najdete na www.anipharmaceuticals.com nebo zavolejte na bezplatné číslo 1-800-308-6755.
Jaké jsou složky přípravku REGLAN?
Aktivní složka: metoklopramid
Neaktivní složky:
REGLAN 10 mg tablety: stearát hořečnatý, mannitol, mikrokrystalická celulóza, kyselina stearová
REGLAN 5 mg tablety: kukuřičný škrob, hliníkový lak D&C yellow 10, hliníkový lak FD&C blue 1, laktóza, mikrokrystalická celulóza, oxid křemičitý, kyselina stearová
