Danazol 50mg, 100mg, 200mg Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Danazol 100 mg a jak se používá?
Danazol 50 mg je lék na předpis používaný k léčbě příznaků endometriózy, hereditárního angioedému a fibrocystického onemocnění prsu. Danazol lze užívat samostatně nebo s jinými léky.
Danazol patří do třídy léků nazývaných androgeny.
Není známo, zda je přípravek Danazol bezpečný a účinný u dětí.
Jaké jsou možné vedlejší účinky Danazolu?
Danazol 100 mg může způsobit závažné nežádoucí účinky, včetně:
- otoky rukou a nohou,
- menstruační změny (špinění, vynechání menstruace),
- změny nálady,
- nervozita,
- změny nálady,
- vyrážka,
- svědění,
- otok obličeje, jazyka nebo hrdla,
- silné závratě a
- potíže s dýcháním
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější nežádoucí účinky přípravku Danazol 200 mg patří:
- přibývání na váze,
- akné,
- mastná pleť nebo vlasy,
- proplachování,
- pocení,
- ztráta vlasů,
- změny hlasu (chrapot, změny výšky),
- bolest krku,
- abnormální růst ochlupení (u žen),
- vaginální suchost, podráždění, pálení nebo svědění,
- zmenšená velikost prsou,
- zadržování vody,
- Deprese,
- nadýmání,
- podrážděnost,
- změny menstruačního cyklu (špinění, nepravidelné krvácení, vynechání menstruace),
- nervozita a
- změny nálady
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
Toto nejsou všechny možné vedlejší účinky přípravku Danazol. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
POPIS
Danazol 50 mg je syntetický steroid odvozený od ethisteronu. Je to bílý až světle žlutý krystalický prášek, prakticky nerozpustný nebo nerozpustný ve vodě a mírně rozpustný v alkoholu. Chemicky je danazol 100 mg 17a-Pregna-2,4-dien-20-yno[2,3-d]-isoxazol-17-ol. Molekulární vzorec je C22H27NO2. Má molekulovou hmotnost 337,46 a následující strukturní vzorec:
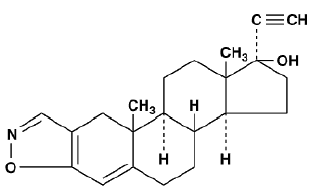
Tobolky Danazolu pro perorální podání obsahují 50 mg, 100 mg nebo 200 mg danazolu.
Neaktivní ingredience
bezvodá laktóza, monohydrát laktózy, magnesium-stearát, předbobtnalý škrob, laurylsulfát sodný, mastek. Obal tobolky pro 200 mg danazolu obsahuje D&C Yellow #10, FD&C Red #40, D&C Red #28, želatinu a oxid titaničitý. Obal tobolky pro 50 mg a 100 mg danazolu 50 mg obsahuje D&C Yellow # 10, FD&C Red # 40, želatinu a oxid titaničitý. Inkoust pro potisk kapslí obsahuje: šelakovou glazuru v ethanolu, černý oxid železitý, n-butylalkohol, propylenglykol, ethanol, metanol, hliníkové jezero FD&C modré č. 2, hliníkové jezero FD&C červené č. 40, hliníkové jezero FD&C modré č. 1 a D&C Yellow No. 10 Aluminium Lake.
INDIKACE
Endometrióza
Danazol 100 mg tobolky jsou indikovány k léčbě endometriózy podléhající hormonální léčbě.
Dědičný angioedém
Danazol tobolky jsou indikovány k prevenci záchvatů angioedému všech typů (kutánního, abdominálního, laryngeálního) u mužů a žen.
DÁVKOVÁNÍ A PODÁVÁNÍ
Endometrióza
středně těžkého až těžkého onemocnění nebo u pacientek neplodných v důsledku endometriózy se doporučuje počáteční dávka 800 mg podaná ve dvou dílčích dávkách. Amenorey a rychlé reakce na bolestivé symptomy je nejlépe dosaženo při této úrovni dávkování. V závislosti na odpovědi pacientky lze zvážit postupnou titraci směrem dolů na dávku dostatečnou k udržení amenorey. U mírných případů se doporučuje počáteční denní dávka 200 mg až 400 mg podaná ve dvou dílčích dávkách a může být upravena v závislosti na odpovědi pacienta. Terapie by měla začít během menstruace. Jinak by měly být provedeny příslušné testy, aby se zajistilo, že pacientka není těhotná během léčby danazolem 50 mg tobolky (viz KONTRAINDIKACE a VAROVÁNÍ ). Je nezbytné, aby léčba pokračovala bez přerušení po dobu 3 až 6 měsíců, ale v případě potřeby může být prodloužena na 9 měsíců. Po ukončení léčby, pokud se příznaky opakují, lze léčbu obnovit .
Dědičný angioedém
Požadavky na dávkování pro kontinuální léčbu hereditárního angioedému tobolkami danazolu by měly být individualizovány na základě klinické odpovědi pacienta. Doporučuje se, aby pacient začal s dávkou 200 mg dvakrát nebo třikrát denně. Po dosažení příznivé počáteční odpovědi ve smyslu prevence epizod edematózních záchvatů by mělo být správné pokračující dávkování stanoveno snížením dávky o 50 % nebo méně v intervalech jednoho až tří měsíců nebo déle, pokud to frekvence záchvatů před léčbou vyžaduje . Pokud dojde k záchvatu, může být denní dávka zvýšena až o 200 mg. Během fáze úpravy dávky je indikováno pečlivé sledování pacientovy odpovědi, zejména pokud má pacient v anamnéze postižení dýchacích cest.
JAK DODÁVÁNO
Danazol 50 mg kapsle USP, 50 mg jsou dostupné jako kukuřičné neprůhledné/bílé neprůhledné tobolky s potiskem „LANNETT“ na víčku a „1392“ na těle a jsou dodávány v:
Láhve po 100 ( NDC 0527-1392-01)
Danazol Kapsle USP, 100 mg jsou dostupné jako kukuřičné neprůhledné/kukuřičné neprůhledné tobolky s potiskem loga „LANNETT“ na víčku a „1368“ na těle a jsou dodávány v:
Láhve po 100 ( NDC 0527-1368-01)
Danazol Kapsle USP, 200 mg jsou dostupné jako oranžové neprůhledné/oranžové neprůhledné tobolky s potiskem „LANNETT“ na víčku a „1369“ na těle a jsou dodávány v:
Láhve po 60 ( NDC 0527-1369-06) Láhve po 100 ( NDC 0527-1369-01)
Skladujte při 20° až 25°C (68° až 77°F) [viz USP Regulovaná pokojová teplota].
Dávkujte v dobře uzavřené nádobě s dětským bezpečnostním uzávěrem, jak je definováno v USP.
Distribuuje: Lannett Company, Inc. Philadelphia, PA 19154. Revize: květen 2018
VEDLEJŠÍ EFEKTY
V souvislosti s užíváním danazolu 100 mg tobolky byly hlášeny následující příhody:
Účinky podobné androgenům zahrnují přibírání na váze, akné a seboreu. Může se objevit mírné hirsutismus, otoky, vypadávání vlasů, změna hlasu, která může mít podobu chrapotu, bolesti v krku nebo nestability či prohloubení výšky tónu, které mohou přetrvávat i po ukončení terapie. Hypertrofie klitorisu je vzácná.
Další možné endokrinní účinky jsou menstruační poruchy včetně špinění, změny načasování cyklu a amenorea. I když se cyklické krvácení a ovulace obvykle vrátí během 60-90 dnů po ukončení léčby danazolovými tobolkami, občas byla hlášena přetrvávající amenorea.
Zčervenání, pocení, vaginální suchost a podráždění a zmenšení velikosti prsou mohou odrážet snížení estrogenu. Byla hlášena nervozita a emoční labilita. U mužů může být během léčby patrné mírné snížení spermatogeneze. U pacientů, kteří dostávají dlouhodobou léčbu, se mohou vyskytnout abnormality objemu spermatu, viskozity, počtu spermií a motility.
pacientů, kteří dostávali denní dávku tobolek danazolu 400 mg nebo více, byla hlášena jaterní dysfunkce, o čemž svědčí reverzibilní zvýšené sérové enzymy a/nebo žloutenka. Doporučuje se, aby pacienti užívající tobolky danazolu byli sledováni na jaterní dysfunkci laboratorními testy a klinickým pozorováním. Byla hlášena závažná jaterní toxicita včetně cholestatické žloutenky, peliosis hepatis, jaterního adenomu, hepatocelulárního poškození, hepatocelulárního ikteru a jaterního selhání (viz VAROVÁNÍ a OPATŘENÍ ).
Během léčby danazolem 50 mg tobolky se mohou objevit abnormality v laboratorních testech včetně CPK, glukózové tolerance, glukagonu, globulinu vázajícího štítnou žlázu, globulinu vázajícího pohlavní hormony, dalších plazmatických proteinů, lipidů a lipoproteinů.
Byly hlášeny následující reakce, příčinná souvislost s podáním tobolek danazolu nebyla potvrzena ani vyvrácena;
Alergický: kopřivka, pruritus a vzácně ucpaný nos;
Účinky na CNS: bolest hlavy, nervozita a emoční labilita, závratě a mdloby, deprese, únava, poruchy spánku, třes, parestézie, slabost, poruchy vidění a vzácně i benigní intrakraniální hypertenze, úzkost, změny chuti k jídlu, zimnice a vzácně křeče, Guillain-Barrého syndrom ;
Gastrointestinální: gastroenteritida, nauzea, zvracení, zácpa a vzácně pankreatitida a slezinná pelióza;
Muskuloskeletální: svalové křeče nebo křeče nebo bolesti, bolesti kloubů, sevření kloubů, otoky kloubů, bolesti zad, krku nebo končetin a vzácně syndrom karpálního tunelu, který může být sekundární k zadržování tekutin;
Genitourinární: hematurie, prodloužená postterapeutická amenorea;
Hematologické: zvýšení počtu červených krvinek a krevních destiček. Může být vyvolána reverzibilní erytrocytóza, leukocytóza nebo polycytémie. Byla také zaznamenána eozinofilie, leukopenie a trombocytopenie.
Kůže: vyrážky (makulopapulární, vezikulární, papulární, purpurové, petechiální) a vzácně citlivost na slunce, Stevens-Johnsonův syndrom a erythema multiforme;
Jiný: zvýšená potřeba inzulinu u diabetických pacientů, změna libida, infarkt myokardu, palpitace, tachykardie, zvýšení krevního tlaku, intersticiální pneumonitida a vzácně katarakta, krvácení z dásní, horečka, bolest pánve, výtok z bradavek. Po dlouhodobém užívání byly ve vzácných případech hlášeny zhoubné nádory jater.
DROGOVÉ INTERAKCE
K prodloužení protrombinového času dochází u pacientů stabilizovaných na warfarinu.
Léčba danazolem 50 mg může způsobit zvýšení hladin karbamazepinu u pacientů užívajících oba léky.

Danazol 50 mg může způsobit inzulínovou rezistenci. Při užívání s antidiabetiky je třeba postupovat opatrně.
Danazol 100 mg může zvýšit plazmatické hladiny cyklosporinu a takrolimu, což vede ke zvýšení renální toxicity těchto léků. Při současném užívání s danazolem může být zapotřebí monitorování systémových koncentrací těchto léků a vhodná úprava dávkování.
Danazol 100 mg může zvýšit kalcemickou odpověď na syntetická analoga vitaminu D u primární hypoparatyreózy.
Riziko myopatie a rhabdomyolýzy se zvyšuje při současném podávání danazolu 50 mg se statiny, jako je simvastatin, atorvastatin a lovastatin. Při současném užívání je třeba postupovat opatrně. Konkrétní informace o omezeních dávek v přítomnosti danazolu naleznete na etiketě statinových léků.
VAROVÁNÍ
Užívání danazolu 100 mg v těhotenství je kontraindikováno. Bezprostředně před zahájením léčby se doporučuje provést citlivý test (např. test beta podjednotek, pokud je k dispozici) schopný určit časné těhotenství. Během léčby by měla být navíc používána nehormonální metoda antikoncepce. Pokud pacientka otěhotní během užívání danazolu 200 mg, podávání léku by mělo být přerušeno a pacientka by měla být informována o možném riziku pro plod. Expozice danazolu 200 mg in utero může mít za následek androgenní účinky na ženský plod; byly hlášeny případy hypertrofie klitorisu, labiální fúze, defektu urogenitálního sinu, vaginální atrézie a nejednoznačných genitálií (viz OPATŘENÍ : Těhotenství, teratogenní účinky).
Byly hlášeny tromboembolie, trombotické a tromboflebitické příhody včetně trombózy sagitálního sinu a život ohrožujících nebo smrtelných cévních mozkových příhod.
Zkušenosti s dlouhodobou léčbou danazolem 100 mg jsou omezené. Při dlouhodobém užívání byly pozorovány peliosis hepatis a benigní jaterní adenom. Peliosis hepatis a jaterní adenom mohou být tiché, dokud nejsou komplikované akutním, potenciálně život ohrožujícím intraabdominálním krvácením. Lékař by proto měl být na tuto možnost upozorněn. Je třeba se pokusit určit nejnižší dávku, která poskytne dostatečnou ochranu. Pokud byl lék zahájen v době exacerbace hereditárního angioneurotického edému v důsledku traumatu, stresu nebo jiné příčiny, je třeba zvážit pravidelné pokusy o snížení nebo ukončení léčby.
Danazol 100 mg byl spojován s několika případy benigní intrakraniální hypertenze známé také jako pseudotumor cerebri. Časné známky a příznaky benigní intrakraniální hypertenze zahrnují edém papily, bolest hlavy, nauzeu a zvracení a poruchy vidění. Pacienti s těmito příznaky by měli být vyšetřeni na edém papily a je-li přítomen, je třeba jim doporučit, aby okamžitě vysadili danazol 100 mg a byli odesláni k neurologovi k další diagnostice a péči.
Během léčby danazolem byla hlášena dočasná změna lipoproteinů ve formě snížených lipoproteinů s vysokou hustotou a možná zvýšení lipoproteinů s nízkou hustotou. Tyto změny mohou být výrazné a předepisující lékaři by měli zvážit potenciální dopad na riziko aterosklerózy a onemocnění koronárních tepen v souladu s potenciálním přínosem terapie pro pacienta.
Pacienti by měli být pečlivě sledováni, zda se u nich nevyskytují známky androgenních účinků, z nichž některé nemusí být reverzibilní ani po ukončení podávání léku.
OPATŘENÍ
Protože tobolky danazolu mohou způsobit určitý stupeň retence tekutin, stavy, které mohou být ovlivněny tímto faktorem, jako je epilepsie, migréna nebo srdeční nebo renální dysfunkce, polycytémie a hypertenze, vyžadují pečlivé sledování. Používejte opatrně u pacientů s diabetes mellitus.
Vzhledem k tomu, že u pacientů léčených tobolkami danazolu byla hlášena dysfunkce jater projevující se mírným zvýšením hladin sérových transamináz, je třeba pravidelně provádět jaterní testy (viz VAROVÁNÍ a NEŽÁDOUCÍ REAKCE ).
Bylo hlášeno, že podávání danazolu 50 mg způsobuje exacerbaci projevů akutní intermitentní porfyrie (viz KONTRAINDIKACE ).
Je třeba zvážit laboratorní monitorování hematologického stavu.
Laboratorní testy
Léčba danazolem může interferovat s laboratorním stanovením testosteronu, androstendionu a dehydroepiandrosteronu. Mezi další metabolické události patří snížení globulinu vázajícího štítnou žlázu a T4 se zvýšeným vychytáváním T3, ale bez poruchy tyreotropního hormonu nebo indexu volného tyroxinu.
Karcinogeneze, mutageneze, zhoršení plodnosti
Současné údaje jsou nedostatečné pro posouzení karcinogenity danazolu.
Těhotenství Teratogenní účinky
(vidět KONTRAINDIKACE .) Danazol 50 mg podávaný perorálně březím potkanům od 6. do 15. dne březosti v dávkách až 250 mg/kg/den (7-15násobek lidské dávky) nevedl k embryotoxicitě nebo teratogenitě vyvolané léčivem ani k rozdílům ve vrhu velikost, životaschopnost nebo hmotnost potomků ve srovnání s kontrolami. U králíků vedlo podávání danazolu 200 mg 6. až 18. den březosti v dávkách 60 mg/kg/den a vyšších (2-4násobek dávky pro člověka) k inhibici vývoje plodu.
Kojící matky
(vidět KONTRAINDIKACE .)
Pediatrické použití
Bezpečnost a účinnost u pediatrických pacientů nebyla stanovena.
Geriatrické použití
Klinické studie tobolek danazolu nezahrnovaly dostatečný počet subjektů ve věku 65 let a více, aby bylo možné určit bezpečnost a účinnost přípravku Danocrine u starších pacientů.
PŘEDÁVKOVAT
Nebyly poskytnuty žádné informace
KONTRAINDIKACE
Danazol 50 mg tobolky by neměly být podávány pacientům s:
KLINICKÁ FARMAKOLOGIE
Danazol potlačuje osu hypofýza-ovariální. Tato suprese je pravděpodobně kombinací snížené hypotalamo-hypofyzární reakce na sníženou produkci estrogenu, změnu metabolismu pohlavních steroidů a interakci danazolu s receptory pohlavních hormonů. Jediným dalším prokazatelným hormonálním účinkem je slabá androgenní aktivita. Danazol 50 mg snižuje produkci folikuly stimulujícího hormonu (FSH) a luteinizačního hormonu (LH).
Nedávné důkazy naznačují přímý inhibiční účinek na gonadálních místech a vazbu danazolu na receptory gonadálních steroidů v cílových orgánech. Kromě toho bylo prokázáno, že danazol 50 mg významně snižuje hladiny IgG, IgM a IgA, stejně jako fosfolipidové a izotopové autoprotilátky IgG u pacientek s endometriózou a souvisejícím zvýšením autoprotilátek, což naznačuje, že by to mohl být další mechanismus, kterým usnadňuje regresi onemocnění. .
Při léčbě endometriózy danazol mění normální a ektopickou tkáň endometria tak, že se stává inaktivní a atrofická. K úplnému vyřešení endometriálních lézí dochází ve většině případů.
Změny vaginální cytologie a cervikálního hlenu odrážejí supresivní účinek danazolu na osu hypofýza-ovariální.
Mohou se objevit změny v menstruačním cyklu.
Obecně je hypofyzární supresivní účinek danazolu 200 mg reverzibilní. Po ukončení léčby danazolem 100 mg se ovulace a cyklické krvácení obvykle vrátí do 60 až 90 dnů.
Při léčbě hereditárního angioedému danazol v účinných dávkách zabraňuje atakám onemocnění charakterizovaného epizodickým edémem břišních útrob, končetin, obličeje a dýchacích cest, který může být invalidizující, a pokud jsou postiženy dýchací cesty, smrtelný. Kromě toho danazol 100 mg částečně nebo úplně koriguje primární biochemickou abnormalitu hereditárního angioedému zvýšením hladin deficitního inhibitoru C1 esterázy (C1El). V důsledku tohoto působení se také zvyšují sérové hladiny složky C4 komplementového systému.
Farmakokinetika
Vstřebávání
Po perorálním podání dávky 400 mg zdravým dobrovolníkům mužského pohlaví je maximálních plazmatických koncentrací danazolu dosaženo za 2 až 8 hodin, s mediánem hodnoty Tmax 4 hodiny. Podmínky ustáleného stavu jsou pozorovány po 6 dnech podávání danazolu 100 mg tobolky dvakrát denně.
Farmakokinetické parametry pro danazol 100 mg tobolky po podání 400 mg perorální dávky zdravým mužům jsou shrnuty v následující tabulce:
Farmakokinetické parametry tobolek danazolu po perorálním podání jednotlivých dávek 100, 200 a 400 mg zdravým dobrovolnicím jsou shrnuty v následující tabulce:
Dávková úměrnost
Studie biologické dostupnosti ukazují, že hladiny v krvi se nezvyšují proporcionálně se zvyšováním podávané dávky.
Podání jedné dávky tobolek danazolu zdravým dobrovolnicím zjistilo, že 4násobné zvýšení dávky vedlo pouze k 1,6násobnému a 2,5násobnému zvýšení AUC a 1,3násobnému a 2,2násobnému zvýšení Cmax nalačno a po jídle. Podobný stupeň neproporcionality dávky byl pozorován v ustáleném stavu.
Food Effect
Podání jednorázové dávky 100 mg a 200 mg tobolek danazolu dobrovolnicím prokázalo, že jak rozsah dostupnosti, tak maximální plazmatická koncentrace se po jídle (> 30 gramů tuku) zvýšily 3 až 4krát, v tomto pořadí, ve srovnání s postní stav. Kromě toho jídlo také zpozdilo střední čas k dosažení maximální koncentrace danazolu o přibližně 30 minut. Dokonce i po vícenásobném dávkování za méně extrémních podmínek jídla/půstu zůstal přibližně 2 až 2,5násobný rozdíl v biologické dostupnosti mezi stavy nasycení a nalačno.
Rozdělení
Danazol 100 mg je lipofilní a může se rozdělit do buněčných membrán, což ukazuje na pravděpodobnost distribuce do hlubokých tkáňových kompartmentů.
Metabolismus A Vylučování
Zdá se, že danazol 200 mg je metabolizován a metabolity jsou eliminovány ledvinami a stolicí. Dva primární metabolity vylučované močí jsou 2-hydroxymethyldanazol 50 mg a ethisteron. Ve výkalech bylo identifikováno nejméně deset různých produktů.
Hlášený poločas eliminace danazolu 100 mg se napříč studiemi liší. Průměrný poločas danazolu u zdravých mužů je 9,7 hodiny. Po 6 měsících podávání 200 mg třikrát denně pacientkám s endometriózou byl poločas danazolu hlášen jako 23,7 hodin.
INFORMACE PRO PACIENTA
Nebyly poskytnuty žádné informace. Podívejte se prosím na VAROVÁNÍ a OPATŘENÍ sekce.
