Imdur 40mg, 20mg, 30mg, 60mg Isosorbide Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Imdur 30 mg a jak se používá?
Imdur 30 mg je lék na předpis používaný k léčbě příznaků bolesti na hrudi (angina pectoris). Imdur 30 mg lze užívat samostatně nebo s jinými léky.
Imdur 20 mg patří do třídy léků nazývaných nitráty, angína.
Není známo, zda je přípravek Imdur 60 mg bezpečný a účinný u dětí.
Jaké jsou možné vedlejší účinky přípravku Imdur?
Nežádoucí účinky přípravku Imdur zahrnují:
- mdloby,
- rychlý, nepravidelný nebo bušící srdeční tep,
- vyrážka,
- svědění,
- otok v obličeji, jazyku a krku,
- silné závratě a
- potíže s dýcháním
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější nežádoucí účinky přípravku Imdur 30 mg patří:
- bolest hlavy,
- závrať,
- závratě a
- nevolnost
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky přípravku Imdur. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
POPIS
Isosorbidmononitrát (ISMN), organický nitrát a hlavní biologicky aktivní metabolit isosorbiddinitrátu (ISDN), je vazodilatátor s účinky na tepny i žíly.
Tablety IMDUR® pro perorální podání obsahují buď 30 mg, 60 mg nebo 120 mg isosorbidmononitrátu ve formulaci s prodlouženým uvolňováním. Kromě toho každá tableta obsahuje následující neaktivní složky: koloidní oxid křemičitý, hydrogenovaný ricinový olej, hypromelóza, monohydrát laktózy, magnesium-stearát, mikrokrystalická celulóza a mastek.
Molekulární vzorec ISMN je C6H9NO6 a molekulová hmotnost je 191,14. Chemický název pro ISMN je 1,4:3,6-dianhydro-,D-glucitol-5-nitrát; sloučenina má následující strukturní vzorec:
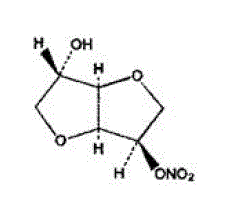
ISMN je bílá krystalická sloučenina bez zápachu, která je stabilní na vzduchu a v roztoku, má teplotu tání asi 90 °C a optickou rotaci +144 ° (2 % ve vodě, 20 °C).
Isosorbidmononitrát je volně rozpustný ve vodě, ethanolu, methanolu, chloroformu, ethylacetátu a dichlormethanu.
INDIKACE
Tablety IMDUR jsou indikovány k prevenci anginy pectoris způsobené onemocněním koronárních tepen. Nástup účinku perorálního isosorbidmononitrátu není dostatečně rychlý na to, aby byl tento přípravek užitečný při přerušení akutní anginózní epizody.
DÁVKOVÁNÍ A PODÁVÁNÍ
Doporučená počáteční dávka tablet IMDUR je 30 mg (podaná jako jedna 30mg tableta nebo jako 1/2 60mg tablety) nebo 60 mg (podaná jako jedna tableta) jednou denně. Po několika dnech může být dávka zvýšena na 120 mg (podaná jako jedna 120 mg tableta nebo dvě 60 mg tablety) jednou denně. Vzácně může být zapotřebí 240 mg. Denní dávka tablet IMDUR by se měla užívat ráno po vstávání. Tablety s prodlouženým uvolňováním IMDUR se nemají žvýkat ani drtit a měly by se spolknout spolu s půl sklenicí tekutiny. Tabletu 30 mg nelámejte.
JAK DODÁVÁNO
IMDUR tablety s prodlouženým uvolňováním 30 mg jsou bílé tablety ve tvaru tobolky s půlicí rýhou na jedné straně a vyraženým „IMDUR“ na straně bez půlicí rýhy. Dodávají se následovně:
Láhve po 100 NDC 0085-1374-01
IMDUR tablety s prodlouženým uvolňováním 60 mg jsou bílé tablety ve tvaru tobolky s půlicí rýhou na jedné straně s quot;60-60" a vyraženým "IMDUR" na straně bez rýhy. Dodávají se následovně:
Láhve po 100 NDC 0085-2028-01
IMDUR 30 mg tablety s prodlouženým uvolňováním 120 mg jsou bílé tablety ve tvaru tobolky s vyrytým „IMDUR“ na jedné straně a „120“ na druhé straně. Dodávají se následovně:
Láhve po 100 NDC 0085-0091-01
Skladujte při kontrolované pokojové teplotě 20°-25°C (68°-77°F) [Viz USP].
Výrobce: Kremers urban pharmaceuticals inc, seymour,IN47274,USA. Revize: prosinec 2010
VEDLEJŠÍ EFEKTY
Níže uvedená tabulka ukazuje četnosti nežádoucích účinků, které se vyskytly u >5 % subjektů ve třech placebem kontrolovaných severoamerických studiích, ve kterých pacienti v rameni s aktivní léčbou dostávali 30 mg, 60 mg, 120 mg nebo 240 mg isosorbidu mononitrát jako IMDUR 60 mg tablety jednou denně. V závorce stejná tabulka uvádí frekvence, se kterými byly tyto nežádoucí účinky spojeny s přerušením léčby. Celkově 8 % pacientů, kteří dostávali 30 mg, 60 mg, 120 mg nebo 240 mg isosorbidmononitrátu ve třech placebem kontrolovaných severoamerických studiích, přerušilo léčbu kvůli nežádoucím účinkům. Většina z nich byla přerušena kvůli bolesti hlavy. Závratě byly zřídka spojeny s vyřazením z těchto studií. Protože se zdá, že bolest hlavy je nežádoucím účinkem závislým na dávce a má tendenci mizet s pokračující léčbou, doporučuje se zahájit léčbu přípravkem IMDUR v nízkých dávkách po dobu několika dní, než se zvýší na požadovanou úroveň.
ČETNOST A NEŽÁDOUCÍ UDÁLOSTI (UKONČENO) *
Kromě toho byly tři severoamerické studie spojeny s 11 kontrolovanými studiemi provedenými v Evropě. Mezi 14 kontrolovanými studiemi bylo celkem 711 pacientů randomizováno k užívání tablet IMDUR. Když byly shromážděné údaje přezkoumány, bolest hlavy a závratě byly jedinými nežádoucími účinky, které byly hlášeny u >5 % pacientů. Další nežádoucí příhody, každou hlášenou ≤ 5 % exponovaných pacientů a v mnoha případech nejistého vztahu k léčbě drogami, byly:
Poruchy autonomního nervového systému : Sucho v ústech, návaly horka.
Tělo jako celek : Astenie, bolest zad, bolest na hrudi, edém, únava, horečka, příznaky podobné chřipce, malátnost, ztuhlost.
Kardiovaskulární poruchy, obecné : Srdeční selhání, hypertenze, hypotenze.
Poruchy centrálního a periferního nervového systému : Závratě, bolest hlavy, hypoestézie, migréna, neuritida, paréza, parestézie, ptóza, třes, vertigo.
Poruchy gastrointestinálního systému Bolesti břicha, zácpa, průjem, dyspepsie, plynatost, žaludeční vřed, gastritida, glositida, hemoragický žaludeční vřed, hemoroidy, řídká stolice, meléna, nevolnost, zvracení.
Poruchy sluchu a vestibulární poruchy : Bolest ucha, tinitus, perforace bubínku.
Poruchy srdeční frekvence a rytmu : Arytmie, arytmie síní, fibrilace síní, bradykardie, blokáda raménka, extrasystola, palpitace, tachykardie, ventrikulární tachykardie.
Poruchy jater a žlučového systému : zvýšení SGOT, zvýšení SGPT.
Metabolické a nutriční poruchy : Hyperurikémie, hypokalémie.
Poruchy pohybového aparátu : Artralgie, zmrzlé rameno, svalová slabost, muskuloskeletální bolest, myalgie, myositida, porucha šlach, torticollis.
Myo-, endo-, perikardiální a chlopňové poruchy : Zhoršení anginy pectoris, srdeční šelest, abnormální srdeční zvuk, infarkt myokardu, abnormalita Q vlny.
Poruchy krevních destiček, krvácení a srážlivosti : Purpura, trombocytopenie.
Psychiatrické poruchy Úzkost, poruchy koncentrace, zmatenost, snížené libido, deprese, impotence, nespavost, nervozita, paronirie, somnolence.
Porucha červených krvinek : Hypochromní anémie.
Poruchy reprodukce, ženy : Atrofická vaginitida, bolest prsou.
Poruchy mechanismu odolnosti : Bakteriální infekce, moniliáza, virová infekce.
Poruchy dýchacího systému : Bronchitida, bronchospasmus, kašel, dušnost, zvýšené sputum, nazální kongesce, faryngitida, pneumonie, plicní infiltrace, chrochtání, rýma, sinusitida.
Poruchy kůže a příloh : Akné, abnormální struktura vlasů, zvýšené pocení, pruritus, vyrážka, kožní uzlík.
Poruchy močového systému : Polyurie, ledvinový kámen, infekce močových cest.
Cévní (extrakardiální) poruchy : Zrudnutí, intermitentní klaudikace, bércové vředy, křečové žíly.
Poruchy zraku : Konjunktivitida, fotofobie, abnormální vidění.
Kromě toho byly během uvádění isosorbidmononitrátu na trh hlášeny následující spontánní nežádoucí účinky: synkopa.

DROGOVÉ INTERAKCE
Vazodilatační účinky isosorbidmononitrátu mohou být aditivní s účinky jiných vazodilatátorů. Bylo zjištěno, že zejména alkohol vykazuje aditivní účinky této odrůdy.
Při kombinaci blokátorů kalciových kanálů a organických nitrátů byla hlášena výrazná symptomatická ortostatická hypotenze. Může být nutné upravit dávkování obou skupin látek.
Interakce drog/laboratorních testů
Dusičnany a dusitany mohou interferovat s barevnou reakcí Zlatkis-Zak a způsobit falešně nízké hodnoty při stanovení cholesterolu v séru.
VAROVÁNÍ
Zesílení vazodilatačních účinků IMDUR sildenafilem může vést k těžké hypotenzi. Časový průběh a závislost této interakce na dávce nebyly studovány. Vhodná podpůrná péče nebyla studována, ale zdá se rozumné považovat to za předávkování nitráty s elevací končetin a centrální expanzí objemu.
Přínosy ISMN u pacientů s akutním infarktem myokardu nebo městnavým srdečním selháním nebyly stanoveny; protože je obtížné rychle ukončit účinky isosorbidmononitrátu, tento lék se v těchto podmínkách nedoporučuje.
Je-li za těchto stavů použit isosorbidmononitrát, musí být provedeno pečlivé klinické nebo hemodynamické monitorování, aby se zabránilo riziku hypotenze a tachykardie.
OPATŘENÍ
Všeobecné
Těžká hypotenze, zejména při vzpřímeném držení těla, se může objevit i při malých dávkách isosorbidmononitrátu. Tento lék by proto měl být používán s opatrností u pacientů, kteří mohou mít depleci objemu nebo kteří z jakéhokoli důvodu již mají hypotenzi. Hypotenze vyvolaná isosorbidmononitrátem může být doprovázena paradoxní bradykardií a zvýšenou anginou pectoris.
Léčba nitráty může zhoršit anginu pectoris způsobenou hypertrofickou kardiomyopatií.
U průmyslových pracovníků, kteří byli dlouhodobě vystaveni neznámým (pravděpodobně vysokým) dávkám organických dusičnanů, se jasně vyskytuje tolerance. Během dočasného vysazení dusičnanů těmto pracovníkům se vyskytly bolesti na hrudi, akutní infarkt myokardu a dokonce náhlá smrt, což dokazuje existenci skutečné fyzické závislosti. Význam těchto pozorování pro rutinní klinické použití perorálního isosorbidmononitrátu není znám.
Karcinogeneze, mutageneze, zhoršení plodnosti
Nebyly pozorovány žádné důkazy karcinogenity u potkanů vystavených izosorbidmononitrátu ve stravě v dávkách až 900 mg/kg/den po dobu prvních 6 měsíců a 500 mg/kg/den po zbývající dobu trvání studie, ve které byla podávána dávka samcům po dobu až 121 týdnů a samice byly podávány po dobu až 137 týdnů. U myší vystavených izosorbidmononitrátu ve stravě po dobu až 104 týdnů v dávkách až 900 mg/kg/den nebyl pozorován žádný důkaz karcinogenity.
Isosorbidmononitrát nevytvářel genové mutace (Amesův test, test myšího lymfomu) ani chromozomové aberace (testy na lidských lymfocytech a myších mikronukleech) v biologicky relevantních koncentracích.
Žádné účinky na fertilitu nebyly pozorovány ve studii, ve které byly samcům a samicím potkanů podávány dávky až 750 mg/kg/den počínaje, u samců 9 týdnů před pářením a u samic 2 týdny před pářením.
Těhotenství
Teratogenní účinky
Těhotenství kategorie B
Ve studiích určených k detekci účinků isosorbidmononitrátu na embryofetální vývoj nebyly dávky až 240 nebo 248 mg/kg/den podávané březím potkanům a králíkům spojeny s důkazy takových účinků. Tyto dávky pro zvířata jsou asi 100krát vyšší než maximální doporučená dávka pro člověka (120 mg u 50 kg ženy), pokud je srovnání založeno na tělesné hmotnosti; když je srovnání založeno na ploše povrchu těla, je dávka pro potkana přibližně 17krát vyšší než dávka pro člověka a dávka pro králíka přibližně 38krát vyšší než dávka pro člověka. Neexistují však žádné adekvátní a dobře kontrolované studie u těhotných žen. Vzhledem k tomu, že reprodukční studie na zvířatech ne vždy předpovídají lidskou odpověď, měly by být tablety IMDUR během těhotenství používány pouze tehdy, je-li to nezbytně nutné.
Neteratogenní účinky
Přežití a vývoj novorozenců a výskyt mrtvě narozených dětí byly nepříznivě ovlivněny, když byly březím potkanům podávány perorální dávky 750 (ale ne 300) mg isosorbidmononitrátu/kg/den během pozdní březosti a laktace. Tato dávka (přibližně 312násobek dávky pro člověka, pokud je srovnání založeno na tělesné hmotnosti a 54násobek dávky pro člověka, pokud je srovnání založeno na ploše povrchu těla) byla spojena se snížením přírůstku hmotnosti matky a motorické aktivity a důkazem zhoršené laktace.
Kojící matky
Není známo, zda se tento lék vylučuje do lidského mléka. Vzhledem k tomu, že mnoho léků se vylučuje do mateřského mléka, je třeba opatrnosti při podávání ISMN kojící matce.
Pediatrické použití
Bezpečnost a účinnost ISMN u pediatrických pacientů nebyla stanovena.
Geriatrické použití
Klinické studie s tabletami IMDUR 60 mg neobsahovaly dostatečné informace o pacientech ve věku 65 a více let, aby bylo možné určit, zda reagují odlišně od mladších pacientů. Jiné hlášené klinické zkušenosti s IMDUR 20 mg nezjistily rozdíly v odpovědi mezi staršími a mladšími pacienty. Klinické zkušenosti s organickými nitráty uváděnými v literatuře identifikovaly potenciál pro těžkou hypotenzi a zvýšenou citlivost na nitráty u starších osob. Obecně by měl být výběr dávky pro staršího pacienta opatrný, obvykle začínající na spodní hranici dávkovacího rozmezí, což odráží vyšší frekvenci snížené funkce jater, ledvin nebo srdce a souběžného onemocnění nebo jiné lékové terapie.
Starší pacienti mohou mít sníženou funkci baroreceptorů a může se u nich rozvinout závažná ortostatická hypotenze, pokud jsou používány vazodilatátory. IMDUR 60 mg by se proto měl používat s opatrností u starších pacientů, kteří mohou mít depleci objemu, užívají více léků nebo kteří z jakéhokoli důvodu již mají hypotenzi. Hypotenze vyvolaná isosorbidmononitrátem může být doprovázena paradoxní bradykardií a zvýšenou anginou pectoris.
Starší pacienti mohou být náchylnější k hypotenzi a mohou mít větší riziko pádu při terapeutických dávkách nitroglycerinu.
Léčba nitráty může zhoršit anginu pectoris způsobenou hypertrofickou kardiomyopatií, zejména u starších osob.
PŘEDÁVKOVAT
Hemodynamické účinky
Špatné účinky předávkování isosorbidmononitrátem jsou obecně výsledkem schopnosti isosorbidmononitrátu vyvolat vazodilataci, žilní hromadění, snížený srdeční výdej a hypotenzi. Tyto hemodynamické změny mohou mít proteinové projevy, včetně zvýšeného intrakraniálního tlaku, s některými nebo všemi přetrvávajícími pulzujícími bolestmi hlavy, zmateností a střední horečkou; vertigo, bušení srdce; zrakové poruchy; nevolnost a zvracení (možná s kolikou a dokonce krvavým průjmem); synkopa (zejména ve vzpřímeném držení těla); hlad po vzduchu a dušnost, později následované sníženým ventilačním úsilím; pocení s kůží buď zarudlou, nebo studenou a vlhkou; srdeční blok a bradykardie; ochrnutí; kóma; záchvaty a smrt.
Laboratorní stanovení sérových hladin isosorbidmononitrátu a jeho metabolitů nejsou široce dostupná a taková stanovení v žádném případě nemají žádnou zavedenou roli v léčbě předávkování isosorbidmononitrátem.
Neexistují žádné údaje naznačující, jaká dávka isosorbidmononitrátu je pravděpodobně život ohrožující u lidí. U potkanů a myší existuje významná letalita při dávkách 2000 mg/kg a 3000 mg/kg, v daném pořadí.
Nejsou k dispozici žádné údaje, které by naznačovaly fyziologické manévry (např. manévry ke změně pH moči), které by mohly urychlit eliminaci isosorbidmononitrátu. Zejména je známo, že dialýza je neúčinná při odstraňování isosorbidmononitrátu z těla.
Není znám žádný specifický antagonista vazodilatačních účinků isosorbidmononitrátu a žádná intervence Není znám žádný specifický antagonista vazodilatačních účinků isosorbidmononitrátu a žádná intervence nebyla předmětem kontrolované studie jako terapie předávkování isosorbidmononitrátem. Vzhledem k tomu, že hypotenze spojená s předávkováním isosorbidmononitrátem je výsledkem venodilatace a arteriální hypovolemie, měla by v této situaci směřovat obezřetná léčba ke zvýšení objemu centrální tekutiny. Pasivní elevace nohou pacienta může být dostačující, ale může být také nutná intravenózní infuze normálního fyziologického roztoku nebo podobné tekutiny.
Použití epinefrinu nebo jiných arteriálních vazokonstriktorů v tomto prostředí pravděpodobně způsobí více škody než užitku.
pacientů s onemocněním ledvin nebo městnavým srdečním selháním není léčba vedoucí k expanzi centrálního objemu bez rizika. Léčba předávkování isosorbidmononitrátem u těchto pacientů může být jemná a obtížná a může být nutné invazivní sledování.
Methemoglobinémie
Methemoglobinémie byla hlášena u pacientů užívajících jiné organické nitráty a pravděpodobně by se také mohla objevit jako vedlejší účinek isosorbidmononitrátu. Nepochybně dusičnanové ionty uvolněné během metabolismu isosorbidmononitrátu mohou oxidovat hemoglobin na methemoglobin. I u pacientů zcela bez aktivity cytochrom b reduktázy, a dokonce i za předpokladu, že nitrátová část isosorbidmononitrátu je kvantitativně aplikována na oxidaci hemoglobinu, by mělo být zapotřebí asi 2 mg/kg isosorbidmononitrátu, než se u kteréhokoli z těchto pacientů projeví klinicky signifikantní ( ≥10%) methemoglobinémie. U pacientů s normální funkcí reduktázy by významná produkce methemoglobinu měla vyžadovat ještě vyšší dávky isosorbidmononitrátu. V jedné studii, ve které 36 pacientů dostávalo 2–4 týdny kontinuální terapie nitroglycerinem v dávce 3,1 až 4,4 mg/h (ekvivalent, v celkové podané dávce dusičnanových iontů, 7,8–11,1 mg isosorbidmononitrátu za hodinu), byla průměrná hladina methemoglobinu naměřeno bylo 0,2 %; to bylo srovnatelné s tím, co bylo pozorováno u paralelních pacientů, kteří dostávali placebo.
Bez ohledu na tato pozorování existují kazuistiky významné methemoglobinemie ve spojení s mírným předávkováním organickými nitráty. Žádný z postižených pacientů nebyl považován za neobvykle vnímavý.
Hladiny methemoglobinu jsou dostupné ve většině klinických laboratoří. Diagnóza by měla být podezřelá u pacientů, kteří vykazují známky zhoršené dodávky kyslíku i přes dostatečný srdeční výdej a adekvátní arteriální pO2. Klasicky je methemoglobinemická krev popsána jako čokoládově hnědá bez změny barvy při vystavení vzduchu. Když je diagnostikována methemoglobinémie, léčbou volby je methylenová modř, 1-2 mg/kg intravenózně.
KONTRAINDIKACE
Tablety IMDUR 20 mg jsou kontraindikovány u pacientů, u kterých se projevila přecitlivělost nebo idiosynkratické reakce na jiné nitráty nebo dusitany.
KLINICKÁ FARMAKOLOGIE
Mechanismus působení
Produkt IMDUR je perorální formulace s prodlouženým uvolňováním ISMN, hlavního aktivního metabolitu isosorbiddinitrátu; většinu klinické aktivity dinitrátu lze připsat mononitrátu.
Hlavním farmakologickým účinkem ISMN a všech organických nitrátů obecně je relaxace hladkého svalstva cév, což vede k dilataci periferních tepen a žil, zejména těch druhých. Dilatace žil podporuje periferní shromažďování krve, snižuje žilní návrat do srdce, čímž snižuje enddiastolický tlak levé komory a tlak v zaklínění plicnice (preload). Arteriolární relaxace snižuje systémový vaskulární odpor, systolický arteriální tlak a střední arteriální tlak (afterload). Dochází také k dilataci koronárních tepen. Relativní význam snížení preloadu, afterloadu a koronární dilatace zůstává nedefinovaný.
Farmakodynamika
Dávkovací režimy pro většinu chronicky užívaných léků jsou navrženy tak, aby poskytovaly plazmatické koncentrace, které jsou trvale vyšší než minimální účinná koncentrace. Tato strategie je nevhodná pro organické dusičnany. Několik dobře kontrolovaných klinických studií použilo zátěžové testování k posouzení antianginózní účinnosti kontinuálně podávaných nitrátů. Ve velké většině těchto studií byly účinné látky k nerozeznání od placeba po 24 hodinách (nebo méně) nepřetržité terapii. Pokusy překonat toleranci zvyšováním dávek, dokonce i na dávky daleko převyšující ty akutně užívané, soustavně selhaly. Teprve poté, co byly dusičnany v těle několik hodin nepřítomné, byla obnovena jejich antianginózní účinnost. Tablety IMDUR při dlouhodobém užívání po dobu 42 dnů v dávce 120 mg jednou denně pokračovaly ve zlepšování výkonu při cvičení po 4 hodinách a 12 hodinách po podání, ale jeho účinky (ačkoli lepší než u placeba) jsou menší nebo v nejlepším případě rovné účinky první dávky 60 mg.
Farmakokinetika a metabolismus
Po perorálním podání ISMN ve formě roztoku nebo tablet s okamžitým uvolňováním je maximálních plazmatických koncentrací ISMN dosaženo za 30 až 60 minut, s absolutní biologickou dostupností přibližně 100 %. Po intravenózním podání je ISMN distribuován do celkové tělesné vody přibližně za 9 minut s distribučním objemem přibližně 0,6-0,7 l/kg. Isosorbidmononitrát se přibližně z 5 % váže na lidské plazmatické proteiny a je distribuován do krevních buněk a slin. Isosorbidmononitrát je primárně metabolizován v játrech, ale na rozdíl od perorálního isosorbiddinitrátu nepodléhá first-pass metabolismu. Isosorbidmononitrát je vylučován denitrací na isosorbid a glukuronidací jako mononitrát, přičemž 96 % podané dávky se vylučuje močí během 5 dnů a pouze asi 1 % se vylučuje stolicí. V moči bylo detekováno nejméně šest různých sloučenin, přičemž asi 2 % dávky se vyloučily jako nezměněné léčivo a nejméně pět metabolitů. Metabolity nejsou farmakologicky aktivní. Renální clearance tvoří pouze asi 4 % celkové tělesné clearance. Průměrný plazmatický eliminační poločas ISMN je přibližně 5 hodin.
Byla hodnocena dispozice ISMN u pacientů s různým stupněm renální insuficience, jaterní cirhózou nebo srdeční dysfunkcí a bylo zjištěno, že je podobné jako u zdravých subjektů. Eliminační poločas ISMN nebyl prodloužen a u pacientů s chronickým selháním ledvin po opakovaném perorálním podání nedošlo k žádné akumulaci léku.
Farmakokinetika a/nebo biologická dostupnost přípravku IMDUR 40 mg tablety byla studována jak u normálních dobrovolníků, tak u pacientů po podání jedné a více dávek. Údaje z těchto studií naznačují, že farmakokinetika ISMN podávaného jako tablety IMDUR je podobná mezi normálními zdravými dobrovolníky a pacienty s anginou pectoris. Ve studiích s jednorázovou a opakovanou dávkou byla farmakokinetika ISMN úměrná dávce mezi 30 mg a 240 mg.
Ve studii s opakovanými dávkami byl hodnocen vliv věku na farmakokinetický profil IMDUR 60 mg a 120 mg (2 × 60 mg) u subjektů ≥ 45 let. Výsledky této studie ukazují, že neexistují žádné významné rozdíly v žádné z farmakokinetických proměnných ISMN mezi staršími (≥65 let) a mladšími jedinci (45–64 let) pro dávku IMDUR 60 mg. Podávání tablet IMDUR 120 mg (2 × 60 mg tablety každých 24 hodin po dobu 7 dnů) vyvolalo zvýšení Cmax a AUC úměrné dávce, beze změn Tmax nebo terminálního poločasu. Starší skupina (65-74 let) vykazovala o 30 % nižší zdánlivou perorální clearance (Cl/F) po vyšší dávce, tj. 120 mg, ve srovnání s mladší skupinou (45-64 let); Cl/F se mezi těmito dvěma skupinami po režimu 60 mg nelišil. Zatímco u mladší skupiny byl Cl/F nezávislý na dávce, starší skupina vykazovala mírně nižší Cl/F po režimu 120 mg ve srovnání s režimem 60 mg. Rozdíly mezi těmito dvěma věkovými skupinami však nebyly statisticky významné. Ve stejné studii ženy vykazovaly mírné (15 %) snížení clearance, když byla dávka zvýšena. Ženy vykazovaly vyšší AUC a Cmax ve srovnání s muži, ale tyto rozdíly byly způsobeny rozdíly v tělesné hmotnosti mezi těmito dvěma skupinami. Když byla data analyzována s použitím věku jako proměnné, výsledky ukázaly, že nebyly žádné významné rozdíly v žádné z farmakokinetických proměnných ISMN mezi staršími (≥65 let) a mladšími jedinci (45-64 let). Na výsledky této studie je však třeba nahlížet s opatrností vzhledem k malému počtu subjektů v každé věkové podskupině a následně i nedostatku dostatečné statistické síly.
Následující tabulka shrnuje klíčové farmakokinetické parametry ISMN po jednorázovém a opakovaném podání ISMN jako perorálního roztoku nebo tablet IMDUR:
Účinky jídla
Vliv potravy na biologickou dostupnost ISMN po podání jedné dávky tablet IMDUR 60 mg byl hodnocen ve třech různých studiích zahrnujících buď „lehkou“ snídani, nebo vysokokalorickou snídani s vysokým obsahem tuku. Výsledky těchto studií ukazují, že současný příjem potravy může snížit rychlost (zvýšení Tmax), ale ne rozsah (AUC) absorpce ISMN.
Klinické testy
Kontrolované studie s tabletami IMDUR prokázaly antianginózní aktivitu po akutním a chronickém podávání. Podávání IMDUR 40 mg tablety jednou denně, užívané brzy ráno při vstávání, zajistilo alespoň 12 hodin antianginózního účinku.
placebem kontrolované paralelní studii bylo podáváno 30, 60, 120 a 240 mg tablet IMDUR 60 mg jednou denně po dobu až 6 týdnů. Před randomizací všichni pacienti dokončili 1- až 3týdenní jednoduše zaslepenou placebovou fázi, aby prokázali schopnost reagovat na dusičnany a celkovou reprodukovatelnost doby cvičení na běžícím pásu. Testy tolerance zátěže za použití Bruceova protokolu byly provedeny před a 4 a 12 hodin po ranní dávce ve dnech 1, 7, 14, 28 a 42 dvojitě zaslepeného období. IMDUR 60 mg tablety 30 a 60 mg (pouze dávky vyhodnocené akutně) prokázaly významné zvýšení celkové doby běhu na běžícím pásu oproti výchozí hodnotě ve srovnání s placebem za 4 a 12 hodin po podání první dávky. V den 42 prokázala dávka 120 a 240 mg tablet IMDUR 40 mg signifikantní prodloužení celkového času na běžícím pásu 4 a 12 hodin po podání, ale 42. den již nebyly dávky 30 a 60 mg odlišitelné od placeba. Během chronického podávání nebyl rebound fenomén pozorován v žádné skupině léčené IMDUR.
Shromážděné údaje ze dvou dalších studií, porovnávající IMDUR 40 mg tablety 60 mg jednou denně, ISDN 30 mg QID a placebo QID u pacientů s chronickou stabilní anginou pectoris pomocí randomizovaného, dvojitě zaslepeného, třícestného zkříženého designu, zjistily statisticky významné zvýšení tolerance zátěže časů pro tablety IMDUR 20 mg ve srovnání s placebem ve 4., 8. a 12. hodině a s ISDN v hodině 4. Zvýšení tolerance zátěže v den 14, i když statisticky významné ve srovnání s placebem, bylo přibližně poloviční ve srovnání s pozorovaným v den 1 studie .
INFORMACE PRO PACIENTA
Pacienti by měli být informováni, že antianginózní účinnost přípravku IMDUR 60 mg tablety lze udržet pečlivým dodržováním předepsaného dávkovacího schématu. U většiny pacientů toho lze dosáhnout tím, že si dávku vezmou hned, jak vstanou.
Stejně jako u jiných nitrátů, denní bolesti hlavy někdy doprovázejí léčbu isosorbidmononitrátem. U pacientů, kteří dostanou tyto bolesti hlavy, jsou bolesti hlavy markerem aktivity léku. Pacienti by měli odolat pokušení vyhnout se bolestem hlavy změnou schématu léčby isosorbidmononitrátem, protože ztráta bolesti hlavy může být spojena se současnou ztrátou antianginózní účinnosti. Aspirin nebo acetaminofen často úspěšně zmírňují bolesti hlavy vyvolané isosorbidmononitrátem bez škodlivého účinku na antianginózní účinnost isosorbidmononitrátu.
Léčba isosorbidmononitrátem může být spojena s točením hlavy ve stoje, zejména těsně po vstávání z lehu nebo sedu. Tento účinek může být častější u pacientů, kteří také konzumovali alkohol.
