Voltaren 100mg, 50mg Diclofenac Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Voltaren a jak se používá?
Voltaren se používá k léčbě příznaků bolesti spojené s revmatoidní artritidou, osteoartritidou, ankylozující spondylitidou, dysmenoreou a mírnou až střední bolestí. Voltaren 100 mg lze užívat samostatně nebo s jinými léky.
Voltaren patří do třídy léků nazývaných nesteroidní protizánětlivé léky (NSAID).
Jaké jsou možné vedlejší účinky přípravku Voltaren 50 mg?
Voltaren může způsobit závažné nežádoucí účinky včetně:
- bolest hlavy,
- hlad,
- pocení,
- podrážděnost,
- závrať,
- nevolnost,
- rychlý srdeční tep,
- pocit úzkosti nebo rozechvění,
- necitlivost nebo mravenčení v rukou, pažích, nohou nebo chodidlech,
- slabost v pažích, rukou, nohou nebo chodidlech,
- palčivá bolest paží, rukou, nohou nebo chodidel,
- vážné změny nálady nebo chování,
- nervozita,
- zmatek,
- míchání,
- paranoia,
- halucinace,
- problémy s pamětí,
- potíže se soustředěním,
- myšlenky na sebevraždu,
- ruptura šlachy,
- náhlá bolest,
- otok,
- modřiny,
- něha,
- ztuhlost,
- pohybové problémy,
- praskání nebo praskání v kterémkoli z vašich kloubů,
- silná bolest žaludku,
- průjem, který je vodnatý nebo krvavý,
- chvění v tvé hrudi,
- dušnost,
- vyrážka,
- dýchací problémy,
- záchvaty (křeče),
- silné bolesti hlavy,
- problémy se zrakem,
- bolest za očima,
- bolest v horní části žaludku,
- ztráta chuti k jídlu,
- tmavá moč,
- stolice hliněné barvy, a
- zežloutnutí kůže nebo očí (žloutenka)
a okamžitě vyhledejte lékařskou pomoc, pokud máte některý z výše uvedených příznaků.
Mezi nejčastější vedlejší účinky přípravku Voltaren patří:
- špatné trávení,
- plyn,
- bolest břicha,
- nevolnost,
- zvracení,
- průjem,
- zácpa,
- bolest hlavy,
- závrať,
- ospalost,
- ucpaný nos,
- svědění,
- zvýšené pocení,
- zvýšený krevní tlak a
- otoky nebo bolest paží nebo nohou
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky přípravku Voltaren. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
VAROVÁNÍ
HEPATOTOXICITA, kardiální toxicita, embryofetální toxicita
Kardiovaskulární trombotické příhody
- Nesteroidní protizánětlivé léky (NSAID) způsobují zvýšené riziko závažných kardiovaskulárních trombotických příhod, včetně infarktu myokardu a mrtvice, které mohou být fatální. Toto riziko se může objevit na začátku léčby a může se zvyšovat s délkou užívání (viz UPOZORNĚNÍ).
- VOLTAREN® je kontraindikován při operaci bypassu koronární artérie (CABG) (viz KONTRAINDIKACE, VAROVÁNÍ).
Gastrointestinální krvácení, ulcerace a perforace
- NSAID způsobují zvýšené riziko závažných gastrointestinálních (GI) nežádoucích příhod včetně krvácení, ulcerace a perforace žaludku nebo střev, které mohou být fatální. Tyto události se mohou objevit kdykoli během používání a bez varovných příznaků. Starší pacienti a pacienti s předchozí anamnézou peptického vředu a/nebo GI krvácení jsou vystaveni většímu riziku závažných GI příhod. (viz VAROVÁNÍ).
POPIS
VOLTAREN® (diclofenac sodný enterosolventní tablety) je derivát kyseliny benzenoctové. VOLTAREN 50 mg je dostupný ve formě tablet s opožděným uvolňováním (enterosolventní) po 75 mg (světle růžové) pro perorální podání. Diklofenak sodný je bílý nebo mírně nažloutlý krystalický prášek a je mírně rozpustný ve vodě při 25 °C. Chemický název je 2-[(2,6-dichlorfenyl)amino]benzenoctová kyselina, monosodná sůl. Molekulová hmotnost je 318,14. Jeho molekulový vzorec je C14H10Cl2NNaO2 a má následující strukturní vzorec
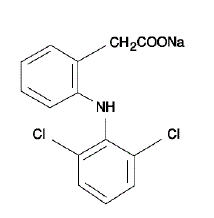
Neaktivní složky přípravku VOLTAREN zahrnují: hydroxypropylmethylcelulózu, oxid železitý, laktózu, stearát hořečnatý, kopolymer kyseliny methakrylové, mikrokrystalickou celulózu, polyethylenglykol, povidon, propylenglykol, hydroxid sodný, sodnou sůl glykolátu škrobu, mastek, oxid titaničitý.
INDIKACE
Než se rozhodnete použít VOLTAREN, pečlivě zvažte potenciální přínosy a rizika přípravku VOLTAREN® (diclofenac sodný enterosolventní tablety) a další možnosti léčby. Používejte nejnižší účinnou dávku po co nejkratší dobu v souladu s individuálními cíli léčby pacienta (viz VAROVÁNÍ ; Gastrointestinální krvácení , Ulcerace , a Perforace ).
VOLTAREN je indikován:
- pro úlevu od známek a příznaků osteoartrózy
- pro úlevu od známek a příznaků revmatoidní artritidy
- pro akutní nebo dlouhodobé použití k úlevě od známek a příznaků ankylozující spondylitidy
DÁVKOVÁNÍ A PODÁVÁNÍ
Než se rozhodnete použít VOLTAREN, pečlivě zvažte potenciální přínosy a rizika přípravku VOLTAREN® (diclofenac sodný enterosolventní tablety) a další možnosti léčby. Používejte nejnižší účinnou dávku po co nejkratší dobu v souladu s individuálními cíli léčby pacienta (viz VAROVÁNÍ ; Gastrointestinální krvácení, ulcerace a perforace ).
Po pozorování odpovědi na úvodní léčbu přípravkem VOLTAREN 100 mg je třeba upravit dávku a frekvenci tak, aby vyhovovaly individuálním potřebám pacienta.
Pro úlevu od osteoartrózy je doporučená dávka 100 až 150 mg/den v rozdělených dávkách (50 mg dvakrát denně nebo třikrát denně nebo 75 mg dvakrát denně).
Pro úlevu od revmatoidní artritidy je doporučená dávka 150 až 200 mg/den v rozdělených dávkách (50 mg třikrát denně nebo čtyřikrát denně nebo 75 mg dvakrát denně).
Pro úlevu od ankylozující spondylitidy je doporučená dávka 100 až 125 mg/den, podaná jako 25 mg čtyřikrát denně, s extra 25 mg dávkou před spaním, pokud je to nutné.
Různé formulace diklofenaku [VOLTAREN® (sodná sůl diklofenaku enterosolventně potažené tablety); VOLTAREN®ÂXR (tablety s prodlouženým uvolňováním sodné soli diklofenaku); CATAFLAM® (tablety s okamžitým uvolňováním diklofenaku draselného)] nejsou nutně bioekvivalentní, i když je síla v miligramech stejná.
JAK DODÁVÁNO
VOLTAREN® (entericky potahované tablety diklofenaku sodného) - 75 mg
Světle růžové, bikonvexní, enterosolventní tablety trojúhelníkového tvaru (černým inkoustem na jedné straně potištěno „VOLTAREN 75“)
Láhve po 100 NDC 0028-0264-01
Skladujte při pokojové teplotě 20 °C až 25 °C (68 °F až 77 °F); odchylky povolené mezi 15 °C a 30 °C (59 °F a 86 °F) [viz USP řízená pokojová teplota ].
Chraňte před vlhkostí. Dávkujte v těsné nádobě (USP).
Distribuce: Novartis Pharmaceuticals Corporation East Hanover, NJ 07936. Revize: duben 2021
VEDLEJŠÍ EFEKTY
Následující nežádoucí účinky jsou podrobněji popsány v jiných částech označení:
- Kardiovaskulární trombotické příhody (viz VAROVÁNÍ )
- GI krvácení, ulcerace a perforace (viz VAROVÁNÍ )
- Hepatotoxicita (viz VAROVÁNÍ )
- Hypertenze (viz VAROVÁNÍ )
- Srdeční selhání a edém (viz VAROVÁNÍ )
- Renální toxicita a hyperkalémie (viz VAROVÁNÍ )
- Anafylaktické reakce (viz VAROVÁNÍ )
- Závažné kožní reakce (viz VAROVÁNÍ )
- Hematologická toxicita (viz VAROVÁNÍ )
Zkušenosti z klinických studií
Vzhledem k tomu, že klinické studie jsou prováděny za velmi odlišných podmínek, nelze míry nežádoucích reakcí pozorované v klinických studiích léku přímo srovnávat s mírami v klinických studiích jiného léku a nemusí odrážet míry pozorované v praxi.
U pacientů užívajících VOLTAREN® (enterosolventní tablety se sodnou solí diklofenaku) nebo jiná NSAID jsou nejčastěji hlášenými nežádoucími účinky vyskytujícími se přibližně u 1 % až 10 % pacientů: Gastrointestinální zkušenosti, včetně: bolesti břicha, zácpy, průjmu, dyspepsie, plynatost, hrubé krvácení/perforace, pálení žáhy, nevolnost, GI vředy (žaludeční/duodenální) a zvracení.
Abnormální funkce ledvin, anémie, závratě, otoky, zvýšené jaterní enzymy, bolesti hlavy, zvýšená doba krvácení, svědění, vyrážky a tinitus. Mezi další nežádoucí účinky hlášené příležitostně patří:
Tělo jako celek: horečka, infekce, sepse
Kardiovaskulární systém: městnavé srdeční selhání, hypertenze, tachykardie, synkopa
Zažívací ústrojí: sucho v ústech, ezofagitida, žaludeční/peptické vředy, gastritida, gastrointestinální krvácení, glositida, hematemeza, hepatitida, žloutenka
Hemický a lymfatický systém: ekchymóza, eozinofilie, leukopenie, meléna, purpura, rektální krvácení, stomatitida, trombocytopenie
Metabolické a nutriční: změny hmotnosti
Nervový systém: úzkost, astenie, zmatenost, deprese, abnormální sny, ospalost, nespavost, malátnost, nervozita, parestézie, ospalost, třes, vertigo
Dýchací systém: astma, dušnost
Kůže a přílohy: alopecie, fotosenzitivita, zvýšené pocení
Speciální smysly: rozmazané vidění
Urogenitální systém: cystitida, dysurie, hematurie, intersticiální nefritida, oligurie/polyurie, proteinurie, selhání ledvin
Další nežádoucí účinky, které se vyskytují vzácně, jsou:
Tělo jako celek: anafylaktické reakce, změny chuti k jídlu, smrt
Kardiovaskulární systém: arytmie, hypotenze, infarkt myokardu, palpitace, vaskulitida
Zažívací ústrojí: kolitida, říhání, fulminantní hepatitida se žloutenkou a bez žloutenky, selhání jater, nekróza jater, pankreatitida
Hemický a lymfatický systém: agranulocytóza, hemolytická anémie, aplastická anémie, lymfadenopatie, pancytopenie
Metabolické a nutriční: hyperglykémie
Nervový systém: křeče, kóma, halucinace, meningitida
Dýchací systém: respirační deprese, zápal plic
Kůže a přílohy: angioedém, toxická epidermální nekrolýza, erythema multiforme, exfoliativní dermatitida, Stevens-Johnsonův syndrom, kopřivka
Speciální smysly: zánět spojivek, poruchy sluchu
PŘEDÁVKOVAT
Symptomy po akutním předávkování NSAID byly typicky omezeny na letargii, ospalost, nauzeu, zvracení a epigastrickou bolest, které byly obvykle reverzibilní podpůrnou péčí. Objevilo se gastrointestinální krvácení. Hypertenze, akutní selhání ledvin, respirační deprese a kóma se vyskytly, ale byly vzácné (viz VAROVÁNÍ ; Kardiovaskulární trombotické příhody, gastrointestinální krvácení, ulcerace a hypertenze, renální toxicita a hyperkalémie ).
Ošetřujte pacienty symptomatickou a podpůrnou péčí po předávkování NSAID. Neexistují žádná specifická antidota. Zvažte zvracení a/nebo aktivní uhlí (60 až 100 gramů u dospělých, 1 až 2 gramy na kg tělesné hmotnosti u pediatrických pacientů) a/nebo osmotické katarzi u symptomatických pacientů pozorovaných do čtyř hodin po požití nebo u pacientů s velkým předávkováním ( 5 až 10násobek doporučené dávky). Forsírovaná diuréza, alkalizace moči, hemodialýza nebo hemoperfuze nemusí být užitečné kvůli vysoké vazbě na proteiny.
Pro další informace o léčbě předávkování kontaktujte toxikologické centrum (1-800-222-1222).
DROGOVÉ INTERAKCE
Klinicky významné lékové interakce s diklofenakem jsou uvedeny v tabulce 2.
VAROVÁNÍ
Kardiovaskulární trombotické příhody
Klinické studie několika COX-2 selektivních a neselektivních NSAID trvající až 3 roky ukázaly zvýšené riziko závažných kardiovaskulárních (KV) trombotických příhod, včetně infarktu myokardu (MI) a cévní mozkové příhody, které mohou být fatální. Na základě dostupných údajů není jasné, že riziko KV trombotických příhod je u všech NSAID podobné. Relativní nárůst závažných KV trombotických příhod nad výchozí hodnotu způsobený užíváním NSAID se zdá být podobný u pacientů se známým KV onemocněním nebo rizikovými faktory KV onemocnění i bez nich. Pacienti se známým KV onemocněním nebo rizikovými faktory však měli vyšší absolutní incidenci nadměrných závažných KV trombotických příhod, a to kvůli jejich zvýšené výchozí frekvenci. Některé observační studie zjistily, že toto zvýšené riziko závažných KV trombotických příhod začalo již v prvních týdnech léčby. Zvýšení KV trombotického rizika bylo nejkonzistentněji pozorováno při vyšších dávkách.
Aby se minimalizovalo potenciální riziko nežádoucí KV příhody u pacientů léčených NSAID, používejte nejnižší účinnou dávku po co nejkratší možnou dobu. Lékaři a pacienti by měli zůstat ostražití ohledně rozvoje takových příhod po celou dobu léčby, a to i v případě, že se nevyskytnou předchozí KV symptomy. Pacienti by měli být informováni o příznacích závažných KV příhod a o krocích, které je třeba učinit, pokud k nim dojde.
Neexistují žádné konzistentní důkazy, že současné užívání aspirinu zmírňuje zvýšené riziko závažných kardiovaskulárních trombotických příhod spojených s užíváním NSAID. Současné užívání aspirinu a NSAID, jako je diklofenak, zvyšuje riziko závažných gastrointestinálních (GI) příhod (viz VAROVÁNÍ ; Gastrointestinální krvácení , Ulcerace , a Perforace ).
Stav po operaci bypassu koronární tepny (CABG).
Dvě velké, kontrolované klinické studie COX-2 selektivního NSAID pro léčbu bolesti v prvních 10 až 14 dnech po operaci CABG zjistily zvýšený výskyt infarktu myokardu a cévní mozkové příhody. NSAID jsou kontraindikována při léčbě CABG (viz KONTRAINDIKACE ).
Pacienti po IM
Observační studie provedené v Dánském národním registru prokázaly, že pacienti léčení NSAID v období po IM měli zvýšené riziko reinfarktu, úmrtí související s kardiovaskulárními chorobami a mortalitu ze všech příčin počínaje prvním týdnem léčby. Ve stejné kohortě byla incidence úmrtí v prvním roce po IM 20 na 100 osoboroků u pacientů léčených NSAID ve srovnání s 12 na 100 osoboroků u pacientů neexponovaných NSAID. Přestože absolutní míra úmrtí po prvním roce po infarktu myokardu poněkud poklesla, zvýšené relativní riziko úmrtí u uživatelů NSAID přetrvávalo alespoň po další čtyři roky sledování.
Vyhněte se použití přípravku VOLTAREN u pacientů s nedávným infarktem myokardu, pokud se neočekává, že přínosy převáží riziko rekurentních KV trombotických příhod. Pokud se VOLTAREN používá u pacientů s nedávným infarktem myokardu, sledujte pacienty s ohledem na známky srdeční ischemie.
Gastrointestinální krvácení, ulcerace a perforace
NSAID, včetně diklofenaku, způsobují závažné gastrointestinální (GI) nežádoucí účinky, včetně zánětu, krvácení, ulcerace a perforace jícnu, žaludku, tenkého střeva nebo tlustého střeva, které mohou být fatální. Tyto závažné nežádoucí účinky se mohou u pacientů léčených NSAID objevit kdykoli, s varovnými příznaky nebo bez nich. Pouze jeden z pěti pacientů, u kterých se vyvine závažný nežádoucí účinek v horní části GI při léčbě NSAID, je symptomatický. Vředy v horní části gastrointestinálního traktu, velké krvácení nebo perforace způsobené NSAID se vyskytly u přibližně 1 % pacientů léčených po dobu 3 až 6 měsíců au přibližně 2 % až 4 % pacientů léčených po dobu jednoho roku. Ani krátkodobá terapie však není bez rizika.
Rizikové faktory GI krvácení, ulcerace a perforace
Pacienti s anamnézou peptického vředu a/nebo GI krvácení, kteří užívají NSAID, měli více než 10násobně zvýšené riziko rozvoje GI krvácení ve srovnání s pacienty bez těchto rizikových faktorů. Mezi další faktory, které zvyšují riziko GI krvácení u pacientů léčených NSAID, patří delší trvání léčby NSAID, současné užívání perorálních kortikosteroidů, aspirinu, antikoagulancií nebo selektivních inhibitorů zpětného vychytávání serotoninu (SSRI); kouření, požívání alkoholu, vyšší věk a špatný celkový zdravotní stav. Většina postmarketingových hlášení fatálních GI příhod se objevila u starších nebo oslabených pacientů. Kromě toho mají pacienti s pokročilým onemocněním jater a/nebo koagulopatií zvýšené riziko GI krvácení.
Strategie MINIMALIZACE GI rizik u pacientů léčených NSAID
- Používejte nejnižší účinnou dávku po co nejkratší možnou dobu.
- Vyhněte se podávání více než jednoho NSAID současně
- Vyhněte se použití u pacientů s vyšším rizikem, pokud se neočekává, že přínosy převáží zvýšené riziko krvácení. U takových pacientů, stejně jako u pacientů s aktivním gastrointestinálním krvácením, zvažte jinou léčbu než NSAID.
- Během léčby nesteroidními antirevmatiky buďte ostražití na známky a příznaky GI ulcerace a krvácení.
- Pokud je podezření na závažnou gastrointestinální nežádoucí příhodu, okamžitě zahajte vyhodnocení a léčbu a přerušte léčbu přípravkem VOLTAREN 50 mg, dokud není závažná gastrointestinální nežádoucí příhoda vyloučena.
- Při současném užívání nízkých dávek kyseliny acetylsalicylové k profylaxi srdce pacienty pečlivěji sledujte, zda se u nich neprojeví gastrointestinální krvácení (viz OPATŘENÍ ; Lékové interakce ).
Hepatotoxicita
V klinických studiích s přípravky obsahujícími diklofenak bylo pozorováno významné zvýšení (tj. více než trojnásobek horní hranice normy [ULN]) aspartátaminotransferázy (AST) (také známé jako SGOT) u přibližně 2 % z přibližně 5 700 pacientů určitou dobu během léčby diklofenakem (alaninaminotransferáza [ALT] nebyla měřena ve všech studiích).
Ve velké, otevřené, kontrolované studii s 3 700 pacienty léčenými perorálním diklofenakem sodným po dobu 2 až 6 měsíců byli pacienti sledováni nejprve po 8 týdnech a 1 200 pacientů bylo sledováno znovu po 24 týdnech. Významné zvýšení ALT a/nebo AST se objevilo u asi 4 % pacientů a zahrnovalo výrazné zvýšení (více než 8násobek ULN) u asi 1 % z 3700 pacientů. V této otevřené studii byla u pacientů pozorována vyšší incidence hraničního (méně než 3násobek ULN), středního (3 až 8násobek ULN) a výrazného (více než 8násobku ULN) zvýšení ALT nebo AST užívání diklofenaku ve srovnání s jinými NSAID. Zvýšení transamináz bylo pozorováno častěji u pacientů s osteoartrózou než u pacientů s revmatoidní artritidou.
Téměř všechna významná zvýšení transamináz byla detekována předtím, než se pacienti stali symptomatickými. Abnormální testy se objevily během prvních 2 měsíců léčby diklofenakem u 42 z 51 pacientů ve všech studiích, u kterých došlo k výraznému zvýšení transamináz.
V postmarketingových hlášeních byly hlášeny případy hepatotoxicity vyvolané léky během prvního měsíce a v některých případech prvních 2 měsíců léčby, ale mohou se objevit kdykoli během léčby diklofenakem. Postmarketingové sledování zaznamenalo případy závažných jaterních reakcí, včetně nekrózy jater, žloutenky, fulminantní hepatitidy se žloutenkou i bez ní a selhání jater. Některé z těchto hlášených případů měly za následek úmrtí nebo transplantaci jater.
evropské retrospektivní populační, případem kontrolované studii bylo 10 případů poškození jater souvisejícího s diklofenakem při současném užívání ve srovnání s neužíváním diklofenaku spojeno se statisticky významným 4násobně upraveným poměrem pravděpodobnosti poškození jater. V této konkrétní studii, na základě celkového počtu 10 případů poškození jater spojených s diklofenakem, se upravený poměr šancí dále zvýšil s ženským pohlavím, dávkami 150 mg nebo více a délkou užívání po dobu delší než 90 dní.
Lékaři by měli měřit transaminázy na začátku a pravidelně u pacientů, kteří jsou dlouhodobě léčeni diklofenakem, protože se může vyvinout závažná hepatotoxicita bez prodromu rozlišujících příznaků. Optimální časy pro provedení prvního a následujících měření transamináz nejsou známy. Na základě údajů z klinických studií a postmarketingových zkušeností by měly být transaminázy monitorovány během 4 až 8 týdnů po zahájení léčby diklofenakem. Závažné jaterní reakce se však mohou objevit kdykoli během léčby diklofenakem.
Pokud abnormální jaterní testy přetrvávají nebo se zhoršují, pokud se rozvinou klinické příznaky a/nebo symptomy odpovídající onemocnění jater nebo pokud se objeví systémové projevy (např. eozinofilie, vyrážka, bolest břicha, průjem, tmavá moč atd.), je třeba přípravek VOLTAREN okamžitě vysadit .
Informujte pacienty o varovných příznacích a příznacích hepatotoxicity (např. nevolnost, únava, letargie, průjem, pruritus, žloutenka, citlivost v pravém horním kvadrantu a příznaky podobné chřipce). Pokud se rozvinou klinické známky a příznaky odpovídající onemocnění jater nebo pokud se objeví systémové projevy (např. eozinofilie, vyrážka atd.), okamžitě přerušte léčbu přípravkem VOLTAREN a proveďte klinické vyšetření pacienta.
Aby se minimalizovalo potenciální riziko nežádoucích jaterních příhod u pacientů léčených přípravkem VOLTAREN, používejte nejnižší účinnou dávku po co nejkratší možnou dobu. Buďte opatrní při předepisování VOLTAREN 100 mg současně s léky, o kterých je známo, že jsou potenciálně hepatotoxické (např. acetaminofen, antibiotika, antiepileptika).
Hypertenze
NSAID, včetně přípravku VOLTAREN 100 mg, mohou vést k novému vzniku hypertenze nebo ke zhoršení již existující hypertenze, přičemž obojí může přispívat ke zvýšenému výskytu KV příhod. Pacienti užívající inhibitory angiotenzin konvertujícího enzymu (ACE), thiazidová diuretika nebo kličková diuretika mohou mít při užívání NSAID zhoršenou odpověď na tyto terapie (viz OPATŘENÍ ; DROGOVÉ INTERAKCE ).
Sledujte krevní tlak (TK) během zahájení léčby NSAID a v průběhu léčby.
Srdeční Selhání A Edém
Metaanalýza randomizovaných kontrolovaných studií Coxib and traditional NSAID Trialists’ Collaboration prokázala přibližně 2-násobný nárůst hospitalizací pro srdeční selhání u pacientů selektivně léčených COX-2 a neselektivních pacientů léčených NSAID ve srovnání s pacienty léčenými placebem. Ve studii dánského národního registru pacientů se srdečním selháním užívání NSAID zvýšilo riziko infarktu myokardu, hospitalizace pro srdeční selhání a úmrtí.
některých pacientů léčených NSAID byla navíc pozorována retence tekutin a edém. Použití diklofenaku může zeslabit kardiovaskulární účinky několika terapeutických látek používaných k léčbě těchto zdravotních stavů (např. diuretik, ACE inhibitorů nebo blokátorů receptorů pro angiotenzin [ARB]) (viz DROGOVÉ INTERAKCE ).
Nepoužívejte VOLTAREN u pacientů se závažným srdečním selháním, pokud se neočekává, že přínosy převáží riziko zhoršení srdečního selhání. Pokud se VOLTAREN 50 mg používá u pacientů se závažným srdečním selháním, sledujte pacienty, zda se u nich nevyskytují známky zhoršení srdečního selhání.
Renální toxicita a hyperkalémie
Renální toxicita
Dlouhodobé podávání NSAID vedlo k renální papilární nekróze a jinému poškození ledvin.
Renální toxicita byla také pozorována u pacientů, u kterých mají renální prostaglandiny kompenzační roli při udržování renální perfuze. U těchto pacientů může podávání NSAID způsobit na dávce závislé snížení tvorby prostaglandinů a sekundárně i renálního průtoku krve, což může urychlit zjevnou renální dekompenzaci. Největší riziko této reakce jsou pacienti s poruchou funkce ledvin, dehydratací, hypovolémií, srdečním selháním, jaterní dysfunkcí, ti, kteří užívají diuretika a ACE inhibitory nebo ARB, a starší lidé. Po přerušení léčby NSAID obvykle následuje návrat do stavu před léčbou.
Z kontrolovaných klinických studií nejsou dostupné žádné informace o použití přípravku VOLTAREN 100 mg u pacientů s pokročilým onemocněním ledvin. Renální účinky přípravku VOLTAREN 50 mg mohou urychlit progresi renální dysfunkce u pacientů s již existujícím onemocněním ledvin.
dehydratovaných nebo hypovolemických pacientů upravte stav objemu před zahájením léčby přípravkem VOLTAREN. Monitorujte renální funkce u pacientů s poruchou funkce ledvin nebo jater, srdečním selháním, dehydratací nebo hypovolémií během užívání přípravku VOLTAREN (viz DROGOVÉ INTERAKCE ). Nepoužívejte VOLTAREN u pacientů s pokročilým onemocněním ledvin, pokud se neočekává, že přínosy převáží riziko zhoršení renálních funkcí. Pokud se VOLTAREN 50 mg používá u pacientů s pokročilým onemocněním ledvin, sledujte pacienty s ohledem na známky zhoršení funkce ledvin.
Hyperkalémie
Při užívání NSAID bylo hlášeno zvýšení koncentrace draslíku v séru, včetně hyperkalémie, a to i u některých pacientů bez poškození ledvin. U pacientů s normální funkcí ledvin byly tyto účinky připisovány hyporeninemicko-hypoaldosteronistickému stavu.
Anafylaktické reakce
Diklofenak byl spojován s anafylaktickými reakcemi u pacientů se známou přecitlivělostí na diklofenak i bez nich a u pacientů s astmatem citlivým na aspirin (viz KONTRAINDIKACE , VAROVÁNÍ ; Exacerbace astmatu souvisejícího s citlivostí na aspirin ).
Exacerbace astmatu souvisejícího s citlivostí na aspirin
Subpopulace pacientů s astmatem může mít astma citlivé na aspirin, které může zahrnovat chronickou rinosinusitidu komplikovanou nosními polypy; těžký, potenciálně fatální bronchospasmus; a/nebo nesnášenlivost aspirinu a jiných NSAID. Protože u pacientů citlivých na aspirin byla hlášena zkřížená reaktivita mezi aspirinem a jinými NSAID, je VOLTAREN 100 mg kontraindikován u pacientů s touto formou citlivosti na aspirin (viz KONTRAINDIKACE ). Pokud se VOLTAREN 100 mg používá u pacientů s již existujícím astmatem (bez známé citlivosti na kyselinu acetylsalicylovou), sledujte pacienty z hlediska změn známek a příznaků astmatu.
Závažné kožní reakce
NSAID, včetně diklofenaku, mohou způsobit závažné kožní nežádoucí reakce, jako je exfoliativní dermatitida, Stevens-Johnsonův syndrom (SJS) a toxická epidermální nekrolýza (TEN), které mohou být fatální. Tyto závažné události mohou nastat bez varování. Informujte pacienty o známkách a příznacích závažných kožních reakcí a aby přerušili užívání přípravku VOLTAREN při prvním výskytu kožní vyrážky nebo jakýchkoli jiných příznaků přecitlivělosti. VOLTAREN je kontraindikován u pacientů s předchozími závažnými kožními reakcemi na NSAID (viz KONTRAINDIKACE ).
Léková reakce s eozinofilií a systémovými příznaky (DRESS)
pacientů užívajících NSAID, jako je VOLTAREN, byla hlášena léková reakce s eozinofilií a systémovými příznaky (DRESS). Některé z těchto událostí byly smrtelné nebo život ohrožující. DRESS se typicky, i když ne výlučně, projevuje horečkou, vyrážkou, lymfadenopatií a/nebo otokem obličeje. Jiné klinické projevy mohou zahrnovat hepatitidu, nefritidu, hematologické abnormality, myokarditidu nebo myozitidu. Někdy mohou příznaky DRESS připomínat akutní virovou infekci. Často je přítomna eozinofilie. Vzhledem k tomu, že tato porucha je ve svém projevu proměnlivá, mohou se na ní podílet i jiné orgánové systémy, které zde nejsou uvedeny. Je důležité si uvědomit, že časné projevy přecitlivělosti, jako je horečka nebo lymfadenopatie, mohou být přítomny, i když vyrážka není zjevná. Pokud jsou takové známky nebo příznaky přítomny, přerušte léčbu přípravkem VOLTAREN 50 mg a okamžitě pacienta vyhodnoťte.
Fetální toxicita
Předčasné uzavření Fetal Ductus Arteriosus
Vyhněte se užívání NSAID, včetně přípravku VOLTAREN 50 mg, u těhotných žen přibližně ve 30. týdnu těhotenství a později. NSAID, včetně přípravku VOLTAREN 50 mg, zvyšují riziko předčasného uzávěru ductus arteriosus plodu přibližně v tomto gestačním věku.
Oligohydramnion/novorozenecké poškození ledvin
Užívání NSAID, včetně VOLTARENU, ve 20. týdnu těhotenství nebo později v těhotenství může způsobit fetální renální dysfunkci vedoucí k oligohydramniu a v některých případech neonatálnímu poškození ledvin. Tyto nežádoucí účinky jsou pozorovány v průměru po dnech až týdnech léčby, ačkoli oligohydramnion byl zřídka hlášen již 48 hodin po zahájení NSAID. Oligohydramnion je často, ale ne vždy, po přerušení léčby reverzibilní. Komplikace prodlouženého oligohydramnia mohou například zahrnovat kontraktury končetin a opožděné dozrávání plic. V některých postmarketingových případech poškození funkce ledvin novorozenců byly vyžadovány invazivní postupy, jako je výměnná transfuze nebo dialýza.
Pokud je léčba NSAID nezbytná mezi 20. a 30. týdnem těhotenství, omezte užívání přípravku VOLTAREN na nejnižší účinnou dávku a na nejkratší možnou dobu. Pokud léčba přípravkem VOLTAREN 50 mg přesáhne 48 hodin, zvažte ultrazvukové monitorování plodové vody. Pokud se objeví oligohydramnion, vysaďte VOLTAREN 100 mg a sledujte podle klinické praxe (viz. OPATŘENÍ ; Těhotenství ).
Hematologická toxicita
U pacientů léčených NSAID se objevila anémie. To může být způsobeno okultní nebo hrubou ztrátou krve, zadržováním tekutin nebo neúplně popsaným vlivem na erytropoézu. Pokud má pacient léčený přípravkem VOLTAREN jakékoli známky nebo příznaky anémie, sledujte hemoglobin nebo hematokrit.
NSAID, včetně přípravku VOLTAREN 100 mg, mohou zvýšit riziko krvácivých příhod. Toto riziko mohou zvýšit přidružená onemocnění, jako jsou poruchy koagulace, současné užívání warfarinu, jiných antikoagulancií, protidestičkových látek (např. aspirin), inhibitorů zpětného vychytávání serotoninu (SSRI) a inhibitorů zpětného vychytávání serotoninu a norepinefrinu (SNRI). Sledujte u těchto pacientů známky krvácení (viz DROGOVÉ INTERAKCE ).
OPATŘENÍ
Všeobecné
Nelze očekávat, že VOLTAREN® (enterosolventní potahované tablety sodné soli diklofenaku) nahrazuje kortikosteroidy nebo léčí nedostatečnost kortikosteroidů. Náhlé vysazení kortikosteroidů může vést k exacerbaci onemocnění. U pacientů na prodloužené léčbě kortikosteroidy by měla být léčba pomalu snižována, pokud se rozhodne kortikosteroidy vysadit, a pacient by měl být pečlivě sledován, zda se u něj neprojeví jakékoli známky nežádoucích účinků, včetně nedostatečnosti nadledvin a exacerbace příznaků artritidy.
Farmakologická aktivita přípravku VOLTAREN 50 mg při snižování horečky a zánětu může snížit užitečnost těchto diagnostických příznaků při detekci komplikací předpokládaných neinfekčních bolestivých stavů.

Informace pro pacienty
Doporučte pacientovi, aby si přečetl označení pacienta schválené FDA ( Průvodce léky ), který doprovází každý vydaný předpis. Před zahájením léčby přípravkem VOLTAREN a pravidelně v průběhu probíhající léčby informujte pacienty, rodiny nebo jejich pečovatele o následujících informacích.
Kardiovaskulární trombotické příhody
Informujte pacienty, aby byli ostražití na příznaky kardiovaskulárních trombotických příhod, včetně bolesti na hrudi, dušnosti, slabosti nebo nezřetelné řeči, a aby jakýkoli z těchto příznaků okamžitě hlásili svému poskytovateli zdravotní péče (viz VAROVÁNÍ ; Kardiovaskulární trombotické příhody ).
Gastrointestinální krvácení, ulcerace a perforace
Poraďte pacientům, aby svému poskytovateli zdravotní péče hlásili příznaky ulcerací a krvácení, včetně bolesti v epigastriu, dyspepsie, meleny a hematemézy. Při současném užívání nízkých dávek kyseliny acetylsalicylové k profylaxi srdce informujte pacienty o zvýšeném riziku známek a příznaků gastrointestinálního krvácení (viz VAROVÁNÍ ; Gastrointestinální krvácení , Ulcerace , a Perforace ).
Hepatotoxicita
Informujte pacienty o varovných příznacích a příznacích hepatotoxicity (např. nevolnost, únava, letargie, svědění, průjem, žloutenka, citlivost v pravém horním kvadrantu a příznaky podobné chřipce). Pokud k tomu dojde, poučte pacienty, aby přestali užívat VOLTAREN 50 mg a okamžitě vyhledali lékařskou léčbu (viz VAROVÁNÍ ; Hepatotoxicita ).
Srdeční Selhání A Edém
Informujte pacienty, aby si dávali pozor na příznaky městnavého srdečního selhání, včetně dušnosti, nevysvětlitelného přírůstku hmotnosti nebo edému, a aby v případě výskytu těchto příznaků kontaktovali svého poskytovatele zdravotní péče (viz VAROVÁNÍ ; Srdeční selhání a edém ).
Anafylaktické reakce
Informujte pacienty o známkách anafylaktické reakce (např. potíže s dýcháním, otok obličeje nebo hrdla). Poučte pacienty, aby vyhledali okamžitou pohotovostní pomoc, pokud k tomu dojde (viz VAROVÁNÍ ; Anafylaktické reakce ).
Vážné kožní reakce, včetně ŠATY
Informujte pacienty, aby okamžitě ukončili užívání přípravku VOLTAREN 50 mg, pokud se u nich objeví jakýkoli typ vyrážky nebo horečky, a co nejdříve kontaktujte svého poskytovatele zdravotní péče (viz VAROVÁNÍ ; Závažné kožní reakce ).
Ženská plodnost
Informujte ženy s reprodukčním potenciálem, které si přejí otěhotnět, že NSAID, včetně přípravku VOLTAREN 50 mg, mohou být spojeny s reverzibilním zpožděním ovulace (viz OPATŘENÍ ; Karcinogeneze, mutageneze, zhoršení plodnosti ).
Fetální toxicita
Informujte těhotné ženy, aby se vyvarovaly užívání VOLTARENU a jiných NSAID, počínaje 30. týdnem těhotenství kvůli riziku předčasného uzavření ductus arteriosus plodu. Pokud je u těhotné ženy mezi 20. až 30. týdnem těhotenství nutná léčba přípravkem VOLTAREN, upozorněte ji, že může být nutné sledovat oligohydramnion, pokud léčba trvá déle než 48 hodin. (vidět VAROVÁNÍ ; Fetální toxicita , OPATŘENÍ , Těhotenství ).
Vyhněte se současnému užívání NSAID
Informujte pacienty, že současné užívání přípravku VOLTAREN 50 mg s jinými NSAID nebo salicyláty (např. diflunisal, salsalát) se nedoporučuje kvůli zvýšenému riziku gastrointestinální toxicity a malému nebo žádnému zvýšení účinnosti (viz VAROVÁNÍ ; Gastrointestinální krvácení , Ulcerace , a Perforace a lékové interakce ). Upozorněte pacienty, že NSAID mohou být přítomna v „volně prodejných“ lécích k léčbě nachlazení, horečky nebo nespavosti.
Užívání NSAID a nízké dávky aspirinu
Informujte pacienty, aby neužívali nízké dávky aspirinu současně s přípravkem VOLTAREN, dokud si nepromluví se svým poskytovatelem zdravotní péče (viz DROGOVÉ INTERAKCE ).
Maskování Zánětu A Horečky
Farmakologická aktivita přípravku VOLTAREN při snižování zánětu a možná i horečky může snížit užitečnost diagnostických příznaků při detekci infekcí.
Laboratorní monitorování
Vzhledem k tomu, že závažné GI krvácení, hepatotoxicita a poškození ledvin se mohou objevit bez varovných příznaků nebo známek, zvažte pravidelné sledování pacientů na dlouhodobé léčbě NSAID pomocí CBC a chemického profilu (viz VAROVÁNÍ ; Gastrointestinální krvácení , Ulcerace a perforace , a Hepatotoxicita ).
Karcinogeneze, mutageneze, zhoršení plodnosti
Karcinogeneze
Dlouhodobé studie karcinogenity u potkanů, kterým byl podáván diklofenak sodný až do 2 mg/kg/den (přibližně 0,1násobek maximální doporučené dávky pro člověka (MRHD) přípravku VOLTAREN 50 mg, 200 mg/den, na základě srovnání plochy povrchu těla (BSA)) odhalily žádné významné zvýšení incidence nádorů. Dvouletá studie karcinogenity prováděná na myších užívajících sodnou sůl diklofenaku v dávkách až 0,3 mg/kg/den (přibližně 0,007násobek MRHD na základě srovnání BSA) u samců a 1 mg/kg/den (přibližně 0,02násobek MRHD na základě Srovnání BSA) u žen neodhalilo žádný onkogenní potenciál.
Mutageneze
Diklofenak sodný nevykazoval mutagenní aktivitu v in vitro testech bodových mutací v savčích (myší lymfom) a mikrobiálních (kvasinky, Ames) testovacích systémech a byl nemutagenní v několika in vitro a in vivo testech na savcích, včetně dominantních letálních a samčích germinálních epiteliálních chromozomálních chromozomálních studií u myší a studie anomálií jádra a chromozomálních aberací u čínských křečků.
Zhoršení Plodnosti
Diklofenak sodný podávaný samcům a samicím potkanů v dávce 4 mg/kg/den (přibližně 0,2násobek MRHD na základě srovnání BSA) neovlivnil fertilitu.
Na základě mechanismu účinku může užívání NSAID zprostředkovaných prostaglandiny, včetně přípravku VOLTAREN 100 mg, oddálit nebo zabránit prasknutí ovariálních folikulů, které je u některých žen spojováno s reverzibilní neplodností. Publikované studie na zvířatech ukázaly, že podávání inhibitorů syntézy prostaglandinů má potenciál narušit prostaglandiny zprostředkovanou rupturu folikulů potřebnou pro ovulaci. Malé studie u žen léčených NSAID také prokázaly reverzibilní zpoždění ovulace. Zvažte vysazení NSAID, včetně přípravku VOLTAREN 100 mg, u žen, které mají potíže s početím nebo které podstupují vyšetření neplodnosti.
Těhotenství
Shrnutí rizik
Užívání NSAID, včetně VOLTARENU, může způsobit předčasné uzavření ductus arteriosus plodu a fetální renální dysfunkci vedoucí k oligohydramniu a v některých případech neonatálnímu poškození ledvin. Kvůli těmto rizikům omezte dávku a délku užívání přípravku VOLTAREN mezi přibližně 20. a 30. týdnem těhotenství a vyhněte se užívání přípravku VOLTAREN přibližně ve 30. týdnu těhotenství a později v těhotenství (viz VAROVÁNÍ ; Fetální toxicita ).
Předčasné uzavření Fetal Ductus Arteriosus
Užívání NSAID, včetně přípravku VOLTAREN 100 mg, přibližně ve 30. týdnu těhotenství nebo později v těhotenství zvyšuje riziko předčasného uzávěru ductus arteriosus plodu.
Oligohydramnion/novorozenecké poškození ledvin
Užívání NSAID přibližně ve 20. týdnu těhotenství nebo později v těhotenství bylo spojeno s případy fetální renální dysfunkce vedoucí k oligohydramniu a v některých případech neonatálnímu poškození ledvin.
Neexistují žádné adekvátní a dobře kontrolované studie s přípravkem VOLTAREN 100 mg u těhotných žen.
Údaje z observačních studií týkající se potenciálních embryo-fetálních rizik užívání NSAID u žen v prvním nebo druhém trimestru těhotenství jsou neprůkazné.
reprodukčních studiích na zvířatech nebyly pozorovány žádné známky teratogenity u myší, potkanů nebo králíků, kterým byl podáván diklofenak během období organogeneze v dávkách až přibližně 0,5, 0,5 a 1násobku maximální doporučené dávky VOLTAREN pro člověka (MRHD). , 200 mg/den, navzdory přítomnosti mateřské a fetální toxicity v těchto dávkách (viz Data ).
Na základě publikovaných údajů na zvířatech bylo prokázáno, že prostaglandiny hrají důležitou roli v permeabilitě cév endometria, implantaci blastocyst a decidualizaci. Ve studiích na zvířatech vedlo podávání inhibitorů syntézy prostaglandinů, jako je diklofenak, ke zvýšeným pre- a postimplantačním ztrátám. Bylo také prokázáno, že prostaglandiny hrají důležitou roli ve vývoji ledvin plodu. V publikovaných studiích na zvířatech bylo hlášeno, že inhibitory syntézy prostaglandinů narušují vývoj ledvin, když jsou podávány v klinicky relevantních dávkách.
Odhadované základní riziko závažných vrozených vad a potratu pro uvedenou populaci (populace) není známo. Všechna těhotenství mají na pozadí riziko vrozené vady, ztráty nebo jiných nepříznivých následků. V obecné populaci USA je odhadované základní riziko závažných vrozených vad a potratu u klinicky uznaných těhotenství 2 % až 4 % a 15 % až 20 %.
Klinické úvahy
Fetální/neonatální nežádoucí reakce
Předčasný uzávěr fetálního ductus arteriosus:
Vyvarujte se užívání NSAID u žen přibližně ve 30. týdnu těhotenství a později v těhotenství, protože NSAID, včetně přípravku VOLTAREN, mohou způsobit předčasné uzavření ductus arteriosus plodu (viz VAROVÁNÍ ; Fetální toxicita ).
Oligohydramnion / neonatální poškození ledvin:
Je-li nutné NSAID přibližně ve 20. týdnu těhotenství nebo později v těhotenství, omezte použití na nejnižší účinnou dávku a nejkratší možnou dobu trvání. Pokud léčba přípravkem VOLTAREN 50 mg přesáhne 48 hodin, zvažte sledování oligohydramnionu ultrazvukem. Pokud se objeví oligohydramnion, přerušte léčbu přípravkem VOLTAREN a postupujte podle klinické praxe (viz VAROVÁNÍ ; Fetální toxicita ).
Data
Lidská data
Předčasný uzávěr fetálního ductus arteriosus:
Publikovaná literatura uvádí, že použití NSAID přibližně ve 30. týdnu těhotenství a později v těhotenství může způsobit předčasné uzavření ductus arteriosus plodu.
Oligohydramnion / neonatální poškození ledvin:
Publikované studie a postmarketingové zprávy popisují užívání NSAID u matek přibližně ve 20. týdnu těhotenství nebo později v těhotenství spojené s fetální renální dysfunkcí vedoucí k oligohydramniu a v některých případech neonatálnímu poškození ledvin. Tyto nežádoucí účinky jsou pozorovány v průměru po dnech až týdnech léčby, ačkoli oligohydramnion byl zřídka hlášen již 48 hodin po zahájení NSAID. V mnoha případech, ale ne ve všech, byl pokles plodové vody přechodný a reverzibilní po vysazení léku. Existuje omezený počet kazuistik užívání NSAID u matek a neonatální renální dysfunkce bez oligohydramnia, z nichž některé byly ireverzibilní. Některé případy neonatální renální dysfunkce vyžadovaly léčbu invazivními postupy, jako je výměnná transfuze nebo dialýza.
Metodologická omezení těchto postmarketingových studií a zpráv zahrnují nedostatek kontrolní skupiny; omezené informace týkající se dávky, trvání a načasování expozice léku; a současné užívání jiných léků. Tato omezení znemožňují stanovení spolehlivého odhadu rizika nepříznivých fetálních a neonatálních výsledků při užívání NSAID matkou. Vzhledem k tomu, že publikované údaje o bezpečnosti týkající se neonatálních výsledků zahrnovaly většinou předčasně narozené děti, je zobecnění určitých hlášených rizik pro donošené dítě vystavené NSAID při užívání matkou nejisté.
Údaje o zvířatech
Reprodukční a vývojové studie na zvířatech prokázaly, že podávání sodné soli diklofenaku během organogeneze nevyvolalo teratogenitu navzdory indukci mateřské toxicity a fetální toxicity u myší při perorálních dávkách až 20 mg/kg/den (přibližně 0,5násobek maximální doporučené dávky pro člověka [MRHD ] VOLTARENU, 200 mg/den, na základě srovnání plochy povrchu těla (BSA) a u potkanů a králíků v perorálních dávkách až 10 mg/kg/den (přibližně 0,5 a 1násobek MRHD na základě BSA srovnání). Ve studii, ve které byly březím krysám perorálně podávány 2 nebo 4 mg/kg diklofenaku (0,1 a 0,2násobek MRHD na základě BSA) od 15. dne gestace do 21. dne laktace, byla zaznamenána významná toxicita pro matku (peritonitida, mortalita). Tyto dávky toxické pro matku byly spojeny s dystokií, prodlouženou gestací, sníženou hmotností a růstem plodu a sníženým přežitím plodu. Bylo prokázáno, že diklofenak prochází placentární bariérou u myší, potkanů a lidí.
Práce nebo dodávka
Neexistují žádné studie o účincích přípravku VOLTAREN během porodu. Ve studiích na zvířatech NSAID, včetně diklofenaku, inhibují syntézu prostaglandinů, způsobují opožděný porod a zvyšují výskyt mrtvého porodu.
Kojící matky
Shrnutí rizik
Na základě dostupných údajů může být diklofenak přítomen v mateřském mléce. Vývojové a zdravotní přínosy kojení by měly být zváženy společně s klinickou potřebou matky VOLTAREN a případnými nežádoucími účinky na kojené dítě z VOLTAREN 100 mg nebo ze základního stavu matky.
Data
Jedna žena léčená perorálně solí diklofenaku, 150 mg/den, měla hladinu diklofenaku v mléce 100 mcg/l, což odpovídá dětské dávce přibližně 0,03 mg/kg/den. Diklofenak nebyl detekovatelný v mateřském mléce u 12 žen užívajících diklofenak (buď po 100 mg/den perorálně po dobu 7 dnů nebo po jednorázové 50 mg intramuskulární dávce podané bezprostředně po porodu).
Pediatrické použití
Bezpečnost a účinnost u pediatrických pacientů nebyla stanovena.
Geriatrické použití
Starší pacienti jsou ve srovnání s mladšími pacienty vystaveni většímu riziku závažných kardiovaskulárních, gastrointestinálních a/nebo renálních nežádoucích reakcí spojených s NSAID. Pokud očekávaný přínos pro staršího pacienta převáží tato potenciální rizika, začněte s dávkováním na spodní hranici dávkovacího rozmezí a sledujte pacienty kvůli nežádoucím účinkům (viz VAROVÁNÍ ; Kardiovaskulární trombotické příhody , Gastrointestinální Krvácení, ulcerace a perforace, hepatotoxicita, renální toxicita a hyperkalémie, BEZPEČNOSTNÍ OPATŘENÍ; Laboratorní monitorování).
Je známo, že diklofenak je v podstatě vylučován ledvinami a riziko nežádoucích reakcí na tento lék může být vyšší u pacientů s poruchou funkce ledvin. Vzhledem k tomu, že u starších pacientů je pravděpodobnější, že budou mít sníženou funkci ledvin, je třeba věnovat pozornost výběru dávky a může být užitečné sledovat funkci ledvin (viz KLINICKÁ FARMAKOLOGIE , NEŽÁDOUCÍ REAKCE ).
PŘEDÁVKOVAT
Nebyly poskytnuty žádné informace
KONTRAINDIKACE
VOLTAREN® je kontraindikován u následujících pacientů:
- Známá přecitlivělost (např. anafylaktické reakce a závažné kožní reakce) na diklofenak nebo kteroukoli složku léčivého přípravku (viz VAROVÁNÍ ; Anafylaktické reakce , Závažné kožní reakce ).
- Anamnéza astmatu, kopřivky nebo jiných reakcí alergického typu po užití aspirinu nebo jiných NSAID. U těchto pacientů byly hlášeny těžké, někdy fatální, anafylaktické reakce na NSAID (viz VAROVÁNÍ ; Anafylaktická reakce , Exacerbace astmatu souvisejícího s citlivostí na aspirin ).
- Při operaci bypassu koronární artérie (CABG) (viz VAROVÁNÍ ; Kardiovaskulární trombotické příhody ).
KLINICKÁ FARMAKOLOGIE
Mechanismus působení
Diklofenak má analgetické, protizánětlivé a antipyretické vlastnosti.
Mechanismus účinku přípravku VOLTAREN 100 mg, stejně jako u jiných NSAID, není zcela objasněn, ale zahrnuje inhibici cyklooxygenázy (COX-1 a COX-2).
Diklofenak je silný inhibitor syntézy prostaglandinů in vitro. Koncentrace diklofenaku dosažené během léčby vyvolaly účinky in vivo. Prostaglandiny senzibilizují aferentní nervy a zesilují účinek bradykininu při vyvolávání bolesti na zvířecích modelech. Prostaglandiny jsou mediátory zánětu. Protože je diklofenak inhibitorem syntézy prostaglandinů, jeho mechanismus účinku může být způsoben poklesem prostaglandinů v periferních tkáních.
Farmakokinetika
Vstřebávání
Diklofenak je 100% absorbován po perorálním podání ve srovnání s intravenózním (IV) podáním, měřeno výtěžkem moči. V důsledku first-pass metabolismu je však systémově dostupných pouze asi 50 % absorbované dávky (viz tabulka 1). Jídlo nemá významný vliv na rozsah absorpce diklofenaku. Obvykle však dochází ke zpoždění nástupu absorpce o 1 až 4,5 hodiny a snížení maximálních plazmatických hladin o méně než 20 %.
Rozdělení
Zdánlivý distribuční objem (V/F) sodné soli diklofenaku je 1,4 l/kg.
Diklofenak se z více než 99 % váže na lidské sérové proteiny, především na albumin. Vazba na sérové proteiny je konstantní v rozmezí koncentrací (0,15 až 105 mcg/ml) dosažených doporučenými dávkami.
Diklofenak difunduje do synoviální tekutiny a ven ze synoviální tekutiny. K difúzi do kloubu dochází, když jsou hladiny v plazmě vyšší než hladiny v synoviální tekutině, načež se proces obrátí a hladiny synoviální tekutiny jsou vyšší než hladiny v plazmě. Není známo, zda difúze do kloubu hraje roli v účinnosti diklofenaku.
Odstranění
Metabolismus
lidské plazmě a moči bylo identifikováno pět metabolitů diklofenaku. Mezi metabolity patří 4'Âhydroxy-, 5-hydroxy-, 3'-hydroxy-, 4',5-dihydroxy- a 3'-hydroxy-4'-methoxy-diclofenac. Hlavní metabolit diklofenaku, 4'-hydroxy-diklofenak, má velmi slabou farmakologickou aktivitu. Tvorba 4-hydroxy-diclofenaku je primárně zprostředkována CYP2C9. Jak diklofenak, tak jeho oxidační metabolity podléhají glukuronidaci nebo sulfataci s následnou exkrecí žlučí. Acylglukuronidace zprostředkovaná UGT2B7 a oxidace zprostředkovaná CYP2C8 mohou také hrát roli v metabolismu diklofenaku. CYP3A4 je zodpovědný za tvorbu minoritních metabolitů, 5-hydroxy- a 3-hydroxy-diklofenaku. U pacientů s renální dysfunkcí byly maximální koncentrace metabolitů 4'-hydroxy- a 5-hydroxy-diklofenaku přibližně 50 % a 4 % původní sloučeniny po jednorázovém perorálním podání ve srovnání s 27 % a 1 % u normálních zdravých subjektů.
Vylučování
Diklofenak je eliminován metabolismem a následným vylučováním glukuronidu a sulfátových konjugátů metabolitů močí a žlučí. Do moči se vylučuje malé množství nebo žádný volný nezměněný diklofenak. Přibližně 65 % dávky se vylučuje močí a přibližně 35 % žlučí jako konjugáty nezměněného diklofenaku a metabolitů. Vzhledem k tomu, že renální eliminace není významnou cestou eliminace nezměněného diklofenaku, není nutná úprava dávkování u pacientů s mírnou až středně těžkou renální dysfunkcí. Terminální poločas nezměněného diklofenaku je přibližně 2 hodiny.
Zvláštní populace
Pediatrická
Farmakokinetika přípravku VOLTAREN nebyla u pediatrických pacientů zkoumána.
Závod
Farmakokinetické rozdíly způsobené rasou nebyly zjištěny.
Poškození jater
Metabolismus jater tvoří téměř 100 % eliminace přípravku VOLTAREN 100 mg, takže pacienti s onemocněním jater mohou vyžadovat snížené dávky přípravku VOLTAREN 50 mg ve srovnání s pacienty s normální funkcí jater.
Renální poškození
Farmakokinetika diklofenaku byla zkoumána u subjektů s renální insuficiencí. Ve studiích u pacientů s poruchou funkce ledvin nebyly zjištěny žádné rozdíly ve farmakokinetice diklofenaku. U pacientů s poruchou funkce ledvin (clearance inulinu 60 až 90, 30 až 60 a méně než 30 ml/min; N = 6 v každé skupině) byly hodnoty plochy pod křivkou (AUC) a rychlost eliminace srovnatelné s hodnotami u zdravých subjektů .
Studie lékových interakcí
vorikonazol
Při současném podávání s vorikonazolem (inhibitor enzymů CYP2C9, 2C19 a 3A4) se Cmax a AUC diklofenaku zvýšily o 114 % a 78 % (viz DROGOVÉ INTERAKCE ).
Aspirin
Když byly NSAID podávány s aspirinem, vazba NSAID na proteiny byla snížena, ačkoli clearance volného NSAID se nezměnila. Klinický význam této interakce není znám. Viz tabulka 2 pro klinicky významné lékové interakce NSAID s aspirinem (viz DROGOVÉ INTERAKCE ).
INFORMACE PRO PACIENTA
Průvodce léky
VOLTAREN® (Vowl-tar-uhn) (diclofenac sodný) potahované tablety
Jaké jsou nejdůležitější informace, které bych měl vědět o lécích nazývaných nesteroidní protizánětlivé léky (NSAID)?
NSAID mohou způsobit závažné nežádoucí účinky, včetně:
- Zvýšené riziko srdečního infarktu nebo mrtvice, které mohou vést k smrti. Toto riziko se může objevit na začátku léčby a může se zvýšit:
- se zvyšujícími se dávkami NSAID
- při delším užívání NSAID
Neužívejte NSAID těsně před nebo po operaci srdce nazývané „bypass koronární artérie (CABG). Vyhněte se užívání NSAID po nedávném srdečním infarktu, pokud vám to neřekne váš poskytovatel zdravotní péče. Pokud užíváte NSAID po nedávném srdečním infarktu, můžete mít zvýšené riziko dalšího srdečního infarktu.
- Zvýšené riziko krvácení, vředů a trhlin (perforace) jícnu (trubice vedoucí z úst do žaludku), žaludku a střev:
- kdykoliv během používání
- bez varovných příznaků
- které mohou způsobit smrt
Riziko vzniku vředu nebo krvácení se zvyšuje s:
- žaludeční vředy nebo krvácení do žaludku nebo střev při užívání NSAID v minulosti
- užívání léků nazývaných „kortikosteroidy“, „antikoagulancia“, „SSRI“ nebo „SNRI“
- zvyšující se dávky NSAID
- delší užívání NSAID
- kouření
- pití alkoholu
- vyšší věk
- špatný zdravotní stav
- pokročilé onemocnění jater
- problémy s krvácením
NSAID by se měly používat pouze:
- přesně podle předpisu
- v nejnižší možné dávce pro vaši léčbu
- na co nejkratší potřebnou dobu
Co jsou NSAID?
NSAID se používají k léčbě bolesti a zarudnutí, otoku a tepla (zánětu) ze zdravotních stavů, jako jsou různé typy artritidy, menstruační křeče a další typy krátkodobé bolesti.
Kdo by neměl užívat NSAID?
Neužívejte NSAID:
- jestliže jste měl(a) astmatický záchvat, kopřivku nebo jinou alergickou reakci na aspirin nebo jiné NSAID.
- těsně před nebo po operaci bypassu srdce.
Než začnete užívat NSAID, informujte svého poskytovatele zdravotní péče o všech svých zdravotních stavech, včetně toho, zda:
- máte problémy s játry nebo ledvinami
- mají vysoký krevní tlak
- mít astma
- jste těhotná nebo plánujete otěhotnět. Užívání NSAID přibližně ve 20. týdnu těhotenství nebo později může poškodit vaše nenarozené dítě. Pokud potřebujete užívat NSAID déle než 2 dny, když jste mezi 20. a 30. týdnem těhotenství, váš poskytovatel zdravotní péče možná bude muset sledovat množství tekutiny ve vaší děloze kolem vašeho dítěte. Přibližně po 30 týdnech těhotenství byste neměla užívat NSAID.
- kojíte nebo plánujete kojit.
Informujte svého poskytovatele zdravotní péče o všech lécích, které užíváte, včetně léků na předpis nebo volně prodejných léků, vitamínů nebo bylinných doplňků. NSAID a některé další léky se mohou vzájemně ovlivňovat a způsobit závažné nežádoucí účinky. Nezačínejte užívat žádný nový lék, aniž byste si nejprve promluvili se svým poskytovatelem zdravotní péče.
Jaké jsou možné vedlejší účinky NSAID?
NSAID mohou způsobit závažné nežádoucí účinky, včetně:
Viz „Jaké jsou nejdůležitější informace, které bych měl vědět o lécích nazývaných nesteroidní protizánětlivé léky (NSAID)?
- nový nebo horší vysoký krevní tlak
- srdeční selhání
- problémy s játry, včetně selhání jater
- problémy s ledvinami, včetně selhání ledvin
- nízký počet červených krvinek (anémie)
- život ohrožující kožní reakce
- život ohrožující alergické reakce
- Mezi další nežádoucí účinky NSAID patří: bolest žaludku, zácpa, průjem, plynatost, pálení žáhy, nevolnost, zvracení, závratě
Získejte okamžitou pomoc v případě nouze, pokud máte některý z následujících příznaků:
- dušnost nebo potíže s dýcháním
- bolest na hrudi
- slabost v jedné části nebo straně vašeho těla
- nezřetelná řeč
- otok obličeje nebo hrdla
Přestaňte užívat NSAID a okamžitě zavolejte svého poskytovatele zdravotní péče, pokud se u Vás objeví některý z následujících příznaků:
- nevolnost
- zvracet krev
- unavenější nebo slabší než obvykle
- průjem
- svědění
- máte krev ve střevech nebo je černá a lepkavá jako dehet
- vaše kůže nebo oči vypadají žlutě
- poruchy trávení nebo bolesti žaludku
- příznaky podobné chřipce
- neobvyklý nárůst hmotnosti
- kožní vyrážka nebo puchýře s horečkou
- otoky paží a nohou, rukou a nohou
Pokud užijete příliš mnoho NSAID, zavolejte svého poskytovatele zdravotní péče nebo okamžitě vyhledejte lékařskou pomoc.
To nejsou všechny možné vedlejší účinky NSAID. Další informace o NSAID získáte u svého poskytovatele zdravotní péče nebo lékárníka. Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA1088
Další informace o NSAID.
- Aspirin je lék NSAID, ale nezvyšuje riziko srdečního infarktu. Aspirin může způsobit krvácení do mozku, žaludku a střev. Aspirin může také způsobit vředy v žaludku a střevech.
- Některá NSA se prodávají v nižších dávkách bez lékařského předpisu (volně prodejné). Poraďte se se svým poskytovatelem zdravotní péče před používáním volně prodejných NSAID po dobu delší než 10 dní.
Obecné informace o bezpečném a účinném užívání NSAID.
Léky jsou někdy předepisovány pro jiné účely, než které jsou uvedeny v Průvodci léky. Neužívejte NSAID pro stav, pro který nebyly předepsány. Nedávejte NSAID jiným lidem, i když mají stejné příznaky jako vy. Může jim to ublížit.
Pokud byste chtěli více informací o NSAID, promluvte si se svým poskytovatelem zdravotní péče. Můžete požádat svého lékárníka nebo poskytovatele zdravotní péče o informace o NSAID, které jsou určeny pro zdravotníky.
Tato příručka pro léky byla schválena americkým Úřadem pro kontrolu potravin a léčiv. Upraveno: duben 2021
