Tofranil 25mg, 50mg, 75mg Imipramine Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Tofranil a jak se používá?
Tofranil 50 mg je lék na předpis používaný k léčbě příznaků deprese. Tofranil 25 mg lze užívat samostatně nebo s jinými léky.
Tofranil patří do třídy léků nazývaných antidepresiva, TCA.
Není známo, zda je přípravek Tofranil bezpečný a účinný u dětí mladších 6 let.
Jaké jsou možné vedlejší účinky přípravku Tofranil 50 mg?
Tofranil může způsobit závažné nežádoucí účinky, včetně:
- změny nálady nebo chování,
- úzkost,
- panický záchvat,
- problémové spaní,
- impulzivní chování,
- podrážděnost,
- míchání,
- nepřátelství,
- agrese,
- neklid,
- hyperaktivita (psychická nebo fyzická),
- více deprese,
- sebevražedné myšlenky,
- rozmazané vidění,
- tunelové vidění,
- bolest nebo otok očí,
- vidět halo kolem světel,
- točení hlavy,
- nová nebo zhoršující se bolest na hrudi,
- bušení srdce,
- chvění v tvé hrudi,
- náhlá necitlivost nebo slabost,
- problémy se zrakem, řečí nebo rovnováhou,
- horečka,
- bolest krku,
- zmatek,
- halucinace,
- neobvyklé myšlenky nebo chování,
- bolestivé nebo obtížné močení,
- záchvaty a
- zežloutnutí kůže nebo očí (žloutenka)
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější vedlejší účinky přípravku Tofranil patří:
- štiplavý pocit,
- slabost,
- nedostatek koordinace,
- suchá ústa,
- nevolnost,
- zvracení,
- zácpa,
- průjem,
- změny vidění,
- zvoní ti v uších,
- zpevnění prsou (u mužů i žen),
- snížená chuť na sex,
- impotence a
- potíže s orgasmem
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky přípravku Tofranil. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Sebevražednost a antidepresiva
Antidepresiva ve srovnání s placebem zvýšila riziko sebevražedného myšlení a chování (suicidality) u dětí, dospívajících a mladých dospělých v krátkodobých studiích velké depresivní poruchy (MDD) a dalších psychiatrických poruch. Každý, kdo zvažuje použití imipramin hydrochloridu nebo jakéhokoli jiného antidepresiva u dětí, dospívajících nebo mladých dospělých, musí toto riziko vyvážit klinickou potřebou. Krátkodobé studie neprokázaly u dospělých starších 24 let zvýšení rizika sebevraždy u antidepresiv ve srovnání s placebem; došlo ke snížení rizika u antidepresiv ve srovnání s placebem u dospělých ve věku 65 let a starších. Deprese a některé další psychiatrické poruchy jsou samy o sobě spojeny se zvýšeným rizikem sebevraždy. Pacienti všech věkových kategorií, u kterých je zahájena léčba antidepresivy, by měli být náležitě sledováni a pečlivě sledováni z hlediska klinického zhoršení, suicidality nebo neobvyklých změn v chování. Rodiny a pečovatelé by měli být informováni o nutnosti pečlivého pozorování a komunikace s předepisujícím lékařem. Imipramin hydrochlorid není schválen pro použití u pediatrických pacientů (viz VAROVÁNÍ Klinické zhoršení a riziko sebevraždy; OPATŘENÍ Informace pro pacienty; a OPATŘENÍ , Pediatrické použití).
POPIS
Tofranil™ je dodáván ve formě tablet pro perorální podání.
Tofranil 75 mg, imipramin hydrochlorid USP, původní tricyklické antidepresivum, je členem skupiny dibenzazepinů. Označuje se jako monohydrochlorid 5-3-(dimethylamino)propyl-10,11-dihydro-5Hdibenz[b,f]-azepinu. Jeho strukturní vzorec je:
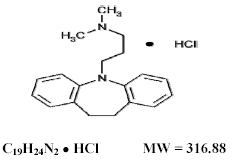
Imipramin hydrochlorid USP je bílý až téměř bílý krystalický prášek bez zápachu nebo prakticky bez zápachu. Je volně rozpustný ve vodě a v alkoholu, rozpustný v acetonu, nerozpustný v etheru a benzenu.
Neaktivní ingredience
Fosforečnan vápenatý, sloučeniny celulózy, dokusát sodný, oxidy železa, stearát hořečnatý, polyethylenglykol, povidon, sodná sůl glykolátu škrobu, sacharóza, mastek a oxid titaničitý.
INDIKACE
Deprese
Pro zmírnění příznaků deprese. Endogenní deprese bude pravděpodobněji zmírněna než jiné depresivní stavy. Než budou patrné optimální terapeutické účinky, může být zapotřebí jeden až tři týdny léčby.
Enuréza v dětství
Může být užitečný jako dočasná doplňková terapie při snižování enurézy u dětí ve věku 6 let a starších poté, co byly příslušnými testy vyloučeny možné organické příčiny. U pacientů s denními symptomy frekvence a urgence by vyšetření mělo zahrnovat mikční cystouretrografii a cystoskopii, je-li to nutné. Účinnost léčby se může s pokračujícím podáváním léků snižovat.
DÁVKOVÁNÍ A PODÁVÁNÍ
Deprese
U starších pacientů a dospívajících se doporučují nižší dávky. Nižší dávky se také doporučují ambulantním pacientům ve srovnání s hospitalizovanými pacienty, kteří budou pod pečlivým dohledem. Dávkování by mělo být zahájeno na nízké úrovni a mělo by se postupně zvyšovat, přičemž je třeba pečlivě sledovat klinickou odpověď a jakékoli známky intolerance. Po remisi může být nutná udržovací medikace po delší dobu, v nejnižší dávce, která udrží remisi.
Obvyklá dávka pro dospělé
Hospitalizovaní pacienti
Zpočátku se 100 mg/den v rozdělených dávkách postupně podle potřeby zvyšovalo na 200 mg/den. Pokud po dvou týdnech nedojde k žádné odpovědi, zvyšte dávku na 250 až 300 mg/den.
Ambulantní pacienti
Zpočátku se 75 mg/den zvýšilo na 150 mg/den. Dávky nad 200 mg/den se nedoporučují. Udržovací dávka 50 až 150 mg/den.
Dospívající a geriatričtí pacienti
Zpočátku 30 až 40 mg/den; obecně není nutné překročit 100 mg/den.
Enuréza v dětství
Zpočátku by měla být u dětí ve věku 6 let a starších vyzkoušena perorální dávka 25 mg/den. Lék by měl být podáván jednu hodinu před spaním. Pokud nedojde k uspokojivé odpovědi do jednoho týdne, zvyšte dávku na 50 mg na noc u dětí do 12 let; děti starší 12 let mohou dostávat až 75 mg na noc. Denní dávka vyšší než 75 mg nezvyšuje účinnost a má tendenci zvyšovat nežádoucí účinky. Důkazy naznačují, že u nočních pomočovačů je lék účinnější podaný dříve a v rozdělených dávkách, tj. 25 mg v poledne, opakované před spaním. Je třeba zvážit zavedení období bez léku po adekvátní terapeutické studii s příznivou odpovědí. Dávkování by mělo být postupně snižováno spíše než náhle vysazeno; to může snížit tendenci k relapsu. Děti, u kterých dojde po vysazení léku k relapsu, ne vždy reagují na následnou léčbu.
Dávka 2,5 mg/kg/den by neměla být překročena. Změny na EKG neznámého významu byly hlášeny u pediatrických pacientů při dávkách dvojnásobku tohoto množství.
Bezpečnost a účinnost přípravku Tofranil jako dočasné doplňkové léčby noční enurézy u dětí mladších 6 let nebyla stanovena.
JAK DODÁVÁNO
Tři síly Tofranil™ (imipramin hydrochlorid USP) jsou dostupné následovně:
– trojúhelníková, bikonvexní, korálově červenohnědá, cukrem potažená tableta s černým potiskem na jedné straně a „10“ na druhé straně.
Láhve po 30 NDC 0406-9920-03 Láhve po 100 ks NDC 0406-9920-01
– kulatá bikonvexní korálově červenohnědá potahovaná tableta s černým potiskem na jedné straně a „25“ na druhé straně.
Láhve po 30 NDC 0406-9921-03 Láhve po 100 ks NDC 0406-9921-01
– kulatá bikonvexní korálově červenohnědá potahovaná tableta s černým potiskem na jedné straně a „50“ na druhé straně.
Láhve po 30 NDC 0406-9922-03 Láhve po 100 ks NDC 0406-9922-01
Skladujte při 20° až 25°C (68° až 77°F) [viz USP Regulovaná pokojová teplota].
Dávkujte v těsné nádobě (USP) s dětským bezpečnostním uzávěrem.
Výrobce: Patheon Inc. Whitby, Ontario, Kanada, L1N 5Z5. Revize: duben 2017
VEDLEJŠÍ EFEKTY
Poznámka – Přestože následující seznam obsahuje několik nežádoucích účinků, které nebyly hlášeny u tohoto konkrétního léku, farmakologické podobnosti mezi tricyklickými antidepresivy vyžadují, aby byla při podávání přípravku Tofranil 25 mg zvážena každá z reakcí.
Kardiovaskulární: Ortostatická hypotenze, hypertenze, tachykardie, palpitace, infarkt myokardu, arytmie, srdeční blok, změny EKG, precipitace městnavého srdečního selhání, cévní mozková příhoda.
psychiatrické: Stavy zmatenosti (zejména u starších osob) s halucinacemi, dezorientací, bludy; úzkost, neklid, agitovanost; nespavost a noční můry; hypománie; exacerbace psychózy.
Neurologický: Necitlivost, brnění, parestézie končetin; poruchy koordinace, ataxie, třes; periferní neuropatie; extrapyramidové příznaky; záchvaty, změny ve vzorcích EEG; tinnitus.
Anticholinergní: Sucho v ústech a vzácně související sublingvální adenitida; rozmazané vidění, poruchy akomodace, mydriáza; zácpa, paralytický ileus; retence moči, opožděná mikce, dilatace močových cest.
Alergický: Kožní vyrážka, petechie, kopřivka, svědění, fotosenzitizace; edém (celkový nebo obličeje a jazyka); drogová horečka; zkřížená citlivost s desipraminem.
Hematologické: útlum kostní dřeně včetně agranulocytózy; eozinofilie; purpura; trombocytopenie.
Gastrointestinální: Nevolnost a zvracení, anorexie, epigastrické potíže, průjem; zvláštní chuť, stomatitida, křeče v břiše, černý jazyk.
Endokrinní: gynekomastie u mužů; zvětšení prsou a galaktorea u žen; zvýšené nebo snížené libido, impotence; otok varlat; zvýšení nebo snížení hladiny cukru v krvi; syndrom nepřiměřené sekrece antidiuretického hormonu (ADH).
Jiný: Žloutenka (simulující obstrukční); změněná funkce jater; přírůstek nebo ztráta hmotnosti; pocení; proplachování; frekvence močení; ospalost, závratě, slabost a únava; bolest hlavy; otok příušní žlázy; alopecie; náchylnost k pádu.
Abstinenční příznaky: I když to neznamená závislost, náhlé ukončení léčby po dlouhodobé léčbě může způsobit nevolnost, bolest hlavy a malátnost.
Poznámka – U enuretických dětí léčených přípravkem Tofranil 75 mg byly nejčastějšími nežádoucími účinky nervozita, poruchy spánku, únava a mírné gastrointestinální poruchy. Tyto obvykle vymizí během pokračujícího podávání léku nebo při snížení dávky. Mezi další reakce, které byly hlášeny, patří zácpa, křeče, úzkost, emoční nestabilita, synkopa a kolaps. Je třeba vzít v úvahu všechny nežádoucí účinky hlášené při užívání u dospělých.
DROGOVÉ INTERAKCE
Léky metabolizované P450 2D6
Biochemická aktivita izozymu cytochromu P450 2D6 (debrisochin hydroxyláza) metabolizujícího léčivo je u podskupiny kavkazské populace snížena (asi 7 až 10 % bělochů jsou tzv. „špatní metabolizátoři“); spolehlivé odhady prevalence snížené aktivity izoenzymu P450 2D6 mezi asijskými, africkými a dalšími populacemi zatím nejsou k dispozici. Špatní metabolizátoři mají při podávání obvyklých dávek vyšší plazmatické koncentrace tricyklických antidepresiv (TCA), než se očekávalo. V závislosti na frakci léčiva metabolizovaného P450 2D6 může být zvýšení plazmatické koncentrace malé nebo poměrně velké (8násobné zvýšení plazmatické AUC TCA).
Některá léčiva navíc inhibují aktivitu tohoto isozymu a dělají normální metabolizátory podobné pomalým metabolizátorům. Jednotlivec, který je stabilní na dané dávce TCA, se může stát náhle toxickým, když je mu současně podáván jeden z těchto inhibičních léků. Mezi léky, které inhibují cytochrom P450 2D6, patří některé, které nejsou metabolizovány enzymem (chinidin; cimetidin) a mnohé, které jsou substráty pro P450 2D6 (mnoho dalších antidepresiv, fenothiaziny a antiarytmika typu 1C propafenon a flekainid). Zatímco všechny selektivní inhibitory zpětného vychytávání serotoninu (SSRI), např. fluoxetin, sertralin a paroxetin, inhibují P450 2D6, mohou se lišit v rozsahu inhibice. Rozsah, v jakém může interakce SSRI-TCA představovat klinické problémy, bude záviset na stupni inhibice a farmakokinetice příslušného SSRI. Přesto je třeba opatrnosti při současném podávání TCA s kterýmkoli ze SSRI a také při přechodu z jedné třídy na druhou. Obzvláště důležité je, že před zahájením léčby TCA u pacienta, kterému je fluoxetin vysazen, musí uplynout dostatečná doba vzhledem k dlouhému poločasu mateřského a aktivního metabolitu (může být zapotřebí alespoň 5 týdnů).
Současné užívání tricyklických antidepresiv s léky, které mohou inhibovat cytochrom P450 2D6, může vyžadovat nižší dávky, než jsou obvykle předepisovány buď pro tricyklické antidepresivum, nebo pro jiný lék. Kromě toho, kdykoli je jedno z těchto dalších léků vysazeno z souběžné léčby, může být vyžadována zvýšená dávka tricyklického antidepresiva. Je žádoucí monitorovat plazmatické hladiny TCA, kdykoli se má TCA podávat společně s jiným lékem, o kterém je známo, že je inhibitorem P450 2D6.
Plazmatická koncentrace imipraminu se může zvýšit, pokud je lék podáván současně s inhibitory jaterních enzymů (např. cimetidin, fluoxetin) a klesnout při současném podávání s induktory jaterních enzymů (např. barbituráty, fenytoin), a proto může úprava dávkování imipraminu být nutné.
příležitostně citlivých pacientů nebo u těch, kteří dostávají anticholinergní léky (včetně antiparkinsonických léků), se navíc mohou účinky podobné atropinu zvýraznit (např. paralytický ileus). Je-li imipramin-hydrochlorid podáván současně s anticholinergními léky, je nutný pečlivý dohled a pečlivá úprava dávkování.
Vyhněte se používání přípravků, jako jsou dekongestanty a lokální anestetika, které obsahují jakýkoli sympatomimetický amin (např. adrenalin, norepinefrin), protože bylo hlášeno, že tricyklická antidepresiva mohou zesilovat účinky katecholaminů.
Při použití imipramin-hydrochloridu s látkami, které snižují krevní tlak, je třeba opatrnosti. Imipramin hydrochlorid může zesilovat účinky léků tlumících CNS.
Pacienti by měli být upozorněni, že imipramin-hydrochlorid může zvýšit tlumivé účinky alkoholu na CNS (viz VAROVÁNÍ ).
VAROVÁNÍ
Klinické zhoršení a riziko sebevraždy
pacientů s velkou depresivní poruchou (MDD), dospělých i dětí, může dojít ke zhoršení jejich deprese a/nebo objevení se sebevražedných myšlenek a chování (suicidality) nebo neobvyklých změn v chování, ať už užívají antidepresiva či nikoli, a to riziko může přetrvávat, dokud nedojde k významné remisi. Sebevražda je známým rizikem deprese a některých dalších psychiatrických poruch a tyto poruchy samy o sobě jsou nejsilnějšími prediktory sebevraždy. Existuje však dlouhotrvající obava, že antidepresiva mohou hrát roli při navození zhoršení deprese a vzniku suicidality u některých pacientů během raných fází léčby. Souhrnné analýzy krátkodobých placebem kontrolovaných studií antidepresiv (SSRI a další) ukázaly, že tyto léky zvyšují riziko sebevražedného myšlení a chování (sebevražednost) u dětí, dospívajících a mladých dospělých (ve věku 18 až 24 let) s těžkou depresivní poruchou. poruchy (MDD) a další psychiatrické poruchy. Krátkodobé studie neprokázaly u dospělých starších 24 let zvýšení rizika sebevraždy u antidepresiv ve srovnání s placebem; došlo ke snížení u antidepresiv ve srovnání s placebem u dospělých ve věku 65 let a starších.
Souhrnné analýzy placebem kontrolovaných studií u dětí a dospívajících s MDD, obsedantně kompulzivní poruchou (OCD) nebo jinými psychiatrickými poruchami zahrnovaly celkem 24 krátkodobých studií s 9 antidepresivy u více než 4400 pacientů. Souhrnné analýzy placebem kontrolovaných studií u dospělých s MDD nebo jinými psychiatrickými poruchami zahrnovaly celkem 295 krátkodobých studií (medián trvání 2 měsíce) s 11 antidepresivy u více než 77 000 pacientů. Mezi drogami existovaly značné rozdíly v riziku sebevraždy, ale téměř u všech zkoumaných drog byla tendence ke zvýšení počtu mladších pacientů. Mezi různými indikacemi byly rozdíly v absolutním riziku suicidality, s nejvyšší incidencí u MDD. Rozdíly v riziku (lék vs. placebo) však byly relativně stabilní v rámci věkových skupin a napříč indikacemi. Tyto rizikové rozdíly (rozdíl lék-placebo v počtu případů sebevraždy na 1000 léčených pacientů) jsou uvedeny v tabulce 1.
žádné z pediatrických studií nedošlo k žádné sebevraždě. Ve studiích s dospělými se vyskytly sebevraždy, ale počet nebyl dostatečný k tomu, aby se dospělo k nějakému závěru o účinku drogy na sebevraždu.
Není známo, zda se riziko sebevraždy rozšiřuje i na dlouhodobé užívání, tj. déle než několik měsíců. Existují však podstatné důkazy z placebem kontrolovaných udržovacích studií u dospělých s depresí, že užívání antidepresiv může oddálit recidivu deprese.
Všichni pacienti léčení antidepresivy pro jakoukoli indikaci by měli být náležitě sledováni a pečlivě sledováni z hlediska klinického zhoršení, suicidality a neobvyklých změn v chování, zejména během prvních několika měsíců lékové terapie nebo v době změny dávky, buď zvýšení nebo klesá.
Následující příznaky, úzkost, agitovanost, záchvaty paniky, nespavost, podrážděnost, nepřátelství, agresivita, impulzivita, akatizie (psychomotorický neklid), hypománie a mánie, byly hlášeny také u dospělých a dětských pacientů léčených antidepresivy pro těžkou depresivní poruchu co se týče dalších indikací, psychiatrických i nepsychiatrických. Ačkoli příčinná souvislost mezi vznikem takových symptomů a buď zhoršením deprese a/nebo vznikem sebevražedných impulzů nebyla prokázána, existuje obava, že takové symptomy mohou představovat prekurzory objevující se sebevraždy.
Je třeba zvážit změnu terapeutického režimu, včetně možného přerušení léčby, u pacientů, jejichž deprese se trvale zhoršuje, nebo u kterých se objevuje náhlá sebevražda nebo symptomy, které mohou být předzvěstí zhoršení deprese nebo sebevražednosti, zvláště pokud jsou tyto příznaky závažné, náhlé na začátku nebo nebyly součástí symptomů pacienta.
Rodiny a ošetřovatelé pacientů léčených antidepresivy pro těžkou depresivní poruchu nebo jiné indikace, psychiatrické i nepsychiatrické, by měli být upozorněni na nutnost sledovat pacienty, zda se u nich neobjeví agitovanost, podrážděnost, neobvyklé změny v chování a další příznaky popsané výše. , jakož i vznik suicidality, a takové příznaky neprodleně hlásit poskytovatelům zdravotní péče. Takové sledování by mělo zahrnovat každodenní pozorování ze strany rodin a pečovatelů. Předpisy pro imipramin hydrochlorid by měly být napsány na nejmenší množství tablet v souladu s dobrou léčbou pacienta, aby se snížilo riziko předávkování.
Screening pacientů na bipolární poruchu
Velká depresivní epizoda může být počátečním projevem bipolární poruchy. Obecně se má za to (ačkoli to nebylo prokázáno v kontrolovaných studiích), že léčba takové epizody samotným antidepresivem může zvýšit pravděpodobnost precipitace smíšené/manické epizody u pacientů s rizikem bipolární poruchy. Není známo, zda některý z výše popsaných příznaků představuje takovou konverzi. Před zahájením léčby antidepresivy by však pacienti s depresivními symptomy měli být adekvátně vyšetřeni, aby se zjistilo, zda jsou ohroženi bipolární poruchou; takový screening by měl zahrnovat podrobnou psychiatrickou anamnézu, včetně rodinné anamnézy sebevraždy, bipolární poruchy a deprese. Je třeba poznamenat, že imipramin hydrochlorid není schválen pro použití při léčbě bipolární deprese.
Glaukom s uzavřeným úhlem
Rozšíření zornice, ke kterému dochází po použití mnoha antidepresiv včetně Tofranilu, může vyvolat záchvat s uzavřeným úhlem u pacienta s anatomicky úzkými úhly, který nemá patentovanou iridektomii.
Děti
V dětství by neměla být překročena dávka 2,5 mg/kg/den přípravku Tofranil 25 mg. Změny na EKG neznámého významu byly hlášeny u pediatrických pacientů při dávkách dvojnásobku tohoto množství.
Extrémní opatrnosti je třeba při podávání tohoto léku: pacientům s kardiovaskulárním onemocněním kvůli možnosti převodních poruch, arytmií, městnavého srdečního selhání, infarktu myokardu, mrtvice a tachykardie. Tito pacienti vyžadují sledování srdce při všech úrovních dávkování léku;
pacienti s anamnézou retence moči nebo anamnézou glaukomu s úzkým úhlem kvůli anticholinergním vlastnostem léku; pacienti s hypertyreózou nebo pacienti užívající léky na štítnou žlázu kvůli možnosti kardiovaskulární toxicity;
pacienti s anamnézou záchvatové poruchy, protože bylo prokázáno, že tento lék snižuje práh záchvatů;
pacienti užívající guanetidin, klonidin nebo podobné látky, protože Tofranil může blokovat farmakologické účinky těchto léků;
pacientů užívajících methylfenidát-hydrochlorid. Vzhledem k tomu, že methylfenidát-hydrochlorid může inhibovat metabolismus Tofranilu 75 mg, může být nutná úprava dávky imipramin-hydrochloridu směrem dolů, pokud je podáván současně s methylfenidát-hydrochloridem.
Tofranil může zvýšit tlumivé účinky alkoholu na CNS. Proto je třeba mít na paměti, že nebezpečí spojené s pokusem o sebevraždu nebo náhodným předávkováním lékem se může zvýšit u pacienta, který užívá nadměrné množství alkoholu (viz OPATŘENÍ ).
Vzhledem k tomu, že přípravek Tofranil může narušit duševní a/nebo fyzické schopnosti potřebné pro provádění potenciálně nebezpečných úkolů, jako je řízení automobilu nebo strojů, je třeba pacienta náležitě upozornit.
OPATŘENÍ
Všeobecné
EKG záznam by měl být pořízen před zahájením podávání vyšších než obvyklých dávek Tofranilu a poté ve vhodných intervalech, dokud není dosaženo ustáleného stavu. (Pacienti s jakýmikoli známkami kardiovaskulárního onemocnění vyžadují srdeční dohled při všech úrovních dávkování léku. Viz VAROVÁNÍ .) Starší pacienti a pacienti se srdečním onemocněním nebo s předchozím srdečním onemocněním jsou vystaveni zvláštnímu riziku rozvoje srdečních abnormalit spojených s užíváním Tofranilu.
Je třeba mít na paměti, že možnost sebevraždy u vážně depresivních pacientů je vlastní nemoci a může přetrvávat, dokud nedojde k významné remisi. Tito pacienti by měli být během rané fáze léčby přípravkem Tofranil 75 mg pečlivě sledováni a mohou vyžadovat hospitalizaci. Předpisy by měly být napsány na nejmenší možné množství. Mohou se objevit hypomanické nebo manické epizody, zejména u pacientů s cyklickými poruchami. Takové reakce mohou vyžadovat přerušení léčby. V případě potřeby lze Tofranil 75 mg obnovit v nižší dávce, jakmile tyto epizody pominou.
Podávání trankvilizéru může být užitečné při kontrole takových epizod.
U schizofrenních pacientů může být příležitostně pozorována aktivace psychózy a může vyžadovat snížení dávky a přidání fenothiazinu.
Současné podávání přípravku Tofranil 50 mg s terapií elektrošoky může zvýšit rizika; taková léčba by měla být omezena na pacienty, pro které je nezbytná, protože klinické zkušenosti jsou omezené.
Pacienti užívající imipramin hydrochlorid by se měli vyhýbat nadměrnému vystavení slunečnímu záření, protože byly hlášeny případy fotosenzibilizace.
Při užívání imipramin-hydrochloridu bylo hlášeno zvýšení i snížení hladiny cukru v krvi.
Imipramin-hydrochlorid by měl být používán s opatrností u pacientů s významně narušenou funkcí ledvin nebo jater.
Pacienti, u kterých se během léčby imipramin-hydrochloridem objeví horečka a bolest v krku, by měli mít vyšetřeny leukocyty a diferenciální krevní obraz. Imipramin-hydrochlorid by měl být vysazen, pokud je prokázána patologická deprese neutrofilů.
Před elektivním chirurgickým zákrokem by měla být léčba imipramin-hydrochloridem přerušena tak dlouho, jak to klinická situace dovolí.
Informace pro pacienty
Předepisující lékaři nebo jiní zdravotničtí pracovníci by měli informovat pacienty, jejich rodiny a jejich pečovatele o výhodách a rizicích spojených s léčbou imipramin-hydrochloridem a měli by jim poradit, jak správně používat. Pacient Průvodce léky o "antidepresivních lécích, depresi a jiných vážných duševních onemocněních a sebevražedných myšlenkách nebo akcích" je k dispozici pro imipramin hydrochlorid. Předepisující lékař nebo zdravotnický pracovník by měl poučit pacienty, jejich rodiny a pečovatele, aby si přečetli Příručku o medikaci, a měl by jim pomoci porozumět jejímu obsahu. Pacienti by měli mít příležitost prodiskutovat obsah Příručky pro léky a získat odpovědi na případné otázky. Úplný text Příručky k medikaci je přetištěn na konci tohoto dokumentu.
Pacienti by měli být informováni o následujících problémech a měli by být požádáni, aby upozornili svého předepisujícího lékaře, pokud k nim dojde během užívání imipramin-hydrochloridu.
Pacienti by měli být poučeni, že užívání přípravku Tofranil může způsobit mírnou dilataci zornic, která u citlivých jedinců může vést k epizodě glaukomu s uzavřeným úhlem. Preexistující glaukom je téměř vždy glaukom s otevřeným úhlem, protože glaukom s uzavřeným úhlem, pokud je diagnostikován, může být definitivně léčen iridektomií. Glaukom s otevřeným úhlem není rizikovým faktorem pro glaukom s uzavřeným úhlem. Pacienti si mohou přát, aby byli vyšetřeni, aby se zjistilo, zda jsou náchylní k uzavření úhlu, a pokud jsou citliví, podstoupí profylaktický postup (např. iridektomie).
Klinické zhoršení a riziko sebevraždy
Pacienti, jejich rodiny a jejich pečovatelé by měli být upozorněni na výskyt úzkosti, agitovanosti, záchvatů paniky, nespavosti, podrážděnosti, nepřátelství, agresivity, impulzivity, akatizie (psychomotorický neklid), hypománie, mánie a dalších neobvyklých změn v chování. zhoršení deprese a sebevražedných myšlenek, zejména na začátku léčby antidepresivy a při zvyšování nebo snižování dávky. Rodiny a pečovatelé pacientů by měli být poučeni, aby každý den hledali výskyt těchto příznaků, protože změny mohou být náhlé. Takové příznaky by měly být hlášeny pacientovu předepisujícímu lékaři nebo zdravotníkovi, zejména pokud jsou závažné, začínají náhle nebo nejsou součástí pacientových příznaků. Příznaky, jako jsou tyto, mohou být spojeny se zvýšeným rizikem sebevražedného myšlení a chování a naznačují potřebu velmi pečlivého sledování a možné změny v léčbě.
Těhotenství
Reprodukční studie na zvířatech přinesly neprůkazné výsledky (viz také Farmakologie zvířat ).
Nebyly provedeny žádné dobře kontrolované studie s těhotnými ženami, které by určily účinek přípravku Tofranil na plod. Existují však klinické zprávy o vrozených malformacích spojených s užíváním léku. Ačkoli nebylo možné stanovit příčinnou souvislost mezi těmito účinky a lékem, nelze vyloučit možnost rizika pro plod při požití Tofranilu matkou. Proto by měl být Tofranil podáván ženám, které jsou nebo mohou otěhotnět, pouze pokud klinický stav jasně odůvodňuje potenciální riziko pro plod.
Kojící matky
Omezené údaje naznačují, že Tofranil 75 mg je pravděpodobně vylučován do lidského mateřského mléka. Obecně platí, že žena užívající lék by neměla kojit, protože existuje možnost, že lék může být vylučován do mateřského mléka a být škodlivý pro dítě.
Pediatrické použití
Bezpečnost a účinnost u jiné pediatrické populace než u pediatrických pacientů s noční enurézou nebyla stanovena (viz BOX VAROVÁNÍ a VAROVÁNÍ , Klinické zhoršení a riziko sebevraždy ). Každý, kdo zvažuje použití imipramin-hydrochloridu u dětí nebo dospívajících, musí vyvážit potenciální rizika s klinickou potřebou.
Bezpečnost a účinnost léku jako dočasné doplňkové léčby noční enurézy u pediatrických pacientů mladších 6 let nebyla stanovena.
Bezpečnost léku pro dlouhodobé, chronické použití jako doplňková léčba noční enurézy u pediatrických pacientů ve věku 6 let nebo starších nebyla stanovena; je třeba zvážit zavedení období bez léku po adekvátní terapeutické studii s příznivou odpovědí.
V dětství by neměla být překročena dávka 2,5 mg/kg/den. Změny na EKG neznámého významu byly hlášeny u pediatrických pacientů při dávkách dvojnásobku tohoto množství.
Geriatrické použití
literatuře byly provedeny čtyři dobře kontrolované, randomizované, dvojitě zaslepené, srovnávací klinické studie paralelních skupin provedené s Tofranilem 50 mg u starší populace. Do těchto studií bylo zahrnuto celkem 651 subjektů. Tyto studie neposkytly srovnání s mladšími subjekty. U starších pacientů nebyly zjištěny žádné další nežádoucí účinky.
Klinické studie přípravku Tofranil 75 mg v původní žádosti nezahrnovaly dostatečný počet subjektů ve věku 65 let a více, aby bylo možné určit, zda reagují odlišně od mladších subjektů. Postmarketingové klinické zkušenosti nezjistily rozdíly v odpovědích mezi staršími a mladšími subjekty. Obecně by měl být výběr dávky pro starší osoby opatrný, obvykle začínající na spodní hranici dávkovacího rozmezí, což odráží vyšší frekvenci snížené funkce jater, ledvin nebo srdce a souběžného onemocnění nebo jiné lékové terapie.
(Viz také DÁVKOVÁNÍ A PODÁVÁNÍ , Puberťák a Geriatričtí pacienti .)
(Viz také OPATŘENÍ , Všeobecné. )
PŘEDÁVKOVAT
důsledku předávkování touto třídou léků může dojít k úmrtí. Při úmyslném předávkování tricyklickými látkami je běžné požití více drog (včetně alkoholu). Vzhledem k tomu, že řízení je složité a mění se, doporučuje se, aby lékař kontaktoval toxikologické centrum pro aktuální informace o léčbě. Příznaky a příznaky toxicity se po předávkování tricyklickými látkami rychle rozvíjejí. Proto je nutné co nejrychlejší sledování v nemocnici.
Děti byly hlášeny jako citlivější než dospělí na akutní předávkování imipramin-hydrochloridem. Akutní předávkování jakýmkoliv množstvím u kojenců nebo malých dětí, zvláště, musí být považováno za závažné a potenciálně smrtelné.
Projevy
Ty se mohou lišit v závažnosti v závislosti na faktorech, jako je množství absorbovaného léku, věk pacienta a interval mezi požitím léku a začátkem léčby. Mezi kritické projevy předávkování patří srdeční dysrytmie, těžká hypotenze, křeče a deprese CNS včetně kómatu. Změny na elektrokardiogramu, zejména v ose nebo šířce QRS, jsou klinicky významnými indikátory tricyklické toxicity.
Další CNS projevy mohou zahrnovat ospalost, strnulost, ataxii, neklid, agitovanost, hyperaktivní reflexy, svalovou rigiditu, atetoidní a choreiformní pohyby.
Srdeční abnormality mohou zahrnovat tachykardii a známky městnavého selhání. Může být také přítomna respirační deprese, cyanóza, šok, zvracení, hyperpyrexie, mydriáza a diaforéza.
Řízení
Získejte EKG a okamžitě zahajte monitorování srdce. Chraňte pacientovy dýchací cesty, zaveďte intravenózní hadičku a zahajte dekontaminaci žaludku. Je nutné minimálně 6 hodin pozorování s monitorováním srdce a sledováním známek CNS nebo respirační deprese, hypotenze, srdečních dysrytmií a/nebo převodních bloků a záchvatů. Pokud se kdykoli během tohoto období objeví známky toxicity, je nutné dlouhodobé sledování. Existují kazuistiky pacientů, kteří podlehli fatálním dysrytmiím pozdě po předávkování; tito pacienti měli před smrtí klinické známky významné otravy a většina z nich byla dekontaminována gastrointestinálním traktem. Sledování plazmatických hladin léčiva by nemělo vést k léčbě pacienta.
Gastrointestinální dekontaminace
Všichni pacienti s podezřením na předávkování tricyklickými látkami by měli dostat gastrointestinální dekontaminaci. To by mělo zahrnovat výplach žaludku ve velkém objemu následovaný aktivním uhlím. Pokud je vědomí narušeno, je třeba před výplachem zajistit dýchací cesty. Emese je kontraindikována.
Kardiovaskulární
Maximální trvání QRS z končetiny ≥ 0,10 sekundy může být nejlepším ukazatelem závažnosti předávkování. K udržení pH séra v rozmezí 7,45 až 7,55 by měl být použit intravenózní hydrogenuhličitan sodný. Pokud je reakce na pH nedostatečná, lze také použít hyperventilaci. Současné užívání hyperventilace a hydrogenuhličitanu sodného by mělo být prováděno s extrémní opatrností, s častým monitorováním pH. pH >7,60 nebo pCO2
Ve vzácných případech může být hemoperfuze prospěšná při akutní refrakterní kardiovaskulární nestabilitě u pacientů s akutní toxicitou. Nicméně hemodialýza, peritoneální dialýza, výměnné transfuze a nucená diuréza byly obecně hlášeny jako neúčinné při tricyklické otravě.
CNS
pacientů s útlumem CNS se doporučuje časná intubace kvůli možnosti náhlého zhoršení. Záchvaty by měly být kontrolovány benzodiazepiny, nebo pokud jsou neúčinné, jinými antikonvulzivními látkami (např. fenobarbitalem, fenytoinem). Fysostigmin se nedoporučuje kromě léčby život ohrožujících příznaků, které nereagují na jiné terapie, a to pouze po konzultaci s toxikologickým centrem.
Psychiatrické sledování
Vzhledem k tomu, že předávkování je často záměrné, mohou se pacienti během fáze zotavení pokusit o sebevraždu jinými způsoby. Vhodné může být doporučení psychiatra.
Pediatrický management
Principy léčby předávkování dětmi a dospělými jsou podobné. Důrazně se doporučuje, aby lékař kontaktoval místní toxikologické centrum pro konkrétní pediatrickou léčbu.
KONTRAINDIKACE
Současné použití sloučenin inhibujících monoaminooxidázu je kontraindikováno. U pacientů užívajících takové kombinace se mohou objevit hyperpyretické krize nebo těžké křečové záchvaty. Zesílení nežádoucích účinků může být vážné nebo dokonce smrtelné. Pokud je žádoucí nahradit Tofranil u pacientů užívajících inhibitor monoaminooxidázy, měl by uplynout tak dlouhý interval, jak to klinická situace dovolí, minimálně 14 dní. Počáteční dávka by měla být nízká a zvyšování by mělo být postupné a opatrně předepisováno.
Lék je kontraindikován v období akutního zotavení po infarktu myokardu. Pacientům se známou přecitlivělostí na tuto sloučeninu by lék neměl být podáván. Je třeba mít na paměti možnost zkřížené citlivosti na jiné dibenzazepinové sloučeniny.
KLINICKÁ FARMAKOLOGIE
Mechanismus účinku přípravku Tofranil 25 mg není definitivně znám. Nepůsobí však primárně stimulací centrálního nervového systému. Předpokládá se, že klinický účinek je způsoben zesílením adrenergních synapsí blokováním vychytávání norepinefrinu na nervových zakončeních. Předpokládá se, že způsob účinku léku při kontrole dětské enurézy je odlišný od jeho antidepresivního účinku.
Farmakologie a toxikologie zvířat
A. Akutní
Orální rozsahy LD50 jsou následující:
Krysa 355 až 682 mg/kg Pes 100 až 215 mg/kg
V závislosti na dávce u obou druhů toxické příznaky postupovaly od deprese, nepravidelného dýchání a ataxie až po křeče a smrt.
B. Reprodukce/Teratogenní
Celkové hodnocení lze shrnout takto:
Orální: Nezávislé studie na třech druzích (krysa, myš a králík) odhalily, že když je Tofranil podáván perorálně v dávkách až přibližně 2-1/2násobku maximální dávky u lidí u prvních 2 druhů a až 25násobku maximální dávky u lidí dávka u třetího druhu je léčivo v podstatě bez teratogenního potenciálu. U tří studovaných druhů se vyskytl pouze jeden případ fetální abnormality (u králíka) a v této studii byla rovněž abnormalita v kontrolní skupině. Ze studií na potkanech však existují důkazy, že určitý systémový a embryotoxický potenciál je prokazatelný. To se projevuje snížením velikosti vrhu, mírným zvýšením mrtvě narozených dětí a snížením průměrné porodní hmotnosti.
