Cleocin 150mg, 300mg Clindamycin Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co jsou Cleocin 300mg hydrochloridové kapsle?
Cleocin Hydrochloride Capsules obsahují antibiotikum indikované k léčbě závažných infekcí způsobených citlivými anaerobními bakteriemi. Cleocin 150 mg hydrochlorid je také indikován k léčbě závažných infekcí způsobených citlivými kmeny streptokoků, pneumokoků a stafylokoků. Jeho použití by mělo být vyhrazeno pro pacienty s alergií na penicilin nebo jiné pacienty, pro které je podle úsudku lékaře penicilin nevhodný. Cleocin hydrochlorid je dostupný v generické formě.
Jaké jsou vedlejší účinky přípravku Cleocin 300 mg hydrochloridové kapsle?
Časté vedlejší účinky Cleocin hydrochloridu zahrnují:
- Clostridium difficile kolitida,
- bolest břicha,
- pseudomembranózní kolitida,
- ezofagitida,
- nevolnost,
- zvracení,
- průjem,
- vyrážka,
- kopřivka,
- závažné alergické reakce (anafylaxe),
- hypersenzitivní reakce,
- svědění,
- vaginální výtok a nepohodlí,
- otok kůže,
- žloutnutí kůže a očí (žloutenka),
- abnormální jaterní funkční testy a
- bolest kloubů.
Aby se snížil vývoj bakterií rezistentních vůči lékům a zachovala se účinnost přípravku CLEOCIN 300 mg HCl a dalších antibakteriálních léků, měl by být přípravek CLEOCIN 300 mg HCl používán pouze k léčbě nebo prevenci infekcí, u kterých je prokázáno nebo existuje silné podezření, že jsou způsobeny bakteriemi.
VAROVÁNÍ
Průjem spojený s Clostridium difficile (CDAD) byl hlášen při použití téměř všech antibakteriálních látek, včetně CLEOCIN HCl, a jeho závažnost se může pohybovat od mírného průjmu až po fatální kolitidu. Léčba antibakteriálními látkami mění normální flóru tlustého střeva, což vede k přemnožení C. difficle.
Vzhledem k tomu, že léčba přípravkem CLEOCIN 150 mg HCl byla spojena se závažnou kolitidou, která může skončit fatálně, měla by být vyhrazena pro závažné infekce, kde jsou méně toxické antimikrobiální látky nevhodné, jak je popsáno v INDIKACE A POUŽITÍ sekce. Neměl by být používán u pacientů s nebakteriálními infekcemi, jako je většina infekcí horních cest dýchacích.
C. difficle produkuje toxiny A a B, které přispívají k rozvoji CDAD. Kmeny C. difficle produkující hypertoxin způsobují zvýšenou morbiditu a mortalitu, protože tyto infekce mohou být odolné vůči antimikrobiální léčbě a mohou vyžadovat kolektomii. CDAD je třeba vzít v úvahu u všech pacientů, kteří mají průjem po užívání antibiotik. Je nutná pečlivá anamnéza, protože CDAD se objevilo více než dva měsíce po podání antibakteriálních látek.
Pokud je podezření na CDAD nebo je potvrzeno, může být nutné přerušit pokračující užívání antibiotik, která nejsou zaměřena proti C. difficle. Podle klinické indikace by měla být zahájena vhodná léčba tekutin a elektrolytů, suplementace proteinů, antibiotická léčba C. difficle a chirurgické vyšetření.
POPIS
Klindamycin hydrochlorid je hydratovaná hydrochloridová sůl klindamycinu. Clindamycin je semisyntetické antibiotikum produkované 7(S)-chlor-substitucí 7(R)-hydroxylové skupiny mateřské sloučeniny linkomycinu.
Kapsle CLEOCIN HCl obsahují klindamycin hydrochlorid odpovídající 75 mg, 150 mg nebo 300 mg klindamycinu.
Neaktivní složky: 75 mg - kukuřičný škrob, FD&C blue no. 1, FD&C žlutá č. 5, želatina, laktóza, stearát hořečnatý a mastek; 150 mg - kukuřičný škrob, FD&C blue no. 1, FD&C žlutá č. 5, želatina, laktóza, stearát hořečnatý, mastek a oxid titaničitý; 300 mg - kukuřičný škrob, FD&C blue no. 1, želatina, laktóza, stearát hořečnatý, mastek a oxid titaničitý.
Strukturní vzorec je znázorněn níže:
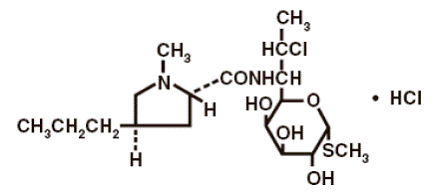
Chemický název hydrochloridu klindamycinu je methyl-7-chlor-6,7,8-trideoxy-6-(1-methyl-trans-4-propyl-L-2-pyrrolidinkarboxamido)-1-thio-L-threo-a- D-galakto-oktopyranosid monohydrochlorid.
INDIKACE
Clindamycin je indikován k léčbě závažných infekcí způsobených citlivými anaerobními bakteriemi.
Clindamycin je také indikován k léčbě závažných infekcí způsobených citlivými kmeny streptokoků, pneumokoků a stafylokoků. Jeho použití by mělo být vyhrazeno pro pacienty s alergií na penicilin nebo jiné pacienty, pro které je podle úsudku lékaře penicilin nevhodný. Kvůli riziku kolitidy, jak je popsáno v RÁMCI VAROVÁNÍ, by měl lékař před výběrem klindamycinu zvážit povahu infekce a vhodnost méně toxických alternativ (např. erythromycinu).
Anaeroby: Závažné infekce dýchacích cest, jako je empyém, anaerobní pneumonitida a plicní absces; závažné infekce kůže a měkkých tkání; septikémie; intraabdominální infekce, jako je peritonitida a intraabdominální absces (typicky vyplývající z anaerobních organismů sídlících v normálním gastrointestinálním traktu); infekce ženské pánve a genitálního traktu, jako je endometritida, negonokokový tuboovariální absces, pánevní celulitida a pooperační infekce vaginální manžety.
streptokoky: Závažné infekce dýchacích cest; závažné infekce kůže a měkkých tkání.
Stafylokoky: Závažné infekce dýchacích cest; závažné infekce kůže a měkkých tkání.
Pneumokoky: Závažné infekce dýchacích cest.
Je třeba provést bakteriologické studie ke stanovení původců a jejich citlivosti na klindamycin.
Aby se snížil vývoj bakterií rezistentních vůči lékům a zachovala se účinnost CLEOCIN HCl a dalších antibakteriálních léků, CLEOCIN HCl by měl být používán pouze k léčbě nebo prevenci infekcí, u kterých je prokázáno nebo existuje silné podezření, že jsou způsobeny citlivými bakteriemi. Pokud jsou k dispozici informace o kultivaci a citlivosti, je třeba je vzít v úvahu při výběru nebo úpravě antibakteriální terapie. Při absenci takových údajů mohou k empirickému výběru terapie přispět místní epidemiologie a vzorce citlivosti.
DÁVKOVÁNÍ A PODÁVÁNÍ
Pokud se během léčby objeví významný průjem, je třeba toto antibiotikum vysadit (viz VAROVÁNÍ V KRABICE ).
Dospělí
Závažné infekce - 150 až 300 mg každých 6 hodin. Závažnější infekce - 300 až 450 mg každých 6 hodin.
Pediatričtí pacienti (pro děti, které jsou schopny polykat tobolky):
Závažné infekce 8 až 16 mg/kg/den (4 až 8 mg/lb/den) rozdělených do tří nebo čtyř stejných dávek. Závažnější infekce – 16 až 20 mg/kg/den (8 až 10 mg/lb/den) rozdělených do tří nebo čtyř stejných dávek.
Aby se předešlo možnosti podráždění jícnu, je třeba CLEOCIN 300 mg HCl tobolky užívat s plnou sklenicí vody.
Kapsle CLEOCIN HCl nejsou vhodné pro děti, které je nedokážou spolknout celé. Tobolky neposkytují přesné dávky mg/kg, proto může být v některých případech nutné použít perorální roztok klindamycin palmitátu.
Závažné infekce způsobené anaerobními bakteriemi se obvykle léčí sterilním roztokem CLEOCIN PHOSPHATE®. Za klinicky vhodných okolností se však lékař může rozhodnout zahájit léčbu nebo pokračovat v léčbě přípravkem CLEOCIN 150 mg HCl tobolky.
V případech β-hemolytických streptokokových infekcí by léčba měla pokračovat alespoň 10 dní.
JAK DODÁVÁNO
CLEOCIN HCl kapsle jsou k dispozici v následujících sílách, barvách a velikostech:
75 mg Zelené lahve po 100 ks NDC 0009-0331-02
150 mg Světle modré a zelené lahve po 100 ks NDC 0009-0225-02
300 mg Světle modré lahve po 100 ks NDC 0009-0395-14
Skladujte při kontrolované pokojové teplotě 20 ° až 25 ° C (68 ° až 77 ° F) [viz USP ].
Distribuuje: Pharmacia & Upjohn Co, divize společnosti Pfizer Inc, NY, NY 10017. Revidováno 2017
VEDLEJŠÍ EFEKTY
Při použití klindamycinu byly hlášeny následující reakce.
Infekce a nákazy: Clostridium difficile kolitida
Gastrointestinální: Bolest břicha, pseudomembranózní kolitida, ezofagitida, nauzea, zvracení a průjem (viz VAROVÁNÍ V KRABICE ). K nástupu příznaků pseudomembranózní kolitidy může dojít během nebo po antibakteriální léčbě (viz VAROVÁNÍ ). Byl hlášen jícnový vřed. Po perorálním podání byla hlášena nepříjemná nebo kovová chuť.
Hypersenzitivní reakce: Generalizované mírné až středně závažné morbiliformní (makulopapulární) kožní vyrážky jsou nejčastěji hlášenými nežádoucími účinky. Během medikamentózní terapie byly pozorovány vezikulobulózní vyrážky a také kopřivka. Byly hlášeny závažné kožní reakce, jako je toxická epidermální nekrolýza, některé s fatálním koncem (viz VAROVÁNÍ ). Byly také hlášeny případy akutní generalizované exantematózní pustulózy (AGEP), erythema multiforme, některé připomínající Stevens-Johnsonův syndrom, anafylaktický šok, anafylaktická reakce a hypersenzitivita.
Kůže a sliznice: Byly hlášeny pruritus, vaginitida, angioedém a vzácné případy exfoliativní dermatitidy. (Vidět Hypersenzitivní reakce .)
Játra: Během léčby klindamycinem byla pozorována žloutenka a abnormality jaterních testů.
Renální: Přestože nebyla prokázána žádná přímá souvislost klindamycinu s poškozením ledvin, byla pozorována renální dysfunkce, jak je prokázáno azotemií, oligurií a/nebo proteinurií.
Hematopoetický: Byla hlášena přechodná neutropenie (leukopenie) a eozinofilie. Byly hlášeny případy agranulocytózy a trombocytopenie. Žádný přímý etiologický vztah k souběžné terapii klindamycinem nemohl být proveden v žádném z výše uvedených.
Imunitní systém: Byly hlášeny případy lékové reakce s eozinofilií a systémovými příznaky (DRESS).
Muskuloskeletální: Byly hlášeny případy polyartritidy.
DROGOVÉ INTERAKCE
Bylo prokázáno, že klindamycin má neuromuskulární blokátory, které mohou zvýšit účinek jiných neuromuskulárních blokátorů. Proto by měl být u pacientů užívajících takové přípravky používán s opatrností.
Klindamycin je metabolizován převážně CYP3A4 a v menší míře CYP3A5 na hlavní metabolit klindamycinsulfoxid a vedlejší metabolit N-desmethylklindamycin. Proto mohou inhibitory CYP3A4 a CYP3A5 zvyšovat plazmatické koncentrace klindamycinu a induktory těchto izoenzymů mohou snižovat plazmatické koncentrace klindamycinu. V přítomnosti silných inhibitorů CYP3A4 sledujte nežádoucí účinky. V přítomnosti silných induktorů CYP3A4, jako je rifampicin, sledujte ztrátu účinnosti.
Studie in vitro ukazují, že klindamycin neinhibuje CYP1A2, CYP2C9, CYP2C19, CYP2E1 nebo CYP2D6 a pouze mírně inhibuje CYP3A4.
Antagonismus byl prokázán mezi klindamycinem a erythromycinem in vitro. Vzhledem k možnému klinickému významu by tyto dva léky neměly být podávány současně.
VAROVÁNÍ
Vidět VAROVÁNÍ V KRABICE
Průjem spojený s Clostridium Difficile
Průjem spojený s Clostridium difficile (CDAD) byl hlášen při použití téměř všech antibakteriálních látek, včetně CLEOCIN 300 mg HCl, a jeho závažnost se může pohybovat od mírného průjmu až po fatální kolitidu. Léčba antibakteriálními látkami mění normální flóru tlustého střeva, což vede k přemnožení C. difficle.
C. difficle produkuje toxiny A a B, které přispívají k rozvoji CDAD. Kmeny C. difficle produkující hypertoxin způsobují zvýšenou morbiditu a mortalitu, protože tyto infekce mohou být odolné vůči antimikrobiální léčbě a mohou vyžadovat kolektomii. CDAD je třeba vzít v úvahu u všech pacientů, kteří mají průjem po užívání antibiotik. Je nutná pečlivá anamnéza, protože CDAD se objevilo více než dva měsíce po podání antibakteriálních látek.
Pokud je podezření na CDAD nebo je potvrzeno, může být nutné přerušit pokračující užívání antibiotik, která nejsou zaměřena proti C. difficle. Podle klinické indikace by měla být zahájena vhodná léčba tekutin a elektrolytů, suplementace proteinů, antibiotická léčba C. difficle a chirurgické vyšetření.
Anafylaktické a závažné reakce z přecitlivělosti
Byly hlášeny anafylaktický šok a anafylaktické reakce (viz NEŽÁDOUCÍ REAKCE ).
Byly hlášeny závažné reakce z přecitlivělosti, včetně závažných kožních reakcí, jako je toxická epidermální nekrolýza (TEN), léková reakce s eozinofilií a systémovými příznaky (DRESS) a Stevens-Johnsonův syndrom (SJS), některé s fatálním koncem (viz NEŽÁDOUCÍ REAKCE ).
V případě takové anafylaktické nebo závažné reakce přecitlivělosti trvale přerušte léčbu a zahajte vhodnou terapii.
Je třeba pečlivě prozkoumat předchozí citlivost na léky a jiné alergeny.
Použití při meningitidě
Vzhledem k tomu, že klindamycin dostatečně nedifunduje do mozkomíšního moku, neměl by být přípravek používán k léčbě meningitidy.
OPATŘENÍ
Všeobecné
Přehled dosavadních zkušeností naznačuje, že podskupina starších pacientů s přidruženým závažným onemocněním může průjem snášet hůře. Pokud je u těchto pacientů indikován klindamycin, je třeba u nich pečlivě sledovat změnu frekvence střev.
CLEOCIN 300 mg HCl by měl být předepisován s opatrností u jedinců s anamnézou gastrointestinálního onemocnění, zejména kolitidy.
CLEOCIN 300 mg HCl by měl být předepisován s opatrností u atopických jedinců.
Indikované chirurgické zákroky by měly být prováděny ve spojení s antibiotickou terapií.
Užívání přípravku CLEOCIN 150 mg HCl občas vede k přemnožení nevnímavých organismů – zejména kvasinek. Pokud dojde k superinfekcím, je třeba přijmout vhodná opatření, jak naznačuje klinická situace.
Úprava dávkování klindamycinu nemusí být nutná u pacientů s onemocněním ledvin. U pacientů se středně těžkým až těžkým onemocněním jater bylo zjištěno prodloužení poločasu klindamycinu. Ze studií však vyplývá, že při podávání každých osm hodin by akumulace měla nastat jen zřídka. Úprava dávkování proto u pacientů s onemocněním jater nemusí být nutná. Při léčbě pacientů se závažným onemocněním jater by však měla být prováděna pravidelná stanovení jaterních enzymů.
75 mg a 150 mg tobolky obsahují FD&C yellow no. 5 (tartrazin), který může u některých vnímavých jedinců způsobit reakce alergického typu (včetně bronchiálního astmatu). Přestože celkový výskyt FD&C žluté ne. Senzitivita 5 (tartrazin) v běžné populaci je nízká, často se vyskytuje u pacientů, kteří mají také přecitlivělost na aspirin.
Je nepravděpodobné, že by předepsání přípravku CLEOCIN 150 mg HCl při absenci prokázané nebo silně suspektní bakteriální infekce nebo profylaktické indikace přineslo pacientovi prospěch a zvýšilo riziko rozvoje bakterií rezistentních na léky.
Laboratorní testy
Během dlouhodobé léčby by měly být pravidelně prováděny testy funkce jater a ledvin a krevní obraz.
Karcinogeneze, mutageneze, zhoršení plodnosti
Nebyly provedeny dlouhodobé studie na zvířatech s klindamycinem ke zhodnocení karcinogenního potenciálu. Provedené testy genotoxicity zahrnovaly mikronukleový test na potkanech a test reverze Ames Salmonella. Oba testy byly negativní.
Studie fertility u potkanů léčených perorálně dávkou až 300 mg/kg/den (přibližně 1,6násobek nejvyšší doporučené dávky pro dospělého člověka na základě mg/m2) neprokázaly žádné účinky na fertilitu nebo schopnost páření.
Těhotenství
Teratogenní účinky
V klinických studiích s těhotnými ženami nebylo systémové podávání klindamycinu během druhého a třetího trimestru spojeno se zvýšenou frekvencí vrozených abnormalit.
Clindamycin by měl být podáván během prvního trimestru těhotenství pouze tehdy, je-li to nezbytně nutné. Neexistují žádné adekvátní a dobře kontrolované studie u těhotných žen během prvního trimestru těhotenství. Vzhledem k tomu, že reprodukční studie na zvířatech ne vždy předpovídají lidskou odpověď, měl by být tento lék používán během těhotenství pouze tehdy, je-li to nezbytně nutné.
Reprodukční studie provedené na potkanech a myších s použitím perorálních dávek klindamycinu až do 600 mg/kg/den (3,2násobek a 1,6násobku nejvyšší doporučené dávky pro dospělého člověka na základě mg/m²) nebo subkutánních dávek klindamycinu až do 250 mg/kg /den (1,3násobek a 0,7násobek nejvyšší doporučené dávky pro dospělého člověka na základě mg/m²) neodhalil žádný důkaz teratogenity.
Kojící matky
Bylo hlášeno, že klindamycin se objevuje v mateřském mléce v rozmezí 0,7 až 3,8 mcg/ml. Clindamycin má potenciál způsobit nežádoucí účinky na gastrointestinální flóru kojeného dítěte. Pokud kojící matka vyžaduje perorální nebo intravenózní klindamycin, není to důvod k přerušení kojení, ale může být preferován alternativní lék. Sledujte u kojence možné nepříznivé účinky na gastrointestinální flóru, jako je průjem, kandidóza (soor, plenková vyrážka) nebo vzácně krev ve stolici, což naznačuje možnou kolitidu spojenou s antibiotiky.
Je třeba zvážit vývojové a zdravotní přínosy kojení spolu s klinickou potřebou matky klindamycin a veškerými potenciálními nežádoucími účinky klindamycinu nebo základního stavu matky na kojené dítě.
Pediatrické použití
Pokud je CLEOCIN 300 mg HCl podáván pediatrické populaci (od narození do 16 let), je žádoucí odpovídající monitorování funkcí orgánového systému.
Geriatrické použití
Klinické studie klindamycinu nezahrnovaly dostatečný počet pacientů ve věku 65 a více let, aby bylo možné určit, zda reagují odlišně od mladších pacientů. Jiné hlášené klinické zkušenosti však naznačují, že kolitida spojená s antibiotiky a průjem (způsobený Clostridium difficile) pozorované ve spojení s většinou antibiotik se vyskytují častěji u starších osob (> 60 let) a mohou být závažnější. Tito pacienti by měli být pečlivě sledováni, aby se u nich nerozvinul průjem.
Farmakokinetické studie s klindamycinem neprokázaly žádné klinicky významné rozdíly mezi mladými a staršími jedinci s normální funkcí jater a normální funkcí ledvin (přizpůsobenou věku) po perorálním nebo intravenózním podání.
PŘEDÁVKOVAT
Významná mortalita byla pozorována u myší při intravenózní dávce 855 mg/kg au potkanů při perorální nebo subkutánní dávce přibližně 2618 mg/kg. U myší byly pozorovány křeče a deprese.
Hemodialýza a peritoneální dialýza nejsou účinné při odstraňování klindamycinu ze séra.
KONTRAINDIKACE
CLEOCIN 150 mg HCl je kontraindikován u jedinců s anamnézou přecitlivělosti na přípravky obsahující klindamycin nebo linkomycin.
KLINICKÁ FARMAKOLOGIE
Human Farmakologie
Vstřebávání
Studie sérových hladin s perorální dávkou 150 mg klindamycin-hydrochloridu u 24 normálních dospělých dobrovolníků ukázaly, že klindamycin byl po perorálním podání rychle absorbován. Průměrná maximální sérová hladina 2,50 mcg/ml byla dosažena za 45 minut; sérové hladiny byly v průměru 1,51 mcg/ml za 3 hodiny a 0,70 mcg/ml za 6 hodin. Absorpce perorální dávky je prakticky úplná (90 %) a současné podávání potravy znatelně nemění sérové koncentrace; sérové hladiny byly jednotné a předvídatelné od osoby k osobě a od dávky k dávce. Studie sérových hladin po opakovaných dávkách CLEOCIN 150 mg HCl po dobu až 14 dnů neprokázaly žádné známky akumulace nebo změněného metabolismu léčiva. Dávky až 2 gramy klindamycinu denně po dobu 14 dnů byly zdravými dobrovolníky dobře snášeny, kromě toho, že výskyt gastrointestinálních vedlejších účinků je vyšší s vyššími dávkami.
Rozdělení
Koncentrace klindamycinu v séru se zvyšovaly lineárně se zvyšující se dávkou. Sérové hladiny překračují MIC (minimální inhibiční koncentrace) u většiny indikovaných organismů po dobu nejméně šesti hodin po podání obvykle doporučených dávek. Klindamycin je široce distribuován v tělesných tekutinách a tkáních (včetně kostí). Žádné významné hladiny klindamycinu se nedosahují v mozkomíšním moku, a to ani v přítomnosti zanícených mozkových blan.
Metabolismus
Studie in vitro na lidských jaterních a střevních mikrozomech ukázaly, že klindamycin je metabolizován převážně cytochromem P450 3A4 (CYP3A4), s malým přispěním CYP3A5, za vzniku klindamycinsulfoxidu a minoritního metabolitu, N-desmethylklindamycinu.
Vylučování
Průměrný biologický poločas je 2,4 hodiny. Přibližně 10 % biologické aktivity se vylučuje močí a 3,6 % stolicí; zbytek je vylučován jako bioinaktivní metabolity.
Zvláštní populace
Renální poškození
Sérový poločas klindamycinu je mírně zvýšen u pacientů s výrazně sníženou funkcí ledvin. Hemodialýza a peritoneální dialýza nejsou účinné při odstraňování klindamycinu ze séra.
Použití u starších osob
Farmakokinetické studie u starších dobrovolníků (61-79 let) a mladších dospělých (18-39 let) ukazují, že samotný věk nemění farmakokinetiku klindamycinu (clearance, poločas eliminace, distribuční objem a plocha pod křivkou sérové koncentrace-čas ) po IV podání klindamycin fosfátu. Po perorálním podání klindamycin-hydrochloridu je poločas eliminace zvýšen na přibližně 4,0 hodiny (rozmezí 3,4-5,1 h) u starších osob ve srovnání s 3,2 hodinami (rozmezí 2,1 - 4,2 h) u mladších dospělých. Rozsah absorpce se však mezi věkovými skupinami neliší a u starších osob s normální funkcí jater a normální (věku přizpůsobenou) funkcí ledvin není nutná žádná úprava dávkování1.
Mikrobiologie
Mechanismus působení
Clindamycin inhibuje syntézu bakteriálních proteinů vazbou na 23S RNA podjednotky 50S ribozomu. Clindamycin je bakteriostatický.
Odpor
Rezistence na klindamycin je nejčastěji způsobena modifikací specifických bází 23S ribozomální RNA. Zkřížená rezistence mezi klindamycinem a linkomycinem je kompletní. Protože se vazebná místa pro tato antibakteriální léčiva překrývají, je někdy pozorována zkřížená rezistence mezi linkosamidy, makrolidy a streptograminem B. Rezistence na klindamycin indukovaná makrolidem se vyskytuje u některých izolátů bakterií rezistentních na makrolidy. Izoláty stafylokoků a beta-hemolytických streptokoků rezistentních na makrolidy by měly být vyšetřeny na indukci rezistence na klindamycin pomocí testu D-zóny.
Antimikrobiální aktivita
Bylo prokázáno, že klindamycin je účinný proti většině izolátů následujících mikroorganismů, a to jak in vitro, tak při klinických infekcích, jak je popsáno v INDIKACE A POUŽITÍ sekce.
Gram-pozitivní bakterie
Staphylococcus aureus (kmeny citlivé na meticilin) Streptococcus pneumoniae (kmeny citlivé na penicilin) Streptococcus pyogenes
Anaerobní bakterie
Clostridium perfringens Fusobacterium necrophorum Fusobacterium nucleatum Peptostreptococcus anaerobius Prevotella melaninogenica
Nejméně 90 % níže uvedených mikroorganismů vykazuje in vitro minimální inhibiční koncentrace (MIC) menší nebo rovné hraničnímu bodu MIC citlivého na klindamycin pro organismy podobného typu, jako jsou ty, které jsou uvedeny v tabulce 1. Nicméně účinnost klindamycinu při léčbě klinických infekce způsobené těmito mikroorganismy nebyla v adekvátních a dobře kontrolovaných klinických studiích prokázána.
Gram-pozitivní bakterie
Staphylococcus epidermidis (kmeny citlivé na meticilin) Streptococcus agalactiae Streptococcus anginosus Streptococcus mitis Streptococcus oralis
Anaerobní bakterie
Actinomyces israelii Clostridium clostridioforme Eggerthella lenta Finegoldia (Peptostreptococcus) magna Micromonas (Peptostreptococcus) micros Prevotella bivia Prevotella intermedia Propionibacterium acnes
Metody testování citlivosti
Je-li to možné, měla by klinická mikrobiologická laboratoř poskytovat lékaři kumulativní výsledky testů citlivosti in vitro na antimikrobiální léky používané v místních nemocnicích a ordinacích jako pravidelné zprávy, které popisují profil citlivosti nozokomiálních a komunitně získaných patogenů. Tyto zprávy by měly pomoci lékaři při výběru antibakteriálního léku pro léčbu.
Techniky ředění
Kvantitativní metody se používají ke stanovení antimikrobiálních minimálních inhibičních koncentrací (MIC). Tyto MIC poskytují odhady citlivosti bakterií na antimikrobiální sloučeniny. MIC by měly být stanoveny pomocí standardizované testovací metody2,3 (bujón a/nebo agar). Hodnoty MIC by měly být interpretovány podle kritérií uvedených v tabulce 1.
Difúzní techniky
Kvantitativní metody, které vyžadují měření průměrů zón, mohou také poskytnout reprodukovatelné odhady citlivosti bakterií na antimikrobiální sloučeniny. Velikost zóny by měla být určena pomocí standardizované metody2,5. Tento postup používá papírové disky impregnované 2 mcg klindamycinu k testování citlivosti bakterií na klindamycin. Body přerušení difúze disku jsou uvedeny v tabulce 1.
Anaerobní techniky
anaerobních bakterií lze citlivost na klindamycin stanovit standardizovanou zkušební metodou2,4. Získané hodnoty MIC by měly být interpretovány podle kritérií uvedených v tabulce 1.
Zpráva o citlivosti (S ) ukazuje, že antimikrobiální léčivo pravděpodobně inhibuje růst patogenu, pokud antimikrobiální léčivo dosáhne koncentrace obvykle dosažitelné v místě infekce. Zpráva o meziproduktu (I) naznačuje, že výsledek by měl být považován za nejednoznačný, a pokud mikroorganismus není plně citlivý na alternativní, klinicky proveditelné léky, test by se měl opakovat. Tato kategorie implikuje možnou klinickou použitelnost v místech těla, kde je léčivo fyziologicky koncentrované, nebo v situacích, kdy lze použít vysokou dávku léčiva. Tato kategorie také poskytuje nárazníkovou zónu, která zabraňuje malým, nekontrolovaným technickým faktorům, aby způsobily velké nesrovnalosti ve výkladu. Zpráva o Resistant (R) ukazuje, že antimikrobiální léčivo pravděpodobně nebude inhibovat růst patogenu, pokud antimikrobiální léčivo dosáhne koncentrace obvykle dosažitelné v místě infekce; měla by být zvolena jiná terapie.
Kontrola kvality
Standardizované postupy testování citlivosti vyžadují použití laboratorních kontrol k monitorování a zajištění přesnosti a přesnosti zásob a činidel používaných v testu a technik jednotlivců provádějících test.2,3,4,5 Standardní prášek klindamycinu by měl poskytnout rozsahy MIC jsou uvedeny v tabulce 2. Pro techniku diskové difúze využívající disk s 2 mcg klindamycinem by měla být splněna kritéria uvedená v tabulce 2.
anaeroby lze testovat buď mikroředěním v bujónu nebo ředěním na agaru. NA=Nelze použít ATCC® je registrovaná ochranná známka American Type Culture Collection
REFERENCE
1. Smith RB, Phillips JP: Hodnocení CLEOCIN HCl a CLEOCIN Phosphate ve stárnoucí populaci. Upjohn TR 8147-82-9122-021, prosinec 1982.
2. CLSI. Výkonové standardy pro testování antimikrobiální citlivosti: 26. vydání. CLSI doplněk M100S. Wayne, PA: Institut pro klinické a laboratorní standardy; 2016.
3. CLSI. Metody ředění Testy antimikrobiální citlivosti pro bakterie, které rostou aerobně; Schválený standard – desáté vydání. CLSI dokument M07-A10. Wayne, PA: Institut pro klinické a laboratorní standardy; 2015.
4. CLSI. Metody pro testování antimikrobiální citlivosti anaerobních bakterií; Schválené standardní osmé vydání. CLSI dokument M11-A8. Wayne, PA: Institut pro klinické a laboratorní standardy; 2012.
5. CLSI. Výkonové standardy pro testy citlivosti antimikrobiálních disků; Schválený standard – dvanácté vydání. CLSI dokument M02-A12. Wayne, PA: Institut pro klinické a laboratorní standardy; 2015.
INFORMACE PRO PACIENTA
Pacienti by měli být poučeni, že antibakteriální léky, včetně CLEOCIN HCl, by měly být používány pouze k léčbě bakteriálních infekcí. Neléčí virové infekce (např. nachlazení). Když je CLEOCIN HCl předepsán k léčbě bakteriální infekce, pacienti by měli být informováni, že ačkoli je běžné, že se na začátku léčby cítí lépe, léky by měly být užívány přesně podle pokynů. Vynechání dávek nebo nedokončení celé terapie může (1) snížit účinnost okamžité léčby a (2) zvýšit pravděpodobnost, že si bakterie vyvinou rezistenci a nebudou v budoucnu léčitelné přípravkem CLEOCIN 150 mg HCl nebo jinými antibakteriálními léky.
Průjem je častým problémem způsobeným antibiotiky, který obvykle končí, když je antibiotikum vysazeno. Někdy po zahájení léčby antibiotiky se u pacientů může vyvinout vodnatá a krvavá stolice (s žaludečními křečemi a horečkou nebo bez nich) dokonce až dva nebo více měsíců po užití poslední dávky antibiotika. Pokud k tomu dojde, pacienti by měli co nejdříve kontaktovat svého lékaře.
