Minocin 50mg, 100mg Minocycline Hydrochloride Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Minocin perorální suspenze a jak se používá?
Minocin (minocyklin hydrochlorid) je tetracyklinové antibiotikum používané k léčbě mnoha různých bakteriálních infekcí, jako jsou infekce močových cest, infekce dýchacích cest, kožní infekce, těžké akné, kapavka, klíšťová horečka, chlamydie a další.
Jaké jsou vedlejší účinky přípravku Minocin perorální suspenze?
Mezi běžné vedlejší účinky přípravku Minocin patří:
- závrať,
- pocit únavy,
- pocit točení,
- bolesti kloubů nebo svalů,
- změna barvy kůže nebo nehtů nebo dásní,
- nevolnost,
- průjem,
- žaludeční nevolnost,
- kožní vyrážka nebo svědění,
- oteklý jazyk, popř
- vaginální svědění nebo výtok.
Informujte svého lékaře, pokud máte závažné nežádoucí účinky přípravku Minocin 50 mg, včetně:
- žaludeční křeče,
- průjem, který je vodnatý nebo krvavý,
- příznaky chřipky,
- vředy v ústech a krku,
- slabost,
- tmavě zbarvená moč,
- neobvyklé krvácení,
- fialové nebo červené skvrny pod kůží,
- horečka,
- vyrážka,
- modřiny,
- silné brnění nebo necitlivost,
- svalová slabost,
- ztráta chuti k jídlu,
- zežloutnutí kůže nebo očí,
- bolest na hrudi,
- nepravidelný srdeční rytmus,
- kašel,
- sípání,
- dušnost,
- zmatek,
- zvracení,
- otok,
- přibývání na váze,
- močí méně než obvykle nebo vůbec ne,
- bolest hlavy nebo bolest za očima,
- zvoní ti v uších,
- problémy se zrakem,
- bolest nebo otok kloubů s horečkou,
- oteklé žlázy,
- Bolest svalů,
- celkový pocit nemoci,
- neobvyklé myšlenky nebo chování,
- záchvaty (křeče), popř
- závažná kožní reakce.
Aby se snížil vývoj bakterií rezistentních vůči lékům a zachovala se účinnost perorální suspenze MINOCIN® a dalších antibakteriálních léků, měla by být perorální suspenze MINOCIN používána pouze k léčbě nebo prevenci infekcí, u kterých je prokázáno nebo existuje silné podezření, že jsou způsobeny bakteriemi.
POPIS
MINOCIN 100 mg minocyklin hydrochlorid, je semisyntetický derivát tetracyklinu, 4,7Bis(dimethylamino)-1,4,4a,5,5a,6,11,12a-oktahydro-3,10,12,12a-tetrahydroxy-1,11 -dioxo-2-naftacenekarboxamid monohydrochlorid.
Jeho strukturní vzorec je:
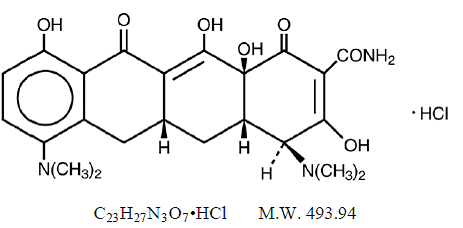 C23H27N3O7.HCl MW 493,94
C23H27N3O7.HCl MW 493,94 MINOCIN 50 mg perorální suspenze obsahuje minocyklin hydrochlorid odpovídající 50 mg minocyklinu na 5 ml (10 mg/ml) a následující neaktivní složky: alkohol, butylparaben, hydroxid vápenatý, celulóza, dekaglyceryltetraoleát, edetát vápenato-sodný, polyguar00 , propylparaben, propylenglykol, sodná sůl sacharinu, siřičitan sodný (viz VAROVÁNÍ ) a sorbitol.
INDIKACE
MINOCIN 100 mg perorální suspenze je indikován k léčbě následujících infekcí způsobených citlivými kmeny určených mikroorganismů:
Skvrnitá horečka Rocky Mountain, tyfus a skupina tyfu, Q horečka, rickettsiové neštovice a klíšťové horečky způsobené rickettsiemi.
Infekce dýchacích cest způsobené Mycoplasma pneumoniae.
Lymphogranuloma venereum způsobený Chlamydia trachomatis.
Psitakóza (ornitóza) způsobená Chlamydophila psittaci.
Trachom způsobený Chlamydia trachomatis, ačkoli infekční agens není vždy eliminován, jak lze posoudit imunofluorescencí.
Inkluzní konjunktivitida způsobená Chlamydia trachomatis.
Negonokoková uretritida, endocervikální nebo rektální infekce u dospělých způsobené Ureaplasma urealyticum nebo Chlamydia trachomatis.
Recidivující horečka způsobená Borrelia recurrentis.
Chancroid způsobený Haemophilus ducreyi.
Mor způsobený Yersinia pestis.
Tularémie způsobená Francisella tularensis.
Cholera způsobená Vibrio cholerae.
Infekce Campylobacter fetus způsobené Campylobacter fetus.
Brucelóza způsobená druhy Brucella (ve spojení se streptomycinem).
Bartonelóza způsobená Bartonella bacilliformis.
Granuloma inguinale způsobená Klebsiella granulomatis.
Minocyklin je indikován k léčbě infekcí způsobených následujícími gramnegativními mikroorganismy, pokud bakteriologické vyšetření ukazuje vhodnou citlivost na léčivo:
Escherichia coli.
Enterobacter aerogenes.
druh Shigella.
Druhy Acinetobacter.
Infekce dýchacích cest způsobené Haemophilus influenzae.
Infekce dýchacích cest a močových cest způsobené druhy Klebsiella.
MINOCIN perorální suspenze je indikována k léčbě infekcí způsobených následujícími grampozitivními mikroorganismy, pokud bakteriologické testy prokáží vhodnou citlivost na léčivo:
Infekce horních cest dýchacích způsobené Streptococcus pneumoniae. Infekce kůže a kožní struktury způsobené Staphylococcus aureus (poznámka: Minocyklin není lékem volby při léčbě žádného typu stafylokokové infekce).
Pokud je penicilin kontraindikován, je minocyklin alternativním lékem v léčbě následujících infekcí:
Nekomplikovaná uretritida u mužů způsobená Neisseria gonorrhoeae a pro léčbu jiných gonokokových infekcí.
Infekce u žen způsobené Neisseria gonorrhoeae.
Syfilis způsobená Treponema pallidum poddruh pallidum.
Vybočení způsobené Treponema pallidum subspecies pertenue.
Listerióza způsobená Listeria monocytogenes.
Antrax způsobený Bacillus anthracis.
Vincentova infekce způsobená Fusobacterium fusiforme.
Aktinomykóza způsobená Actinomyces israelii.
Infekce způsobené druhy Clostridium.
Při akutní střevní amebiáze může být minocyklin užitečným doplňkem amebicidů.
U těžkého akné může být minocyklin užitečnou doplňkovou terapií.
Perorální minocyklin je indikován k léčbě asymptomatických nosičů Neisseria meningitidis k odstranění meningokoků z nosohltanu. Aby byla zachována užitečnost minocyklinu při léčbě asymptomatických nosičů meningokoků, měly by být prováděny diagnostické laboratorní postupy, včetně sérotypizace a testování citlivosti, aby se zjistil stav nosiče a správná léčba. Doporučuje se, aby profylaktické použití minocyklinu bylo vyhrazeno pro situace, kdy je riziko meningokokové meningitidy vysoké.
Perorální minocyklin není indikován k léčbě meningokokové infekce.
Ačkoli nebyly provedeny žádné kontrolované klinické studie účinnosti, omezené klinické údaje ukazují, že perorální hydrochlorid minocyklinu byl úspěšně používán při léčbě infekcí způsobených Mycobacterium marinum.
Aby se snížil vývoj bakterií rezistentních vůči lékům a zachovala se účinnost perorální suspenze MINOCIN 100 mg a dalších antibakteriálních léků, měla by být perorální suspenze MINOCIN používána pouze k léčbě nebo prevenci infekcí, u kterých je prokázáno nebo existuje silné podezření, že jsou způsobeny citlivými bakteriemi. Pokud jsou k dispozici informace o kultivaci a citlivosti, je třeba je vzít v úvahu při výběru nebo úpravě antibakteriální terapie. Při absenci takových údajů mohou k empirickému výběru terapie přispět místní epidemiologie a vzorce citlivosti.
DÁVKOVÁNÍ A PODÁVÁNÍ
OBVYKLÁ DÁVKOVÁNÍ A FREKVENCE PODÁVÁNÍ MINOCYKLINU SE LIŠÍ OD OSTATNÍCH TETRACYKLINŮ. PŘEKROČENÍ DOPORUČENÉHO DÁVKOVÁNÍ MŮŽE ZPŮSOBIT ZVÝŠENÝ VÝSKYT NEŽÁDOUCÍCH ÚČINKŮ.
Léčba by měla pokračovat alespoň 24 až 48 hodin po ústupu příznaků a horečky.
Dosavadní studie ukázaly, že absorpce perorální suspenze MINOCIN není výrazně ovlivněna potravinami a mléčnými výrobky.
Farmakokinetika minocyklinu u pacientů s poruchou funkce ledvin (CLCR VAROVÁNÍ ).
Při léčbě streptokokových infekcí by měla být podávána terapeutická dávka tetracyklinu po dobu nejméně deseti dnů.
Pro pediatrické pacienty starší 8 let
Obvyklá pediatrická dávka přípravku MINOCIN je zpočátku 4 mg/kg a poté 2 mg/kg každých 12 hodin, přičemž se nesmí překročit obvyklá dávka pro dospělé.
Dospělí
Obvyklá dávka přípravku MINOCIN je zpočátku 200 mg a poté 100 mg každých 12 hodin.
Při léčbě syfilis by měla být obvyklá dávka přípravku MINOCIN podávána po dobu 10 až 15 dnů. Doporučuje se pečlivé sledování, včetně laboratorních testů.
Pacienti s kapavkou citliví na penicilin mohou být léčeni přípravkem MINOCIN 50 mg, podávaným zpočátku jako 200 mg, následně 100 mg každých 12 hodin po dobu minimálně 4 dnů, s kultivací po terapii během 2 až 3 dnů.
Při léčbě nosičství meningokoků je doporučená dávka 100 mg každých 12 hodin po dobu 5 dnů.
Infekce Mycobacterium marinum: Ačkoli optimální dávky nebyly stanoveny, v omezeném počtu případů bylo úspěšně použito 100 mg každých 12 hodin po dobu 6 až 8 týdnů.
Nekomplikovaná uretrální, endocervikální nebo rektální infekce u dospělých způsobená Chlamydia trachomatis nebo Ureaplasma urealyticum: 100 mg perorálně každých 12 hodin po dobu nejméně 7 dnů.
Při léčbě nekomplikované gonokokové uretritidy u mužů se doporučuje 100 mg dvakrát denně perorálně po dobu 5 dnů.
JAK DODÁVÁNO
MINOCIN (minocyklin hydrochlorid) perorální suspenze obsahuje minocyklin hydrochlorid odpovídající 50 mg minocyklinu na čajovou lžičku (5 ml). Konzervováno propylparabenem 0,10 % a butylparabenem 0,06 % alkoholem USP 5 % v/v. S příchutí pudinku.
NDC 16781-473-60 - Láhev 2 fl. Oz. (60 ml)
Skladujte při kontrolované pokojové teplotě 20° až 25°C (68° až 77°F).
NEZMRZŇUJTE.
Vyrobeno pro: Onset Dermatologics, LLC Cumberland, RI 02864. Revize: listopad 2018
VEDLEJŠÍ EFEKTY
Vzhledem k prakticky úplné absorpci perorálního minocyklinu nebyly vedlejší účinky na dolní střevo, zejména průjem, časté. U pacientů užívajících tetracykliny byly pozorovány následující nežádoucí účinky.
Tělo jako celek: Horečka a změna barvy sekretů.
Gastrointestinální: Anorexie, nauzea, zvracení, průjem, dyspepsie, stomatitida, glositida, dysfagie, hypoplazie skloviny, enterokolitida, pseudomembranózní kolitida, pankreatitida, zánětlivé léze (s moniliálním přerůstáním) v orální a anogenitální oblasti.
Genitourinární: Vulvovaginitida.
Jaterní toxicita: Hyperbilirubinémie, jaterní cholestáza, zvýšení jaterních enzymů, fatální jaterní selhání a žloutenka. Byla hlášena hepatitida, včetně autoimunitní hepatitidy, a selhání jater (viz OPATŘENÍ ).

Kůže: Alopecie, erythema nodosum, hyperpigmentace nehtů, pruritus, toxická epidermální nekrolýza, vaskulitida, makulopapulózní vyrážka a erytematózní vyrážka. Byla hlášena exfoliativní dermatitida. Byly hlášeny fixní lékové erupce, včetně balanitidy. Byl hlášen multiformní erytém a Stevens-Johnsonův syndrom. Fotosenzitivita je diskutována výše (viz VAROVÁNÍ ). Byla hlášena pigmentace kůže a sliznic.
Respirační: Kašel, dušnost, bronchospasmus, exacerbace astmatu a pneumonitida.
Renální toxicita: Intersticiální nefritida. Bylo hlášeno zvýšení BUN a zjevně souvisí s dávkou (viz VAROVÁNÍ ). Bylo hlášeno reverzibilní akutní selhání ledvin.
Muskuloskeletální: Artralgie, artritida, změna barvy kostí, myalgie, ztuhlost kloubů a otoky kloubů.
Hypersenzitivní reakce: Byly hlášeny kopřivka, angioneurotický edém, polyartralgie, anafylaxe/anafylaktoidní reakce (včetně šoku a úmrtí), anafylaktoidní purpura, myokarditida, perikarditida, exacerbace systémového lupus erythematodes a plicní infiltráty s eozinofilií. Byl také hlášen přechodný syndrom podobný lupusu a reakce podobné sérové nemoci.
Krev: Byla hlášena agranulocytóza, hemolytická anémie, trombocytopenie, leukopenie, neutropenie, pancytopenie a eozinofilie.
Centrální nervový systém: Křeče, závratě, hypestezie, parestézie, sedace a vertigo. Pseudotumor cerebri (benigní intrakraniální hypertenze) u dospělých a vypouklé fontanely u kojenců (viz OPATŘENÍ - Všeobecné ). Byla hlášena i bolest hlavy.
Jiný: Rakovina štítné žlázy byla hlášena po uvedení přípravku na trh v souvislosti s přípravky obsahujícími minocykliny. Pokud je léčba minocykliny podávána po delší dobu, je třeba zvážit sledování známek rakoviny štítné žlázy. Bylo hlášeno, že tetracykliny při dlouhodobém podávání způsobují hnědočerné mikroskopické zbarvení štítné žlázy. Byly hlášeny případy abnormální funkce štítné žlázy.
Změna barvy zubů u dětí mladších 8 let (viz VAROVÁNÍ ) a také u dospělých.
Bylo hlášeno zbarvení ústní dutiny (včetně jazyka, rtů a dásní).
U pacientů užívajících přípravek MINOCIN (hydrochlorid minocyklinu) byl hlášen tinnitus a snížený sluch.
Byly hlášeny následující syndromy. V některých případech zahrnujících tyto syndromy byla hlášena smrt. Stejně jako u jiných závažných nežádoucích účinků, pokud je rozpoznán některý z těchto syndromů, je třeba lék okamžitě vysadit:
Syndrom přecitlivělosti sestávající z kožní reakce (jako je vyrážka nebo exfoliativní dermatitida), eozinofilie a jednoho nebo více z následujících: hepatitida, pneumonitida, nefritida, myokarditida a perikarditida. Může být přítomna horečka a lymfadenopatie.
Lupus-like syndrom sestávající z pozitivní antinukleární protilátky; artralgie, artritida, ztuhlost kloubů nebo otoky kloubů; a jedno nebo více z následujících: horečka, myalgie, hepatitida, vyrážka a vaskulitida.
syndrom podobný sérové nemoci sestávající z horečky; kopřivka nebo vyrážka; a artralgie, artritida, ztuhlost kloubů nebo otoky kloubů a lymfadenopatie. Může být přítomna eozinofilie.
Chcete-li nahlásit PODezření na NEŽÁDOUCÍ REAKCE, kontaktujte společnost Valeant Pharmaceuticals North America LLC na čísle 1-800-321-4576 nebo FDA na čísle 1-800-FDA-1088 nebo www.fda.gov/medwatch.
DROGOVÉ INTERAKCE
Protože bylo prokázáno, že tetracykliny snižují aktivitu plazmatického protrombinu, pacienti, kteří jsou na antikoagulační léčbě, mohou vyžadovat úpravu dávky antikoagulancia směrem dolů.
Vzhledem k tomu, že bakteriostatické léky mohou interferovat s baktericidním účinkem penicilinu, je vhodné vyhnout se podávání léků třídy tetracyklinů ve spojení s penicilinem.
Absorpci tetracyklinů zhoršují antacida obsahující hliník, vápník nebo hořčík a přípravky obsahující železo.
Bylo hlášeno, že současné užívání tetracyklinu a methoxyfluranu vede k fatální renální toxicitě.
Současné užívání tetracyklinů s perorálními kontraceptivy může snížit účinnost perorálních kontraceptiv.
Je třeba se vyhnout podávání isotretinoinu krátce před, během a krátce po léčbě minocykliny. Každé léčivo samotné bylo spojováno s pseudotumorem cerebri (viz OPATŘENÍ ).
Zvýšené riziko ergotismu při podávání námelových alkaloidů nebo jejich derivátů s tetracykliny.
VAROVÁNÍ
Vývoj zubů
MINOCIN perorální suspenze, stejně jako jiná antibiotika třídy tetracyklinů, může způsobit poškození plodu, když je podávána těhotné ženě. Pokud se během těhotenství užívá jakýkoli tetracyklin nebo pokud pacientka otěhotní během užívání těchto léků, měla by být informována o potenciálním riziku pro plod. Užívání léků třídy tetracyklinů během vývoje zubů (poslední polovina těhotenství, kojenecké období a dětství do 8 let věku) může způsobit trvalé zabarvení zubů (žluto-šedo-hnědé).
Tato nežádoucí reakce je častější při dlouhodobém užívání léku, ale byla pozorována po opakovaných krátkodobých cyklech. Byla také hlášena hypoplazie skloviny. Tetracyklinové léky by se proto neměly používat během vývoje zubů, pokud jiné léky pravděpodobně nebudou účinné nebo nejsou kontraindikovány.
Vývoj kostry
Všechny tetracykliny tvoří stabilní vápníkový komplex v jakékoli kostotvorné tkáni. Snížení rychlosti růstu fibuly bylo pozorováno u předčasně narozených dětí, kterým byl perorálně podáván tetracyklin v dávkách 25 mg/kg každých šest hodin. Ukázalo se, že tato reakce je reverzibilní, když byl lék vysazen.
Použití v těhotenství
Výsledky studií na zvířatech ukazují, že tetracykliny procházejí placentou, nacházejí se ve fetálních tkáních a mohou mít toxické účinky na vyvíjející se plod (často související s retardací vývoje kostry). Důkazy embryotoxicity byly zaznamenány u zvířat léčených na počátku březosti. Bezpečnost přípravku MINOCIN pro použití během těhotenství nebyla stanovena.
Dermatologická reakce
Při užívání minocyklinu byla hlášena léková vyrážka s eozinofilií a systémovými příznaky (DRESS), včetně fatálních případů. Pokud je tento syndrom rozpoznán, lék by měl být okamžitě vysazen.
Antianabolické působení
Antianabolické působení tetracyklinů může způsobit zvýšení BUN. I když to není problém u pacientů s normální funkcí ledvin, u pacientů s významně narušenou funkcí mohou vyšší hladiny tetracyklinu v séru vést k azotemii, hyperfosfatémii a acidóze. Za těchto podmínek se doporučuje monitorování kreatininu a BUN a celková denní dávka by neměla překročit 200 mg za 24 hodin (viz DÁVKOVÁNÍ A PODÁVÁNÍ ). Pokud dojde k poškození ledvin, i obvyklé perorální nebo parenterální dávky mohou vést k systémové akumulaci léku a možné jaterní toxicitě.
Fotosenzitivita
U některých jedinců užívajících tetracykliny byla pozorována fotosenzitivita projevující se přehnanou reakcí na spálení sluncem. To bylo hlášeno u minocyklinu.
Účinky na centrální nervový systém
Při léčbě minocykliny byly hlášeny nežádoucí účinky na centrální nervový systém včetně točení hlavy, závrať nebo vertigo. Pacienti, kteří pociťují tyto příznaky, by měli být při léčbě minocykliny opatrní, aby řídili vozidla nebo obsluhovali nebezpečné stroje. Tyto příznaky mohou během léčby vymizet a obvykle rychle vymizí po vysazení léku.
Průjem spojený s Clostridium Difficile
Průjem spojený s Clostridium difficile (CDAD) byl hlášen při použití téměř všech antibakteriálních látek, včetně přípravku MINOCIN 50 mg, a jeho závažnost se může pohybovat od mírného průjmu až po fatální kolitidu. Léčba antibakteriálními látkami mění normální flóru tlustého střeva, což vede k přemnožení C. difficile.
C. difficile produkuje toxiny A a B, které přispívají k rozvoji CDAD. Kmeny C. difficile produkující hypertoxin způsobují zvýšenou morbiditu a mortalitu, protože tyto infekce mohou být odolné vůči antimikrobiální léčbě a mohou vyžadovat kolektomii. CDAD je třeba vzít v úvahu u všech pacientů, kteří mají průjem po užívání antibiotik. Je nutná pečlivá anamnéza, protože CDAD se objevilo více než dva měsíce po podání antibakteriálních látek.
Pokud je podezření na CDAD nebo je potvrzeno, může být nutné přerušit pokračující užívání antibiotik, která nejsou zaměřena proti C. difficile. Podle klinické indikace by měla být zahájena vhodná léčba tekutin a elektrolytů, suplementace proteinů, antibiotická léčba C. difficile a chirurgické vyšetření.
Přecitlivělost na siřičitan sodný
MINOCIN perorální suspenze obsahuje siřičitan sodný, siřičitan, který může u některých vnímavých osob způsobit reakce alergického typu včetně anafylaktických příznaků a život ohrožujících nebo méně závažných astmatických příhod. Celková prevalence sulfitové senzitivity v obecné populaci je neznámá a pravděpodobně nízká. Senzitivita na siřičitany je pozorována častěji u astmatiků než u neastmatických lidí.
Intrakraniální hypertenze
Intrakraniální hypertenze (IH, pseudotumor cerebri) je spojována s užíváním tetracyklinů včetně přípravku MINOCIN. Klinické projevy IH zahrnují bolest hlavy, rozmazané vidění, diplopii a ztrátu zraku; na fundoskopii lze nalézt papiledém. Ženy ve fertilním věku, které mají nadváhu nebo mají IH v anamnéze, jsou vystaveny většímu riziku rozvoje IH související s tetracyklinem. Je třeba se vyvarovat současného užívání isotretinoinu a MINOCINU, protože je také známo, že isotretinoin způsobuje pseudotumor cerebri.
Ačkoli IH obvykle odezní po přerušení léčby, existuje možnost trvalé ztráty zraku. Pokud se během léčby rozvinou zrakové příznaky, je zaručeno rychlé oftalmologické vyšetření. Vzhledem k tomu, že intrakraniální tlak může zůstat zvýšený ještě týdny po vysazení léku, měli by být pacienti sledováni, dokud se nestabilizují.
OPATŘENÍ
Všeobecné
Stejně jako u jiných antibiotických přípravků může použití tohoto léku vést k přemnožení necitlivých organismů, včetně plísní. Pokud dojde k superinfekci, antibiotika by měla být vysazena a měla by být zahájena vhodná léčba.
U minocyklinu byla hlášena hepatotoxicita; proto by měl být minocyklin používán s opatrností u pacientů s jaterní dysfunkcí a ve spojení s jinými hepatotoxickými léky.
Incize a drenáž nebo jiné chirurgické zákroky by měly být prováděny ve spojení s antibiotickou léčbou, pokud je to indikováno.
Je nepravděpodobné, že by předepsání perorální suspenze MINOCIN v nepřítomnosti prokázané nebo silně suspektní bakteriální infekce nebo profylaktické indikace přineslo pacientovi prospěch a zvýšilo riziko rozvoje bakterií rezistentních na léky.
Laboratorní testy
Měla by být prováděna pravidelná laboratorní vyšetření orgánových systémů, včetně hematopoetických, ledvinových a jaterních.
Všichni pacienti s kapavkou by měli mít v době diagnózy sérologické vyšetření na syfilis. Pacienti léčení minocyklinem by měli mít po 3 měsících kontrolní sérologické vyšetření na syfilis.
Interakce drog/laboratorních testů
V důsledku interference s fluorescenčním testem může dojít k falešnému zvýšení hladin katecholaminů v moči.
Karcinogeneze, mutageneze, zhoršení plodnosti
Dietní podávání minocyklinu v dlouhodobých studiích tumorigenicity u potkanů vedlo k průkazu produkce tumoru štítné žlázy. Bylo také zjištěno, že minocyklin způsobuje hyperplazii štítné žlázy u potkanů a psů. Kromě toho existují důkazy o onkogenní aktivitě u potkanů ve studiích s příbuzným antibiotikem, oxytetracyklinem (tj. nádory nadledvin a hypofýzy). Podobně, ačkoli nebyly provedeny studie mutagenity minocyklinu, byly hlášeny pozitivní výsledky in vitro testů savčích buněk (tj. myší lymfom a plicní buňky čínského křečka) pro příbuzná antibiotika (tetracyklin hydrochlorid a oxytetracyklin). Studie segmentu I (fertilita a obecná reprodukce) poskytly důkaz, že minocyklin zhoršuje plodnost u samců potkanů.
Těhotenství
Shrnutí rizik
Všechna těhotenství mají na pozadí riziko vrozených vad, ztráty nebo jiného nepříznivého výsledku bez ohledu na expozici léku. Neexistují žádné adekvátní a dobře kontrolované studie o použití minocyklinu u těhotných žen. Minocyklin, stejně jako jiná antibiotika třídy tetracyklinů, prochází placentou a může způsobit poškození plodu, když je podáván těhotné ženě. Po uvedení přípravku na trh byly hlášeny vzácné spontánní zprávy o vrozených anomáliích včetně zmenšení končetin. O těchto zprávách jsou k dispozici pouze omezené informace; nelze tedy stanovit žádný závěr o příčinné souvislosti. Pokud je minocyklin užíván během těhotenství nebo pokud pacientka otěhotní během užívání tohoto léku, pacientka by měla být informována o potenciálním riziku pro plod.
Neteratogenní účinky: (viz VAROVÁNÍ ).
Práce a dodání
Vliv tetracyklinů na porod není znám.
Kojící matky
Tetracykliny se vylučují do lidského mléka. Vzhledem k potenciálu závažných nežádoucích účinků tetracyklinů u kojených dětí je třeba rozhodnout, zda přerušit kojení nebo přerušit léčbu, přičemž je třeba vzít v úvahu důležitost léku pro matku (viz VAROVÁNÍ ).
Pediatrické použití
Minocyklin se nedoporučuje používat u dětí mladších 8 let, pokud očekávaný přínos léčby nepřeváží rizika (viz VAROVÁNÍ ).
Geriatrické použití
Klinické studie perorálního minocyklinu nezahrnovaly dostatečný počet subjektů ve věku 65 a více let, aby bylo možné určit, zda reagují odlišně od mladších subjektů. Obecně platí, že výběr dávky pro staršího pacienta by měl být opatrný, obvykle začíná na spodní hranici dávkovacího rozmezí, což odráží vyšší frekvenci snížené funkce jater, ledvin nebo srdce a souběžného onemocnění nebo jiné lékové terapie (viz VAROVÁNÍ , DÁVKOVÁNÍ A PODÁVÁNÍ ).
MINOCIN 50 mg perorální suspenze obsahuje 4,3 mg (0,18 mEq) sodíku na 5 ml.
PŘEDÁVKOVAT
Nežádoucí účinky častěji pozorované při předávkování jsou závratě, nevolnost a zvracení.
Není známo žádné specifické antidotum pro minocyklin.
V případě předávkování přerušte léčbu, ošetřete symptomaticky a zaveďte podpůrná opatření. Minocyklin není ve významných množstvích odstraněn hemodialýzou nebo peritoneální dialýzou.
KONTRAINDIKACE
Tento lék je kontraindikován u osob, u kterých se projevila přecitlivělost na některý z tetracyklinů nebo na kteroukoli složku přípravku.
KLINICKÁ FARMAKOLOGIE
Po jednorázové dávce dvou 100 mg tobolek naplněných práškem minocyklin HCl podané deseti normálním dospělým dobrovolníkům se hladiny v séru pohybovaly od 0,74 do 4,45 mcg/ml za 1 hodinu (průměr 2,24); po 12 hodinách se pohybovaly od 0,34 do 2,36 mcg/ml (průměr 1,25). Sérový poločas po jednorázové dávce 200 mg u 12 v podstatě normálních dobrovolníků se pohyboval od 11 do 17 hodin. U sedmi pacientů s jaterní dysfunkcí se pohybovala v rozmezí 11 až 16 hodin au 5 pacientů s renální dysfunkcí v rozmezí 18 až 69 hodin. Výtěžek minocyklinu v moči a stolici při podání 12 normálním dobrovolníkům byl poloviční až třetinový oproti jiným tetracyklinům.
Mikrobiologie
Mechanismus působení
Tetracykliny jsou primárně bakteriostatické a předpokládá se, že uplatňují svůj antimikrobiální účinek inhibicí syntézy proteinů. Tetracykliny, včetně minocyklinu, mají podobné antimikrobiální spektrum účinnosti proti širokému spektru grampozitivních a gramnegativních organismů. Běžná je zkřížená rezistence těchto organismů na tetracyklin.
Antimikrobiální aktivita
Bylo prokázáno, že minocyklin je účinný proti většině kmenů následujících mikroorganismů, a to jak in vitro, tak při klinických infekcích, jak je popsáno v INDIKACE sekce:
Gram-pozitivní bakterie
Bacillus anthracis Listeria monocytogenes Staphylococcus aureus Streptococcus pneumoniae
Gram-negativní bakterie
Bartonella bacilliformis Brucella druh Klebsiella granulomatis Campylobacter fetus Francisella tularensis Haemophilus ducreyi Vibrio cholerae Yersinia pestis Acinetobacter druh Enterobacter aerogenes Escherichia coli Haemophilus influenzae Klebsiella druh Neisseagelia mennoriss
Jiné mikroorganismy
Actinomyces druh Borrelia recurrentis Chlamydophila psittaci Chlamydia trachomatis Clostridium druh Entamoeba druh Fusobacterium nucleatum poddruh fusiforme Mycobacterium marinum Mycoplasma pneumoniae Propionibacterium acnes Rickettsiae Treponema pallidum Uponemalid poddruh pallidum
Testování citlivosti
Konkrétní informace týkající se interpretačních kritérií testu citlivosti a souvisejících testovacích metod a standardů kontroly kvality uznaných FDA pro tento lék naleznete na: https://www.fda.gov/STIC.
Farmakologie zvířat A Toxikologie
Bylo pozorováno, že minocyklin HCl způsobuje tmavé zbarvení štítné žlázy u experimentálních zvířat (krysy, miniprasata, psi a opice). U potkanů vedla chronická léčba hydrochloridem minocyklinu ke strumě doprovázené zvýšeným vychytáváním radioaktivního jódu a průkazem produkce tumoru štítné žlázy. Bylo také zjištěno, že hydrochlorid minocyklinu způsobuje hyperplazii štítné žlázy u potkanů a psů.
INFORMACE PRO PACIENTA
Průjem je častým problémem způsobeným antibiotiky, který obvykle končí, když je antibiotikum vysazeno. Někdy po zahájení léčby antibiotiky se u pacientů může vyvinout vodnatá a krvavá stolice (s žaludečními křečemi a horečkou nebo bez nich) dokonce až dva nebo více měsíců po užití poslední dávky antibiotika. Pokud k tomu dojde, pacienti by měli co nejdříve kontaktovat svého lékaře.
některých jedinců užívajících tetracykliny byla pozorována fotosenzitivita projevující se přehnanou reakcí na spálení sluncem. Pacienti, kteří jsou náchylní být vystaveni přímému slunečnímu záření nebo ultrafialovému světlu, by měli být upozorněni, že k této reakci může dojít u tetracyklinových léků, a léčba by měla být přerušena při prvních známkách kožního erytému. Tato reakce byla hlášena při použití minocyklinu.
Pacienti, kteří mají příznaky centrálního nervového systému, by měli být při léčbě minocykliny upozorněni na to, aby řídili vozidla nebo obsluhovali nebezpečné stroje (viz VAROVÁNÍ ).
Současné užívání tetracyklinu s perorálními kontraceptivy může snížit účinnost perorálních kontraceptiv (viz DROGOVÉ INTERAKCE ).
Pacienti by měli být poučeni, že antibakteriální léky včetně přípravku MINOCIN 50 mg perorální suspenze by měly být používány pouze k léčbě bakteriálních infekcí. Neléčí virové infekce (např. nachlazení). Když je MINOCIN perorální suspenze předepsána k léčbě bakteriální infekce, pacienti by měli být informováni, že ačkoli je běžné, že se na začátku léčby cítí lépe, lék by měl být užíván přesně podle pokynů. Vynechání dávek nebo nedokončení celé terapie může (1) snížit účinnost okamžité léčby a (2) zvýšit pravděpodobnost, že si bakterie vyvinou rezistenci a nebudou v budoucnu léčitelné přípravkem MINOCIN 50 mg perorální suspenze nebo jinými antibakteriálními léky. .
Nepoužité zásoby tetracyklinových antibiotik by měly být zlikvidovány do data expirace.
