Calan 40mg, 80mg, 120mg, 240mg Verapamil Použití, vedlejší účinky a dávkování. Cena v internetové lékárně. Generické léky bez předpisu.
Co je Calan 240 mg a jak se používá?
Calan 80 mg je lék na předpis používaný k léčbě příznaků vysokého krevního tlaku (hypertenze), bolesti na hrudi (angina pectoris) a některých poruch srdečního rytmu. Calan lze užívat samostatně nebo s jinými léky.
Calan patří do třídy léků nazývaných Antidysrytmika, IV; blokátory vápníkových kanálů; Blokátory vápníkových kanálů, nedihydropyridin.
Není známo, zda je Calan bezpečný a účinný u dětí.
Jaké jsou možné vedlejší účinky přípravku Calan?
Calan může způsobit závažné nežádoucí účinky, včetně:
- kopřivka,
- potíže s dýcháním,
- otok obličeje, rtů, jazyka nebo hrdla,
- bolest na hrudi,
- rychlý nebo pomalý srdeční tep,
- točení hlavy,
- dušnost,
- otok,
- rychlý nárůst hmotnosti
- ,
- horečka,
- bolest v horní části žaludku,
- necítím se dobře,
- úzkost,
- pocení,
- bledá kůže,
- sípání,
- lapal po dechu a
- kašel s napěněným hlenem
- nevolnost,
- zácpa,
- bolest hlavy,
- závratě a
- nízký krevní tlak
Pokud máte některý z výše uvedených příznaků, okamžitě vyhledejte lékařskou pomoc.
Mezi nejčastější vedlejší účinky přípravku Calan 80 mg patří:
Informujte lékaře, pokud máte jakýkoli nežádoucí účinek, který vás obtěžuje nebo který neustupuje.
To nejsou všechny možné vedlejší účinky Calanu. Pro více informací se zeptejte svého lékaře nebo lékárníka.
Zavolejte svého lékaře o radu ohledně nežádoucích účinků. Nežádoucí účinky můžete hlásit úřadu FDA na čísle 1-800-FDA-1088.
POPIS
CALAN (verapamil HCl) je inhibitor influxu kalciových iontů (blokátor pomalého kanálu nebo antagonista kalciových iontů) dostupný pro perorální podání ve filmem potahovaných tabletách obsahujících 40 mg, 80 mg nebo 120 mg verapamil hydrochloridu.
Strukturní vzorec verapamilu HCl je:
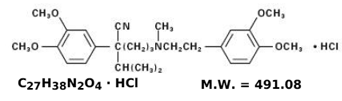 C27H38N2O4. HC1 MW = 491,08
C27H38N2O4. HC1 MW = 491,08 Benzenacetonitril, a-[3-[[2-(3,4-dimethoxyfenyl)ethyl]methylamino]propyl]-3,4dimethoxy-a-(1-methylethyl)hydrochlorid
Verapamil HCl je téměř bílý, krystalický prášek, prakticky bez zápachu, s hořkou chutí. Je rozpustný ve vodě, chloroformu a methanolu. Verapamil HCl není chemicky příbuzný s jinými kardioaktivními léky.
Neaktivní složky zahrnují mikrokrystalickou celulózu, kukuřičný škrob, želatinu, hydroxypropylcelulózu, hypromelózu, barvivo na bázi oxidu železa, laktózu, stearát hořečnatý, polyethylenglykol, mastek a oxid titaničitý.
INDIKACE
Tablety CALAN jsou indikovány k léčbě následujících onemocnění:
Angina
- Vasospastická (Prinzmetalova varianta) angina pectoris
- Nestabilní (crescendo, preinfarkt) angina pectoris
Arytmie
Esenciální hypertenze
CALAN 120 mg je indikován k léčbě hypertenze, ke snížení krevního tlaku. Snížení krevního tlaku snižuje riziko fatálních i nefatálních kardiovaskulárních příhod, především mozkových mrtvic a infarktů myokardu. Tyto přínosy byly pozorovány v kontrolovaných studiích antihypertenziv ze široké škály farmakologických tříd včetně tohoto léčiva.
Kontrola vysokého krevního tlaku by měla být součástí komplexního řízení kardiovaskulárních rizik, včetně kontroly lipidů, léčby diabetu, antitrombotické léčby, odvykání kouření, cvičení a omezeného příjmu sodíku. Mnoho pacientů bude k dosažení cílů krevního tlaku potřebovat více než jeden lék. Konkrétní rady ohledně cílů a managementu naleznete v publikovaných pokynech, jako jsou pokyny Společného národního výboru pro prevenci, detekci, hodnocení a léčbu vysokého krevního tlaku (JNC) Národního vzdělávacího programu pro vysoký krevní tlak.
randomizovaných kontrolovaných studiích bylo prokázáno, že četná antihypertenziva z různých farmakologických tříd a s různými mechanismy účinku snižují kardiovaskulární morbiditu a mortalitu a lze dojít k závěru, že se jedná o snížení krevního tlaku a ne o některé další farmakologické vlastnosti. léky, které jsou z velké části zodpovědné za tyto výhody. Největším a nejkonzistentnějším kardiovaskulárním přínosem bylo snížení rizika cévní mozkové příhody, ale pravidelně bylo také pozorováno snížení infarktu myokardu a kardiovaskulární mortality.
Zvýšený systolický nebo diastolický tlak způsobuje zvýšené kardiovaskulární riziko a zvýšení absolutního rizika na mmHg je větší při vyšších krevních tlacích, takže i mírné snížení těžké hypertenze může poskytnout podstatný přínos. Snížení relativního rizika snížením krevního tlaku je v populacích podobné s různým absolutním rizikem, takže absolutní přínos je větší u pacientů s vyšším rizikem nezávisle na jejich hypertenzi (například pacienti s diabetem nebo hyperlipidémií), u takových pacientů by se dalo očekávat těžit z agresivnější léčby k cíli nižšího krevního tlaku.
Některá antihypertenziva mají menší účinky na krevní tlak (jako monoterapie) u černošských pacientů a mnoho antihypertenziv má další schválené indikace a účinky (např. na anginu pectoris, srdeční selhání nebo diabetické onemocnění ledvin). Tyto úvahy mohou vést k výběru terapie.
DÁVKOVÁNÍ A PODÁVÁNÍ
Dávka verapamilu musí být individualizována titrací. Užitečnost a bezpečnost dávek přesahujících 480 mg/den nebyly stanoveny; proto by tato denní dávka neměla být překročena. Vzhledem k tomu, že poločas verapamilu se během chronického podávání zvyšuje, maximální odpověď může být opožděna.
Angina
Klinické studie ukazují, že obvyklá dávka je 80 mg až 120 mg třikrát denně. U pacientů, kteří mohou mít zvýšenou odpověď na verapamil (např. snížená funkce jater, starší pacienti atd.), však může být oprávněná dávka 40 mg třikrát denně. Titrace směrem nahoru by měla být založena na terapeutické účinnosti a bezpečnosti hodnocené přibližně osm hodin po podání dávky. Dávkování může být zvyšováno v denních (např. u pacientů s nestabilní anginou pectoris) nebo v týdenních intervalech, dokud není dosaženo optimální klinické odpovědi.
Arytmie
Dávkování u digitalizovaných pacientů s chronickou fibrilací síní (viz OPATŘENÍ ) se pohybuje od 240 do 320 mg/den v rozdělených (tid nebo qid) dávkách. Dávka pro profylaxi PSVT (nedigitalizovaní pacienti) se pohybuje od 240 do 480 mg/den v rozdělených (tid nebo qid) dávkách. Obecně platí, že maximální účinky pro jakoukoli danou dávku budou zřejmé během prvních 48 hodin terapie.
Esenciální hypertenze
Dávka by měla být individualizována titrací. Obvyklá počáteční monoterapeutická dávka v klinických studiích byla 80 mg třikrát denně (240 mg/den). Byly použity denní dávky 360 a 480 mg, ale neexistuje žádný důkaz, že by dávky přesahující 360 mg poskytovaly přidaný účinek. Je třeba zvážit zahájení titrace na 40 mg třikrát denně u pacientů, kteří mohou reagovat na nižší dávky, jako jsou starší lidé nebo lidé malého vzrůstu. Antihypertenzní účinky přípravku CALAN jsou patrné během prvního týdne léčby. Titrace směrem nahoru by měla být založena na terapeutické účinnosti hodnocené na konci dávkovacího intervalu.
JAK DODÁVÁNO
CALAN 40 mg tablety jsou kulaté, růžové, potahované, s vyraženým CALAN na jedné straně a 40 na druhé straně, dodávané jako:
CALAN 80 mg tablety jsou oválné, broskvové, s půlicí rýhou, potahované, s vyraženým CALAN na jedné straně a 80 na druhé straně, dodávané jako:
CALAN 120 mg tablety jsou oválné, hnědé, s půlicí rýhou, potahované, s vyraženým CALAN 120 na jedné straně, dodávané jako:
Uchovávejte při teplotě 59° až 77°F (15° až 25°C) a chraňte před světlem. Dávkujte v těsných, světlu odolných nádobách.
Distribuce: GD Searle LLC,Division Pfizer Inc,NY 10017. Revize: září 2017
VEDLEJŠÍ EFEKTY
Závažné nežádoucí účinky jsou méně časté, když je léčba přípravkem CALAN 40 mg zahájena titrací dávky směrem nahoru v rámci doporučené jednotlivé a celkové denní dávky. Vidět VAROVÁNÍ pro diskusi o srdečním selhání, hypotenzi, zvýšených jaterních enzymech, AV blokádě a rychlé ventrikulární reakci. V souvislosti s užíváním verapamilu byl zřídka hlášen reverzibilní (po vysazení verapamilu) neobstrukční paralytický ileus. Následující reakce na perorálně podávaný verapamil se vyskytly s četností vyšší než 1,0 % nebo se vyskytly s nižší četností, ale v klinických studiích u 4 954 pacientů se jevily jasně související s lékem:
klinických studiích týkajících se kontroly ventrikulární odpovědi u digitalizovaných pacientů, kteří měli fibrilaci nebo flutter síní, se frekvence komor pod 50 v klidu vyskytla u 15 % pacientů a asymptomatická hypotenze se vyskytla u 5 % pacientů.
Následující reakce, hlášené u 1,0 % nebo méně pacientů, se objevily za podmínek (otevřené studie, marketingové zkušenosti), kdy je kauzální vztah nejistý; jsou uvedeny, aby upozornily lékaře na možný vztah:
Kardiovaskulární: angina pectoris, atrioventrikulární disociace, bolest na hrudi, klaudikace, infarkt myokardu, palpitace, purpura (vaskulitida), synkopa.
Zažívací ústrojí: průjem, sucho v ústech, gastrointestinální potíže, gingivální hyperplazie.
Hemické a lymfatické: ekchymóza nebo modřiny.
Nervový systém: cévní mozková příhoda, zmatenost, poruchy rovnováhy, nespavost, svalové křeče, parestézie, psychotické symptomy, třes, somnolence, extrapyramidové symptomy.
Kůže: artralgie a vyrážka, exantém, vypadávání vlasů, hyperkeratóza, makuly, pocení, kopřivka, Stevens-Johnsonův syndrom, erythema multiforme.
Speciální smysly: rozmazané vidění, tinnitus.
Urogenitální: gynekomastie, galaktorea/hyperprolaktinémie, zvýšené močení, flekatá menstruace, impotence.
Léčba akutních kardiovaskulárních nežádoucích reakcí
Frekvence kardiovaskulárních nežádoucích účinků, které vyžadují léčbu, je vzácná; zkušenosti s jejich léčbou jsou proto omezené. Kdykoli se po perorálním podání verapamilu objeví těžká hypotenze nebo úplná AV blokáda, je třeba okamžitě použít příslušná naléhavá opatření; např. intravenózně podaný norepinefrin bitartrát, atropin sulfát, isoproterenol HCl (vše v obvyklých dávkách) nebo glukonát vápenatý (10% roztok). U pacientů s hypertrofickou kardiomyopatií (IHSS) je třeba k udržení krevního tlaku používat alfa-adrenergní látky (fenylefrin HCl, metaraminolbitartrát nebo metoxamin HCl) a je třeba se vyhnout isoproterenolu a noradrenalinu. Pokud je nutná další podpora, lze podat dopamin HCl nebo dobutamin HCl. Skutečná léčba a dávkování by měly záviset na závažnosti klinické situace a úsudku a zkušenostech ošetřujícího lékaře.
DROGOVÉ INTERAKCE
Induktory/inhibitory cytochromů
Metabolické studie in vitro ukazují, že verapamil je metabolizován cytochromem P450 CYP3A4, CYP1A2, CYP2C8, CYP2C9 a CYP2C18. Klinicky významné interakce byly hlášeny s inhibitory CYP3A4 (např. erythromycinem, ritonavirem), které způsobily zvýšení plazmatických hladin verapamilu, zatímco induktory CYP3A4 (např. rifampin) způsobily snížení plazmatických hladin verapamilu.
Inhibitory HMG-CoA reduktázy
Použití inhibitorů HMG-CoA reduktázy, které jsou substráty CYP3A4, v kombinaci s verapamilem bylo spojeno s hlášeními myopatie/rhabdomyolýzy.
Současné podávání opakovaných dávek 10 mg verapamilu s 80 mg simvastatinu vedlo k expozici simvastatinu 2,5krát vyšší než po samotném simvastatinu. Omezte dávku simvastatinu u pacientů užívajících verapamil na 10 mg denně. Omezte denní dávku lovastatinu na 40 mg. Mohou být nutné nižší počáteční a udržovací dávky jiných substrátů CYP3A4 (např. atorvastatinu), protože verapamil může zvýšit plazmatickou koncentraci těchto léků.
ivabradin
Současné užívání verapamilu zvyšuje expozici ivabradinu a může zhoršit bradykardii a poruchy vedení vzruchu. Vyhněte se současnému podávání verapamilu a ivabradinu.
Aspirin
V několika hlášených případech vedlo současné podávání verapamilu s aspirinem ke zvýšení doby krvácení delší, než bylo pozorováno u samotného aspirinu.
Grepový džus
Grapefruitová šťáva může zvýšit plazmatické hladiny verapamilu.
Alkohol
Verapamil může zvýšit koncentraci alkoholu v krvi a prodloužit jeho účinky.
Beta-blokátory
Kontrolované studie na malém počtu pacientů naznačují, že současné užívání přípravku CALAN 120 mg a perorálních beta-adrenergních blokátorů může být prospěšné u některých pacientů s chronickou stabilní anginou pectoris nebo hypertenzí, ale dostupné informace nejsou dostatečné pro spolehlivé předpovídání účinků souběžné léčby u pacientů s dysfunkcí levé komory nebo abnormalitami srdečního vedení. Současná léčba beta-adrenergními blokátory a verapamilem může mít za následek aditivní negativní účinky na srdeční frekvenci, atrioventrikulární vedení a/nebo srdeční kontraktilitu.
jedné studii zahrnující 15 pacientů léčených vysokými dávkami propranololu (střední dávka: 480 mg/den; rozmezí: 160 až 1 280 mg/den) pro těžkou anginu pectoris se zachovanou funkcí levé komory (ejekční frakce větší než 35 %) byla hemodynamická účinky další terapie verapamilem HCl byly hodnoceny pomocí invazivních metod. Přidání verapamilu k vysokým dávkám beta-blokátorů vyvolalo mírné negativní inotropní a chronotropní účinky, které nebyly dostatečně závažné, aby omezily krátkodobou (48 hodin) kombinovanou terapii v této studii. Tyto mírné kardiodepresivní účinky přetrvávaly déle než 6, ale méně než 30 hodin po náhlém vysazení beta-blokátorů a úzce souvisely s plazmatickými hladinami propranololu. Primární interakce verapamil/beta-blokátor v této studii se zdála být spíše hemodynamická než elektrofyziologická.
jiných studiích verapamil obecně nevyvolával signifikantní negativní inotropní, chronotropní nebo dromotropní účinky u pacientů se zachovanou funkcí levé komory, kteří dostávali nízké nebo střední dávky propranololu (méně než nebo rovné 320 mg/den); u některých pacientů však kombinovaná terapie takové účinky skutečně vyvolala. Proto, pokud se používá kombinovaná léčba, je třeba pečlivě sledovat klinický stav. Kombinované léčbě je třeba se obvykle vyhnout u pacientů s abnormalitami atrioventrikulárního vedení au pacientů s útlumem funkce levé komory.
Asymptomatická bradykardie (36 tepů/min) s bludným síňovým kardiostimulátorem byla pozorována u pacienta užívajícího současně timolol (beta-adrenergní blokátor) oční kapky a perorální verapamil.
Snížení clearance metoprololu a propranololu bylo pozorováno při současném podávání obou léčiv s verapamilem. Při současném podávání verapamilu a atenololu byl pozorován proměnlivý účinek.
Digitální
Klinické použití verapamilu u digitalizovaných pacientů ukázalo, že tato kombinace je dobře tolerována, pokud jsou dávky digoxinu správně upraveny. Chronická léčba verapamilem však může během prvního týdne léčby zvýšit hladiny digoxinu v séru o 50 % až 75 %, což může vést k toxicitě digitalisu. U pacientů s jaterní cirhózou je vliv verapamilu na kinetiku digoxinu zesílen. Verapamil může snížit celkovou tělesnou clearance a extrarenální clearance digitoxinu o 27 %, resp. 29 %. Při podávání verapamilu by měly být sníženy udržovací a digitalizační dávky a pacient by měl být znovu posouzen, aby se zabránilo nadměrné nebo nedostatečné digitalizaci. Kdykoli existuje podezření na nadměrnou digitalizaci, měla by být denní dávka digitalisu snížena nebo dočasně přerušena. Při přerušení užívání přípravku CALAN 80 mg by měl být pacient znovu vyhodnocen, aby se zabránilo nedostatečné digitalizaci.
Antihypertenziva
Verapamil podávaný současně s perorálními antihypertenzivy (např. vazodilatátory, inhibitory angiotenzin-konvertujícího enzymu, diuretika, beta-blokátory) bude mít obvykle aditivní účinek na snížení krevního tlaku. Pacienti užívající tyto kombinace by měli být náležitě sledováni. Současné užívání látek, které tlumí alfa-adrenergní funkci, s verapamilem může vést ke snížení krevního tlaku, které je u některých pacientů nadměrné. Takový účinek byl pozorován v jedné studii po současném podávání verapamilu a prazosinu.
Antiarytmická činidla
disopyramid
Dokud nebudou získány údaje o možných interakcích mezi verapamilem a disopyramidem, neměl by být disopyramid podáván během 48 hodin před nebo 24 hodin po podání verapamilu.
Flekainid
Studie na zdravých dobrovolnících ukázala, že současné podávání flekainidu a verapamilu může mít aditivní účinky na kontraktilitu myokardu, AV vedení a repolarizaci. Současná léčba flekainidem a verapamilem může vést k aditivnímu negativně inotropnímu účinku a prodloužení atrioventrikulárního vedení.
Chinidin
U malého počtu pacientů s hypertrofickou kardiomyopatií (IHSS) vedlo současné užívání verapamilu a chinidinu k významné hypotenzi. Do doby, než budou získány další údaje, je pravděpodobně třeba se vyhnout kombinované léčbě verapamilem a chinidinem u pacientů s hypertrofickou kardiomyopatií.
Elektrofyziologické účinky chinidinu a verapamilu na AV vedení byly studovány u 8 pacientů. Verapamil významně působil proti účinkům chinidinu na AV vedení. Během léčby verapamilem byly hlášeny zvýšené hladiny chinidinu.

Ostatní agenti
Dusičnany
Verapamil byl podáván současně s krátkodobě a dlouhodobě působícími nitráty bez jakýchkoli nežádoucích lékových interakcí. Farmakologický profil obou léků a klinické zkušenosti naznačují příznivé interakce.
Cimetidin
Interakce mezi cimetidinem a chronicky podávaným verapamilem nebyla studována. V akutních studiích na zdravých dobrovolnících byly získány různé výsledky clearance; clearance verapamilu byla buď snížena nebo nezměněna.
Lithium
Při souběžné léčbě verapamilem-lithiem byla hlášena zvýšená citlivost na účinky lithia (neurotoxicita); bylo pozorováno, že hladiny lithia se někdy zvyšují, někdy snižují a někdy se nemění. Pacienti užívající oba léky musí být pečlivě sledováni.
karbamazepin
Léčba verapamilem může během kombinované léčby zvýšit koncentrace karbamazepinu. To může vyvolat vedlejší účinky karbamazepinu, jako je diplopie, bolest hlavy, ataxie nebo závratě.
rifampin
Léčba rifampinem může výrazně snížit biologickou dostupnost perorálního verapamilu.
fenobarbital
Léčba fenobarbitalem může zvýšit clearance verapamilu.
Cyklosporin
Léčba verapamilem může zvýšit sérové hladiny cyklosporinu.
Theofylin
Verapamil může inhibovat clearance a zvyšovat plazmatické hladiny theofylinu.
Inhalační anestetika
Pokusy na zvířatech ukázaly, že inhalační anestetika snižují kardiovaskulární aktivitu tím, že snižují pohyb iontů vápníku dovnitř. Při současném použití je třeba pečlivě titrovat inhalační anestetika a antagonisty vápníku, jako je verapamil, aby se zabránilo nadměrné kardiovaskulární depresi.
Neuromuskulární blokátory
Klinické údaje a studie na zvířatech naznačují, že verapamil může potencovat aktivitu neuromuskulárních blokátorů (podobných kurare a depolarizujících). Při současném užívání léků může být nutné snížit dávku verapamilu a/nebo dávku neuromuskulárního blokátoru.
telithromycin
Hypotenze a bradyarytmie byly pozorovány u pacientů užívajících současně telithromycin, antibiotikum ze třídy ketolidů.
klonidin
V souvislosti s užíváním klonidinu současně s verapamilem byla hlášena sinusová bradykardie vedoucí k hospitalizaci a zavedení kardiostimulátoru. Monitorujte srdeční frekvenci u pacientů užívajících současně verapamil a klonidin.
Inhibitory savčího cíle rapamycinu (mTOR).
Ve studii s 25 zdravými dobrovolníky, kterým byl současně podáván verapamil se sirolimem, byly Cmax sirolimu v plné krvi zvýšeny o 130 % a AUC o 120 %. Cmax a AUC S-(-) verapamilu v plazmě byly zvýšeny o 50 %. Současné podávání verapamilu s everolimem 16 zdravým dobrovolníkům zvýšilo Cmax everolimu o 130 % a AUC o 250 %. Při současném užívání inhibitorů mTOR (např. sirolimu, temsirolimu a everolimu) a verapamilu zvažte vhodné snížení dávek obou léků.
VAROVÁNÍ
Srdeční selhání
Verapamil má negativně inotropní účinek, který je u většiny pacientů kompenzován vlastnostmi snížení afterloadu (snížení systémové vaskulární rezistence) bez čistého zhoršení komorové výkonnosti. Podle klinických zkušeností se 4 954 pacienty se u 87 (1,8 %) vyvinulo městnavé srdeční selhání nebo plicní edém. Verapamil by se neměl používat u pacientů se závažnou dysfunkcí levé komory (např. ejekční frakce nižší než 30 %) nebo středně těžkými až závažnými příznaky srdečního selhání a u pacientů s jakýmkoli stupněm komorové dysfunkce, pokud užívají beta-adrenergní blokátory (viz DROGOVÉ INTERAKCE ). Pacienti s mírnější komorovou dysfunkcí by měli být pokud možno před léčbou verapamilem kontrolováni optimálními dávkami digitalisu a/nebo diuretik. ( Všimněte si interakce s digoxinem v části BEZPEČNOSTNÍ OPATŘENÍ )
Hypotenze
Farmakologický účinek verapamilu může příležitostně způsobit pokles krevního tlaku pod normální hodnoty, což může vést k závratím nebo symptomatické hypotenzi. Incidence hypotenze pozorovaná u 4 954 pacientů zařazených do klinických studií byla 2,5 %. U hypertoniků je pokles krevního tlaku pod normální hodnotu neobvyklé. Testování na naklápěcím stole (60 stupňů) nebylo schopno vyvolat ortostatickou hypotenzi.
Zvýšené jaterní enzymy
Bylo hlášeno zvýšení transamináz se současným zvýšením alkalické fosfatázy a bilirubinu nebo bez něj. Taková zvýšení byla někdy přechodná a mohou vymizet i při pokračující léčbě verapamilem. Několik případů hepatocelulárního poškození souvisejícího s verapamilem bylo prokázáno opětovným podáním; polovina z nich měla kromě zvýšení SGOT, SGPT a alkalické fosfatázy klinické příznaky (nevolnost, horečka a/nebo bolest v pravém horním kvadrantu). U pacientů užívajících verapamil je proto rozumné pravidelně sledovat jaterní funkce.
Obtokový trakt příslušenství (Wolff-Parkinson-White nebo Lown-Ganong-Levine)
některých pacientů s paroxysmální a/nebo chronickou fibrilací síní nebo flutterem síní a koexistující přídatnou AV dráhou se vyvinulo zvýšené antegrádní vedení přes přídatnou dráhu obcházející AV uzel, což vyvolalo velmi rychlou komorovou odpověď nebo komorovou fibrilaci po intravenózním podání verapamilu (nebo digitalisu). . Ačkoli riziko tohoto výskytu u perorálního verapamilu nebylo stanoveno, tito pacienti užívající perorální verapamil mohou být ohroženi a jeho použití u těchto pacientů je kontraindikováno (viz KONTRAINDIKACE ). Léčba je obvykle DC-kardioverze. Po perorálním podání CALANu byla bezpečně a účinně použita kardioverze.
Atrioventrikulární blok
Účinek verapamilu na AV vedení a SA uzel může způsobit asymptomatickou AV blokádu 1. stupně a přechodnou bradykardii, někdy doprovázenou uzlovými únikovými rytmy. Prodloužení PR-intervalu koreluje s plazmatickými koncentracemi verapamilu, zejména během časné titrační fáze terapie. Vyšší stupně AV blokády však byly pozorovány zřídka (0,8 %). Výrazná blokáda prvního stupně nebo progresivní vývoj do AV blokády druhého nebo třetího stupně vyžaduje v závislosti na klinické situaci snížení dávky nebo ve vzácných případech vysazení verapamilu HCl a zahájení vhodné léčby.
Pacienti s hypertrofickou kardiomyopatií (IHSS)
A120 pacientů s hypertrofickou kardiomyopatií (většina z nich refrakterních nebo netolerujících propranolol), kteří dostávali léčbu verapamilem v dávkách až 720 mg/den, byly pozorovány různé závažné nežádoucí účinky. Tři pacienti zemřeli na plicní edém; všichni měli těžkou obstrukci výtoku levé komory a v anamnéze dysfunkci levé komory. Osm dalších pacientů mělo plicní edém a/nebo těžkou hypotenzi; U většiny těchto pacientů byl přítomen abnormálně vysoký (vyšší než 20 mm Hg) plicní tlak v zaklínění a výrazná obstrukce výtoku levé komory. Současné podávání chinidinu (viz OPATŘENÍ , DROGOVÉ INTERAKCE předcházela těžké hypotenzi u 3 z 8 pacientů (u 2 z nich se rozvinul plicní edém). Sinusová bradykardie se vyskytla u 11 % pacientů, AV blokáda 2. stupně u 4 % a sinusová zástava u 2 %. Je třeba ocenit, že tato skupina pacientů měla závažné onemocnění s vysokou mortalitou. Většina nežádoucích účinků dobře reagovala na snížení dávky a jen zřídka muselo být užívání verapamilu přerušeno.
OPATŘENÍ
Všeobecné
Použití u pacientů s poruchou funkce jater
Vzhledem k tomu, že verapamil je vysoce metabolizován v játrech, měl by být pacientům s poruchou funkce jater podáván s opatrností. Těžká jaterní dysfunkce prodlužuje poločas eliminace verapamilu na přibližně 14 až 16 hodin; proto by těmto pacientům mělo být podáno přibližně 30 % dávky podané pacientům s normální funkcí jater. Pečlivé sledování abnormálního prodloužení PR intervalu nebo jiných známek nadměrných farmakologických účinků (viz PŘEDÁVKOVAT ) by mělo být provedeno.
Použití u pacientů s oslabeným (sníženým) neuromuskulárním přenosem
Bylo hlášeno, že verapamil snižuje neuromuskulární přenos u pacientů s Duchennovou svalovou dystrofií, prodlužuje zotavení z neuromuskulárního blokátoru vekuronia a způsobuje zhoršení myasthenia gravis. Může být nutné snížit dávku verapamilu, pokud je podáván pacientům s oslabeným nervosvalovým přenosem.
Použití u pacientů s poruchou funkce ledvin
Asi 70 % podané dávky verapamilu se vylučuje ve formě metabolitů močí. Verapamil nelze odstranit hemodialýzou. Dokud nebudou k dispozici další údaje, měl by být verapamil podáván pacientům s poruchou funkce ledvin opatrně. U těchto pacientů je třeba pečlivě sledovat abnormální prodloužení PR intervalu nebo jiné známky předávkování (viz PŘEDÁVKOVAT ).
Karcinogeneze, mutageneze, zhoršení plodnosti
18měsíční studie toxicity na potkanech s nízkým násobkem (6násobkem) maximální doporučené dávky pro člověka, a nikoli maximální tolerované dávky, nenaznačila tumorigenní potenciál. Nebyly žádné důkazy o karcinogenním potenciálu verapamilu podávaného ve stravě potkanů po dobu dvou let v dávkách 10, 35 a 120 mg/kg/den nebo přibližně 1, 3,5 a 12násobku maximální doporučené denní dávky u člověka dávka (480 mg/den nebo 9,6 mg/kg/den).
Verapamil nebyl mutagenní v Amesově testu u 5 testovacích kmenů při 3 mg na plotnu s metabolickou aktivací nebo bez ní.
Studie u samic potkanů při denních dietních dávkách až 5,5násobku (55 mg/kg/den) maximální doporučené dávky pro člověka neprokázaly zhoršenou fertilitu. Účinky na mužskou fertilitu nebyly stanoveny.
Těhotenství
Reprodukční studie byly provedeny na králících a potkanech při perorálních dávkách až 1,5 (15 mg/kg/den) a 6 (60 mg/kg/den) násobku perorální denní dávky u člověka a neodhalily žádné známky teratogenity. U potkanů byl však tento násobek lidské dávky embryocidní a zpomalil růst a vývoj plodu, pravděpodobně kvůli nepříznivým účinkům na matku, které se odrážely ve snížených přírůstcích hmotnosti samic. Bylo také prokázáno, že tato perorální dávka způsobuje hypotenzi u potkanů. Neexistují žádné adekvátní a dobře kontrolované studie u těhotných žen. Vzhledem k tomu, že reprodukční studie na zvířatech nejsou vždy prediktivní pro lidskou odpověď, měl by být tento lék používán během těhotenství pouze tehdy, je-li to nezbytně nutné. Verapamil prochází placentární bariérou a může být detekován v krvi z pupečníkové žíly při porodu.
Práce a dodání
Není známo, zda má použití verapamilu během porodu okamžité nebo opožděné nepříznivé účinky na plod, nebo zda prodlužuje trvání porodu nebo zvyšuje potřebu porodu kleštěmi nebo jiné porodnické intervence. Takové nežádoucí účinky nebyly v literatuře popsány, navzdory dlouhé historii používání verapamilu v Evropě při léčbě srdečních vedlejších účinků beta-adrenergních agonistických látek používaných k léčbě předčasného porodu.
Kojící matky
Verapamil se vylučuje do lidského mléka. Vzhledem k možnosti nežádoucích účinků verapamilu u kojených dětí by mělo být kojení během podávání verapamilu přerušeno.
Pediatrické použití
Bezpečnost a účinnost u pediatrických pacientů nebyla stanovena.
PŘEDÁVKOVAT
Všechny předávkování verapamilem považujte za závažné a udržujte pozorování po dobu nejméně 48 hodin (zejména CALAN 120 mg SR), nejlépe v nepřetržité nemocniční péči. U lékové formy s prodlouženým uvolňováním se mohou objevit opožděné farmakodynamické důsledky. Je známo, že verapamil zkracuje dobu průchodu gastrointestinálním traktem.
Léčba předávkování by měla být podpůrná. Beta-adrenergní stimulace nebo parenterální podávání roztoků vápníku může zvýšit tok iontů vápníku přes pomalý kanál a byly účinně použity při léčbě úmyslného předávkování verapamilem. V několika hlášených případech bylo předávkování blokátory kalciových kanálů spojeno s hypotenzí a bradykardií, zpočátku refrakterní na atropin, ale stále citlivější na tuto léčbu, když pacienti dostávali velké dávky (blízko 1 gramu/hodinu po dobu delší než 24 hodin) chlorid vápenatý. Verapamil nelze odstranit hemodialýzou. Klinicky významné hypotenzní reakce nebo AV blokáda vysokého stupně by měly být léčeny vazopresorickými látkami nebo kardiostimulací. Asystolii je třeba řešit obvyklými opatřeními včetně kardiopulmonální resuscitace.
KONTRAINDIKACE
Tablety Verapamil HCl jsou kontraindikovány u:
KLINICKÁ FARMAKOLOGIE
CALAN 80mg je inhibitor influxu vápníkových iontů (blokátor pomalého kanálu nebo antagonista vápníkových iontů), který uplatňuje své farmakologické účinky modulací přítoku iontového vápníku přes buněčnou membránu arteriálního hladkého svalstva a také ve vodivých a kontraktilních buňkách myokardu.
Mechanismus působení
Angina
Přesný mechanismus účinku přípravku CALAN 40mg jako antianginózního činidla musí být plně určen, ale zahrnuje následující dva mechanismy:
Není jasné, zda tento účinek hraje nějakou roli u klasické námahové anginy pectoris, ale studie tolerance zátěže neprokázaly zvýšení součinu maximální zátěžové frekvence a tlaku, což je široce přijímaná míra využití kyslíku. To naznačuje, že obecně není úleva od spasmu nebo dilatace koronárních tepen důležitým faktorem u klasické anginy pectoris.
Arytmie
Elektrická aktivita přes AV uzel závisí do značné míry na přítoku vápníku pomalým kanálem. Snížením přítoku vápníku prodlužuje CALAN 120 mg účinnou refrakterní periodu v AV uzlu a zpomaluje AV vedení v závislosti na frekvenci. Tato vlastnost odpovídá za schopnost přípravku CALAN 240 mg zpomalit komorovou frekvenci u pacientů s chronickým flutterem síní nebo fibrilací síní.
Normální sinusový rytmus obvykle není ovlivněn, ale u pacientů se syndromem nemocného sinu může CALAN interferovat s generováním impulsu sinusového uzlu a může vyvolat zástavu sinusu nebo sinoatriální blokádu. Atrioventrikulární blokáda se může objevit u pacientů bez preexistujících poruch vedení (viz VAROVÁNÍ ). CALAN 240 mg snižuje frekvenci epizod paroxysmální supraventrikulární tachykardie.
CALAN 240 mg nemění normální síňový akční potenciál ani dobu intraventrikulárního vedení, ale u snížených síňových vláken snižuje amplitudu, rychlost depolarizace a rychlost vedení. CALAN může zkrátit antegrádní efektivní refrakterní periodu akcesorního bypassového traktu. U pacientů s flutterem síní nebo fibrilací síní a koexistující přídatnou AV cestou po podání verapamilu byla hlášena akcelerace komorové frekvence a/nebo fibrilace komor (viz VAROVÁNÍ ).
CALAN má lokální anestetický účinek, který je 1,6krát vyšší než prokain na ekvimolárním základě. Není známo, zda je tento účinek důležitý v dávkách používaných u člověka.
Esenciální hypertenze
CALAN 120 mg má antihypertenzní účinky snížením systémové vaskulární rezistence, obvykle bez ortostatického snížení krevního tlaku nebo reflexní tachykardie; bradykardie (frekvence nižší než 50 tepů/min) je méně častá (1,4 %). Během izometrického nebo dynamického cvičení CALAN nemění systolickou srdeční funkci u pacientů s normální funkcí komor.
CALAN nemění celkové hladiny vápníku v séru. Jedna zpráva však naznačila, že hladiny vápníku nad normálním rozmezím mohou změnit terapeutický účinek přípravku CALAN.
Farmakokinetika a metabolismus
Absorbuje se více než 90 % perorálně podané dávky CALANu. Vzhledem k rychlé biotransformaci verapamilu během jeho prvního průchodu portálním oběhem se biologická dostupnost pohybuje od 20 % do 35 %. Maximální plazmatické koncentrace je dosaženo za 1 až 2 hodiny po perorálním podání. Chronické perorální podávání 120 mg verapamilu HCl každých 6 hodin vedlo k plazmatickým hladinám verapamilu v rozmezí od 125 do 400 ng/ml, přičemž občas byly hlášeny vyšší hodnoty. Existuje nelineární korelace mezi podanou dávkou verapamilu a plazmatickými hladinami verapamilu. Nebyl stanoven žádný vztah mezi plazmatickou koncentrací verapamilu a snížením krevního tlaku. Při časné titraci dávky verapamilu existuje vztah mezi plazmatickou koncentrací verapamilu a prodloužením PR intervalu. Při chronickém podávání však může tento vztah vymizet. Průměrný poločas eliminace ve studiích s jednorázovou dávkou se pohyboval od 2,8 do 7,4 hodin. Ve stejných studiích se po opakovaném podávání zvýšil poločas na rozmezí 4,5 až 12,0 hodin (po méně než 10 po sobě jdoucích dávkách podaných s odstupem 6 hodin). Poločas verapamilu se může během titrace prodloužit. Stárnutí může ovlivnit farmakokinetiku verapamilu. U starších pacientů může být poločas eliminace prodloužen. U zdravých mužů podléhá perorálně podávaný CALAN 240 mg rozsáhlému metabolismu v játrech. V plazmě bylo identifikováno dvanáct metabolitů; všechny kromě norverapamilu jsou přítomny pouze ve stopových množstvích. Norverapamil může dosáhnout plazmatických koncentrací v ustáleném stavu přibližně rovných koncentracím samotného verapamilu. Kardiovaskulární aktivita norverapamilu se zdá být přibližně 20 % aktivity verapamilu. Přibližně 70 % podané dávky se vyloučí ve formě metabolitů v moči a 16 % nebo více ve stolici během 5 dnů. Asi 3 až 4 % se vyloučí močí jako nezměněné léčivo. Přibližně 90 % se váže na plazmatické bílkoviny. U pacientů s jaterní insuficiencí je metabolismus zpožděn a poločas eliminace prodloužen až na 14 až 16 hodin (viz OPATŘENÍ ); distribuční objem se zvýší a plazmatická clearance se sníží na přibližně 30 % normálu. Hodnoty clearance verapamilu naznačují, že pacienti s jaterní dysfunkcí mohou dosáhnout terapeutických plazmatických koncentrací verapamilu s jednou třetinou perorální denní dávky potřebné pro pacienty s normální funkcí jater.
Po čtyřech týdnech perorálního dávkování (120 mg qid) byly v mozkomíšním moku zaznamenány hladiny verapamilu a norverapamilu s odhadovaným rozdělovacím koeficientem 0,06 pro verapamil a 0,04 pro norverapamil.
Hemodynamika a metabolismus myokardu
CALAN 120 mg snižuje afterload a kontraktilitu myokardu. Zlepšená diastolická funkce levé komory u pacientů s idiopatickou hypertrofickou subaortální stenózou (IHSS) au pacientů s koronárním srdečním onemocněním byla také pozorována při léčbě přípravkem CALAN. U většiny pacientů, včetně pacientů s organickým srdečním onemocněním, je negativně inotropní účinek CALAN 240 mg vyrovnán snížením afterloadu a srdeční index obvykle není snížen. U pacientů se závažnou dysfunkcí levé komory (např. tlak v zaklínění plic nad 20 mm Hg nebo ejekční frakce nižší než 30 %) nebo u pacientů užívajících beta-adrenergní blokátory nebo jiná kardiodepresiva se však může objevit zhoršení funkce komory (viz DROGOVÉ INTERAKCE ).
Plicní funkce
CALAN 120 mg nevyvolává bronchokonstrikci, a proto nenarušuje ventilační funkci.
Farmakologie zvířat a/nebo toxikologie zvířat
chronických toxikologických studiích na zvířatech způsoboval verapamil změny lentikulární a/nebo šicí linie při dávkách 30 mg/kg/den nebo vyšších a u psů bíglů, ale ne u potkanů, kataraktu při 62,5 mg/kg/den nebo vyšších. Rozvoj katarakty v důsledku verapamilu nebyl u člověka hlášen.
INFORMACE PRO PACIENTA
Nebyly poskytnuty žádné informace. Podívejte se prosím na VAROVÁNÍ a OPATŘENÍ sekce.
